 研发追踪
研发追踪
 药明康德
药明康德
 2023.09.18
2023.09.18
 2083
2083
Madrigal Pharmaceuticals今日宣布,美国FDA已接受其在研药品resmetirom治疗伴有肝纤维化的非酒精性脂肪性肝炎(NASH)成人患者的新药申请(NDA),并授予优先审评资格。FDA预计于2024年3月14日前完成审评。
NASH是非酒精性脂肪性肝病(NAFLD)的更晚期形式。据估计,全球超过20%的成年人患有NAFLD。NASH是导致肝脏相关死亡的主要原因,对全球卫生系统造成日益加重的负担。此外,NASH患者,特别是那些具有更多代谢风险因素(高血压、合并2型糖尿病)的患者,心血管不良事件的风险增加,发病率和死亡率也相应提高。一旦NASH发展为显著的肝纤维化(F2和F3阶段),患者产生不良肝损伤结果的风险急剧上升。
Resmetirom是一种每日一次、口服、甲状腺激素受体(THR)-β选择性激动剂,旨在靶向NASH的关键基础病因。甲状腺激素通过激活肝细胞中的β受体,在肝功能中发挥核心作用,影响从血清胆固醇和甘油三酯水平,到肝脏中脂肪病理性积聚等一系列健康参数。THR-β受体在肝脏中的作用是肝脏正常功能的关键。Resmetirom具有高选择性,能够避免激活介导肝脏外(包括心脏和骨骼)甲状腺激素活性的THR-α受体,并且在肝脏部位被特异性摄取。之前的试验证实resmetirom的安全性,即对THR-α受体无活性,对骨骼或心脏参数无影响,同时不影响甲状腺激素通路的其它激素。
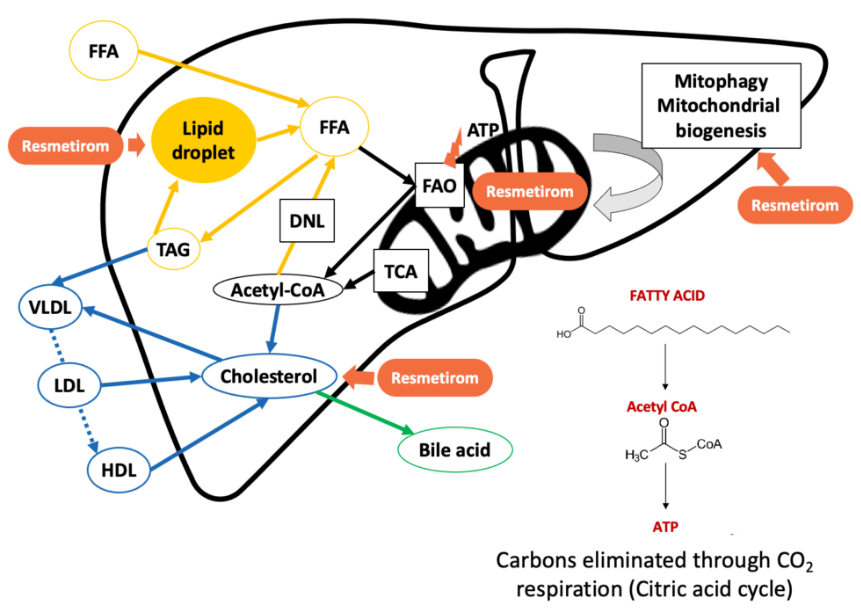
▲Resmetirom作用机制(图片来源:Madrigal Pharmaceuticals官网)
去年12月,Madrigal Pharmaceuticals公司宣布关键性临床试验MAESTRO-NASH达到组织学主要终点。更多接受resmetirom治疗的患者获得NASH症状缓解,非酒精性脂肪肝活动评分(NAS)降低≥2分,且肝纤维化无恶化;以及肝纤维化至少改善一个阶段,且NAS无恶化。具体数据请见下图:
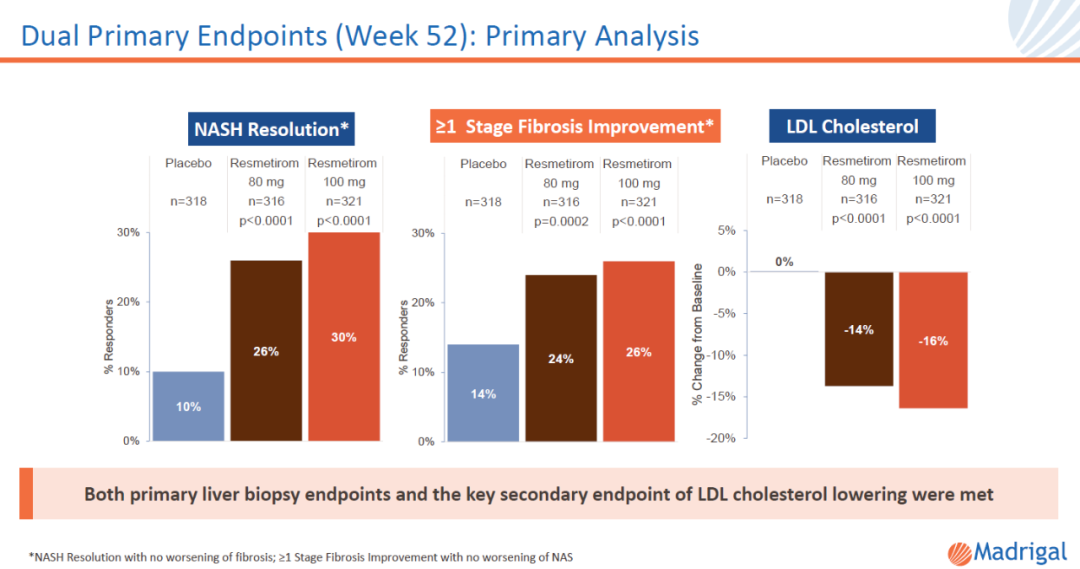
▲Resmetirom在关键性3期临床试验中的主要终点数据(图片来源:Madrigal公司官网)
此外,resmetirom还达到试验的多项次要终点,其中包括与基线相比,显著降低包括低密度脂蛋白胆固醇(LDL-C)在内的多种脂质和脂蛋白指标。
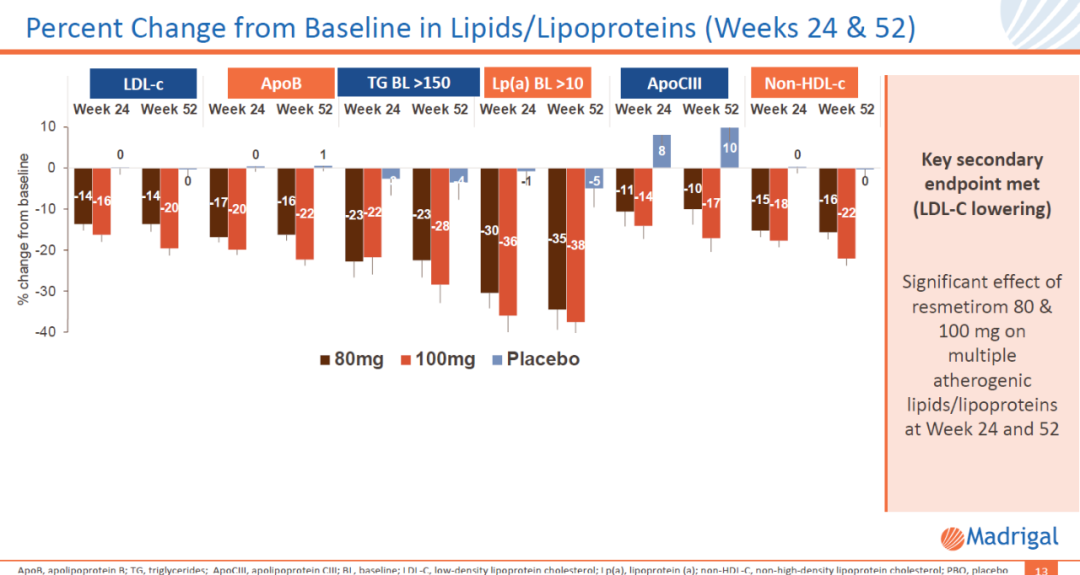
▲Resmetirom降低多种脂质和脂蛋白指标(图片来源:Madrigal公司官网)
利用基于核磁共振的无创检测手段对肝脏脂肪水平的评估显示,接受剂量为100 mg的resmetirom治疗52周后,患者肝脏脂肪水平平均降低51%。肝纤维化、肝脏体积和脾脏体积也显著降低。
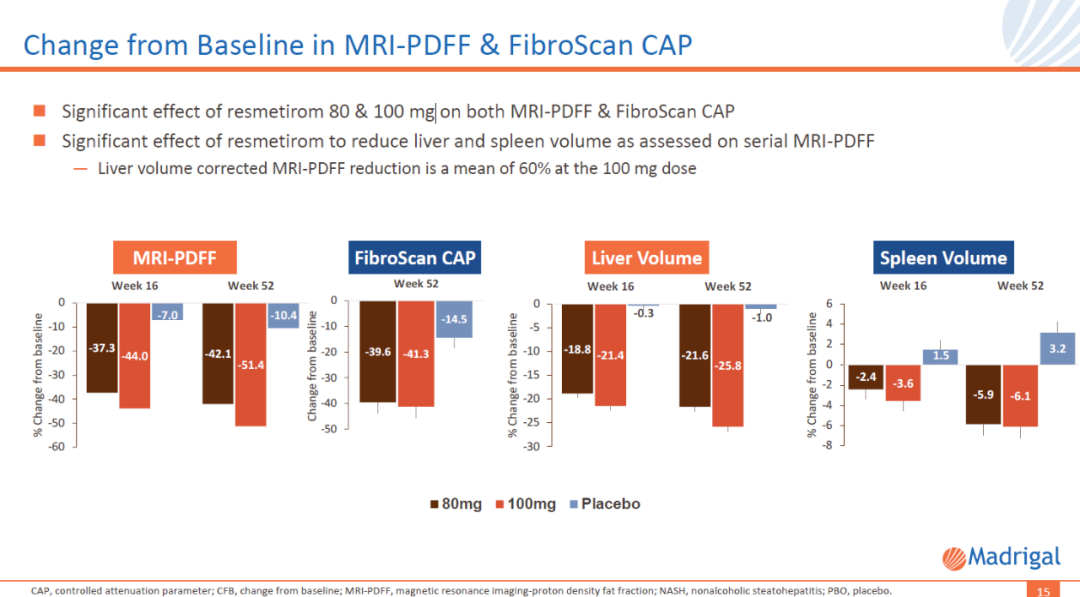
图片来源:Madrigal公司官网
Madrigal在今年7月完成向美国FDA滚动提交resmetirom的新药申请,用于治疗伴肝纤维化的NASH成人患者,该疾病尚无获批疗法。2023年4月,resmetirom被美国FDA授予治疗伴肝纤维化的NASH成人患者的突破性疗法认定。

 新浪医药
新浪医药
 2018.07.12
2018.07.12
 34556
34556

 医谷
医谷
 2019.03.18
2019.03.18
 18903
18903

 医药地理
医药地理
 2018.10.22
2018.10.22
 18897
18897