 会员动态
会员动态
 医药观澜
医药观澜
 2024.04.26
2024.04.26
 338
338
4月25日,中国国家药监局药品审评中心(CDE)官网公示,信达生物IBI343拟纳入突破性治疗品种,针对适应症为至少接受过二种系统性治疗的Claudin(CLDN)18.2表达阳性的晚期胃/胃食管交界处腺癌。根据信达生物公开资料,IBI343是一款靶向Claudin18.2的抗体偶联药物(ADC)。目前该产品正在针对Claudin18.2阳性、HER2阴性胃癌开展3期临床研究。
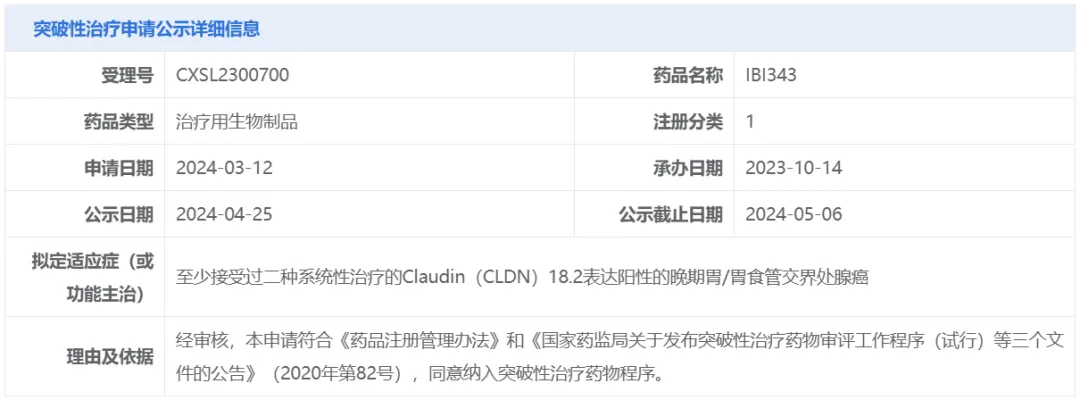
截图来源:CDE官网
Claudin是正常组织紧密连接中重要的一种蛋白质,具有4个跨膜结构域,它参与细胞旁通透性和电导等过程的调节。Claudin18.2在包含胃癌在内的消化道癌症中高度表达。因此,Claudin18.2为治疗胃癌、胰腺癌等实体肿瘤的有效靶标。
IBI343是信达生物管线中第一个进入临床阶段的ADC候选产品,针对靶点为Claudin18.2,并实现了对细胞毒素exatecan的糖基定点偶联。它与表达Claudin18.2的肿瘤细胞结合后,可发生Claudin18.2依赖性ADC内化,释放毒素药物引起DNA损伤,导致肿瘤细胞凋亡。游离的毒素药物也可以通过质膜扩散到达并杀死相邻的肿瘤细胞,具有旁观者效应。
根据信达生物在2024年美国癌症研究协会(AACR)年会公布的临床前数据,IBI343在多种不同表达量的肿瘤细胞系上展现了良好的Claudin18.2特异性体外杀伤活性,并在多种人源肿瘤异种移植小鼠模型上展现了良好的肿瘤抑制活性。此外,基于糖基的定点偶联技术显著增强了整个ADC的稳定性。该产品在恒河猴的GLP毒理实验中展现了较好的安全性,并在高至30mg/kg的剂量下耐受性良好。
在即将召开的2024年美国临床肿瘤学会(ASCO)年会上,信达生物还即将以壁报形式展示IBI343在晚期胰腺导管腺癌或胆道癌患者的安全性和疗效。
根据中国药物临床试验登记与信息公示平台官网,信达生物已经启动了IBI343的国际多中心3期临床研究(G-HOPE-001),该研究将评价IBI343单药对比研究者选择的治疗用于既往接受过治疗的Claudin18.2阳性、HER2阴性、局部晚期不可切除或转移性胃或胃食管交界处腺癌受试者的有效性和安全性。该研究由沈琳教授担任主要研究者,将在中国、日本的70家临床研究机构入组受试者。
值得一提的是,除了IBI343,信达生物还开发了多款其它的ADC在研药物,其中有多款已进入到临床试验阶段(见下表)。其中,IBI334和IBI3001各有一项研究入选了本届2024年美国癌症研究协会(AACR)年会的Late-Breaking Research环节。
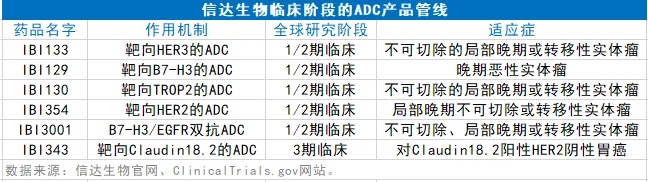
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网. Retrieved Apr 25, 2024, from https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d
[2] 信达生物在美国癌症研究协会(AACR)2024年会公布多项创新管线的临床前数据. Retrieved April 8, 2024 from https://mp.weixin.qq.com/s/IPgxIkvbvqb76xdYYfeFzg
[3] 信达生物官网. From http://cn.innoventbio.com/?ivk_sa=1021577i#/pline
[4]信达生物IBI343(CLDN 18.2抗体药物偶联物)在澳大利亚完成首例受试者给药. Retrieved Oct 31, 2022, from https://mp.weixin.qq.com/s/K2-nIbZwCZompUtMCdtr_g

 豪森药业
豪森药业
 2019.05.08
2019.05.08
 27682
27682

 蒲公英
蒲公英
 2018.07.10
2018.07.10
 15559
15559

 生物制药小编
生物制药小编
 2018.06.27
2018.06.27
 15005
15005