 产业资讯
产业资讯
 医麦客
医麦客
 2024.04.29
2024.04.29
 159
159
HER3在多种实体肿瘤中均有表达,包括乳腺癌、肺癌等,HER3的过表达与非小细胞肺癌(NSCLC)癌细胞的转移、预后不良以及患者存活率的降低密切相关。HER3信号通路已被科学研究证实与抗EGFR/HER2疗法的耐药机制紧密相联。这一发现为抗击非小细胞肺癌提供了新的治疗思路,使得HER3成为治疗非小细胞肺癌等实体瘤极具潜力的靶点,已经吸引着众多制药企业涌入赛道争夺市场。
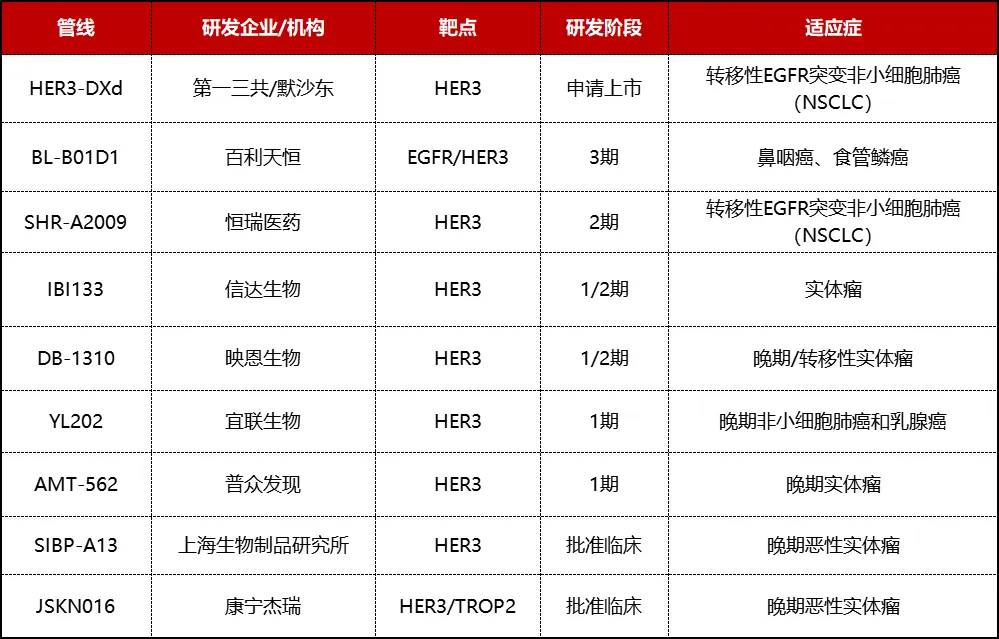
▲ HER3 ADC获批临床的代表管线 来源:星耀研究院整理
在全球HER3 ADC的竞争格局中,第一三共的HER3-DXd已经提交上市申请,有望率先撞线,打破HER3因缺乏显著激酶活性而难以成药的困境。Endeavor BioMedicines于近日完成了1.325亿美元的C轮融资,部分资金将用于推动靶向HER3的ADC候选药物ENV-501的临床概念验证研究。
国内创新企业的表现也尤为活跃,百利天恒、恒瑞医药、信达生物、映恩生物、宜联生物等企业进展频频。优异的技术平台成为出海的风帆,宜联生物的YL202出海BioNtech、百利天恒HER3/EGFR ADC出海BMS,合作潜在总金额超过90亿美元。国内外企业正在探索新兴靶点HER3的广阔蓝海。
第一三共/默沙东HER3-DXd:
有望成为全球首个针对HER3靶点疗法
去年年底,第一三共/默沙东宣布美国FDA受理了他们开发的HER3 ADC候选产品HER3-DXd(U3-1402)的生物制品许可申请,并授予其优先审评资格,用于治疗既往接受过两种或两种以上全身治疗的局部晚期或转移性EGFR突变非小细胞肺癌(NSCLC)成人患者。FDA的审评决议日期(PDUFA日期)定于2024年6月26日。HER3-DXd有望成为全球首个上市的、针对HER3靶点的创新疗法。
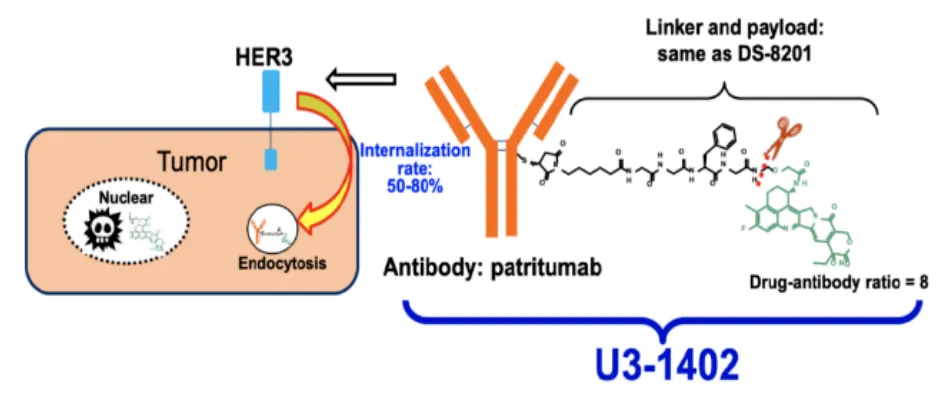
▲HER3-DXd(U3-1402)作用机制 来源:第一三共官网
该款HER3 ADC由第一三共开发,采用其独有的DXd ADC技术设计,由全人源化抗HER3 IgG1单克隆抗体通过可裂解四肽连接子与拓扑异构酶I抑制剂有效载荷(一种依喜替康衍生物,DXd)连接组成。2023年10月,第一三共与默沙东于达成220亿美元的全球合作,共同开发并商业化包括HER3-DXd在内的三款ADC新药。
Endeavor完成1.325亿美元C轮融资,
将HER3 ADC推入临床
近日,Endeavor BioMedicines宣布成功完成了1.325亿美元的C轮融资,获得资金将用于推动其治疗特发性肺纤维化(IPF)和进行性肺纤维化(PPF)的在研小分子疗法ENV-101的临床开发。此外,这笔资金还将支持针对HER3阳性实体瘤的ENV-501临床概念验证研究。ENV-501是新一代靶向HER3的ADC,结合了先进的化学和遗传学特性,旨在优化药物递送至肿瘤,从而提高其效力并减少非靶向毒性。Endeavor计划在2024年启动ENV-501的1/2期临床试验。
百利天恒BL-B01D1:
全球首创的EGFR/HER3双抗ADC
百利天恒全资子公司SystImmune开发的BL-B01D1是全球首创的EGFR/HER3 双抗ADC,其单药治疗末线鼻咽癌、二线食管鳞癌的临床研究已进入III期研究阶段,临床开发进度仅次于第一三共和默沙东的HER3-DXd。BL-B01D1采用酶切可裂解的linker,payload是TOP I,为百利天恒自主研发的喜树碱衍生物ED04,DAR值为8。从作用机制来讲,由于其特殊的结构特征,SI-B001并不会直接与HER3相结合,从而避免了分子对于维持正常生理功能靶点的抑制作用,药物的毒副作用低,有望带来更宽的治疗窗口。
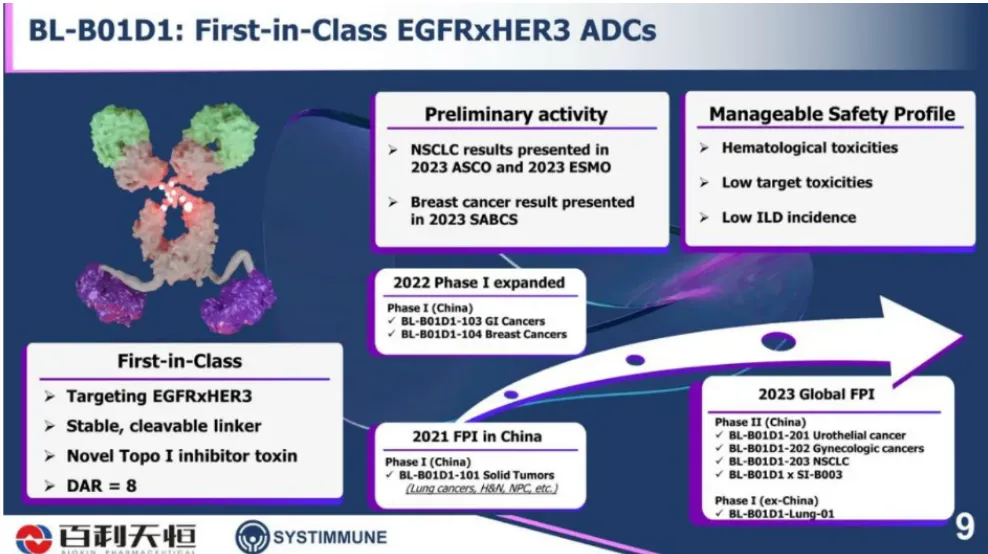
▲BL-B01D1结构 来源:百利天恒官网
2023年ASCO大会上,百利天恒更新了BL-B01D1在鼻咽癌中的进展,经过至少1次疗效评估的鼻咽癌受试者共28例,客观缓解率(ORR)为53.6%,疾病控制率(DCR)为100%。2023年12月,百利天恒超80亿美元携手BMS开发和商业化BL-B01D1。今年3月11日,百利天恒已收到8亿美元首付款。
恒瑞医药:SHR-A2009
SHR-A2009是恒瑞医药自主研发的一款以HER3为靶点的ADC,可特异性结合肿瘤细胞表面上的HER3,进而被内吞至细胞内并转运至溶酶体中,水解释放游离毒素。今年年初,SHR-A2009获得美国FDA授予快速通道资格,用于治疗经第三代EGFR-TKI和含铂化疗后疾病进展的EGFR突变的转移性NSCLC,成为恒瑞医药历史上第一个获得美国FDA快速通道资格认定的创新药。此前,SHR-A2009单药用于治疗晚期/转移性实体瘤治疗的临床试验申请已获得中美双批。
信达生物: IBI133
今年4月15日,信达生物开发的HER3 ADC候选产品IBI133临床试验申请获得默示许可。据悉,IBI133已于去年12月在澳大利亚启动了一项1/2期临床试验(NCT06170190),针对实体瘤患者。
映恩生物:DB-1310
DB-1310是映恩生物基于其DITAC技术平台开发的靶向HER3的ADC产品,由新型人源化抗Her3单克隆抗体通过马来酰亚胺可裂解linker与专有的DNA拓扑异构酶I抑制剂共价连接,DAR值约为8。2023年5月,DB-1310的临床试验申请获CDE受理,拟用于治疗晚期/转移性实体瘤,目前处于临床1/2期。在临床前研究中表现出优异的肿瘤抑制效果和安全性,并且在与EGFR小分子抑制剂联合使用中表现出优秀的协同抑制肿瘤效果。
宜联生物:YL202
宜联生物开发的靶向HER3的新型ADC候选药物YL202也深受全球制药巨头青睐。2023年10月,宜联生物宣布与BioNTech达成合作协议,将YL202的大中华区外全球权益授权BioNTech。本次交易将支付7000万美元首付款,以及额外开发、监管和商业化里程碑付款,潜在总金额超过10亿美元。
宜联生物打造的ADC平台技术TMALIN在实现高DAR值均一性稳定偶联的同时,进一步提高ADC药物的治疗窗,增强ADC药物在实体肿瘤中的治疗效果。非临床研究表明,YL202介导了有效的肿瘤杀伤作用。体内药效学(PD)研究表明,YL202在人肿瘤细胞异种移植和表达HER3的人肿瘤异种移植瘤模型中均具有剂量依赖性的抗肿瘤活性。目前,YL202已在晚期非小细胞肺癌和乳腺癌患者中完成临床1期试验,未来将在前列腺癌和食管鳞癌适应症上探索研究。
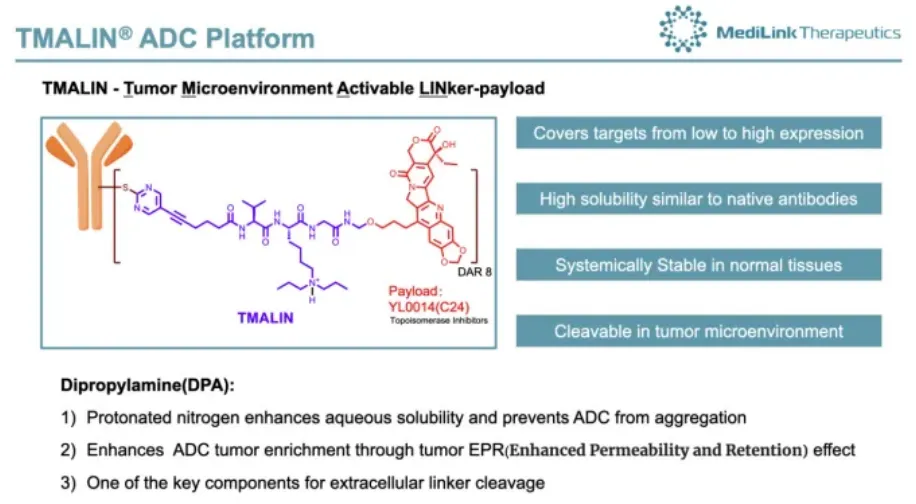
▲TMALIN技术平台 来源:宜联生物官网
普众发现:AMT-562
今年2月27日,普众发现(MultitudeTherapeutics)靶向HER3的ADC候选产品AMT-562获批临床,拟用于治疗晚期实体瘤。AMT-562由一种新型抗HER3抗体Ab562和一种增强了亲水性的连接子MC-VA-PABC结合有效载荷exatecan(依喜替康)构成。抗体部分Ab562具有降低潜在毒性、改善肿瘤渗透性的潜力;有效载荷exatecan具有比其衍生物deruxtecan(DXd)更高的细胞毒性效力。目前正在澳大利亚开展一项针对晚期实体瘤的1期临床研究。研究表明AMT-562有可能成为一种具有更宽治疗窗口的HER3靶向ADC,可以克服耐药性。
上海生物制品研究所:SIBP-A13
2023年9月18日,国药集团中国生物上海生物制品研究所自主研发的靶向HER3 ADC新药SIBP-A13获得NMPA临床试验批准通知书,拟用于在晚期恶性实体瘤患者中开展临床试验。
SIBP-A13基于国内领先的第3代ADC技术研发,具有连接子可裂解、载荷活性强、抗肿瘤“旁观者效应”等药物优势。SIBP-A13药效研究数据显示其可有效抑制多种肿瘤生长,对肺癌、乳腺癌等多种实体瘤具有治疗潜力。临床前药代动力学及毒理研究显示,SIBP-A13在动物体内稳定性良好,游离小分子水平显著低于同类产品,具有较好的安全性及耐受性。
康宁杰瑞:JSKN016
2024年3月19日,康宁杰瑞的JSKN016注射液获NMPA临床批准,用于治疗晚期恶性实体瘤。JSKN016可同时靶向HER3和TROP2,与肿瘤细胞表面TROP2或者HER3结合后,通过靶点介导的内吞作用进入到溶酶体中,释放出具有细胞毒性的拓扑异构酶I抑制剂 (TOPIi),进而诱导肿瘤细胞死亡,此外该抑制剂还可以穿透细胞膜进入到抗原阴性的肿瘤细胞中发挥旁观者效应。两者的叠加作用可以有效抑制肿瘤细胞的生长。
结语
随着临床开发的不断深入,ADC药物在多种癌症中都显示出良好的抗癌效果,有望改变各种癌症的治疗策略。而HER3的表达因主要见于肺癌、乳腺癌、结直肠癌、胃癌等多个常见肿瘤,具有成为泛癌ADC的潜力,正受到制药企业的研发热捧,第一三共等开拓者能否继续开疆辟土,恒瑞医药等跟随者能否后来居上,等待积极的数据给出答案。

 CPhI制药在线
CPhI制药在线
 2018.07.24
2018.07.24
 49870
49870

 艾美仕
艾美仕
 2018.07.09
2018.07.09
 34839
34839


 2014.03.11
2014.03.11
 31197
31197