 产业资讯
产业资讯
 医药观澜
医药观澜
 2024.05.07
2024.05.07
 136
136
中国药物临床试验登记与信息公示平台近日公示,阿斯利康(AstraZeneca)已经启动一项ALXN2220注射液的国际多中心(含中国)3期临床研究,针对受试者群体为经确诊的野生型或遗传型转甲状腺素蛋白介导的淀粉样变性成年心肌病(ATTR-CM)患者。公开资料显示,ALXN2220(又称NI006)是一款抗淀粉样转甲状腺素蛋白(ATTR)单克隆抗体,为一款心脏淀粉样蛋白“耗竭剂”。

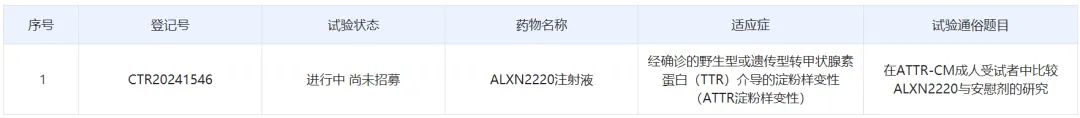
截图来源:中国药物临床试验登记与信息公示平台官网
ATTR-CM是一种全身性的进行性致命疾病,可导致患者发生进行性心力衰竭和死亡。ATTR-CM患者由于衰老或基因突变,导致ATTR错误折叠,并作为淀粉样纤维在心肌中沉积,从而损害相应器官组织的正常功能,并最终导致死亡。尽管该病已有疗法获批,但这些疗法均只能防止淀粉样蛋白积累,对于心脏中已经有大量淀粉样蛋白沉积的中度至重度ATTR-CM患者,他们依然面临着极大的未竟需求。
ALXN2220是一款在研人源化单克隆抗体,专为吞噬免疫细胞清除ATTR而开发。该产品可特异性靶向错误折叠的转甲状腺素蛋白,通过清除心脏中的淀粉样纤维沉积物,针对ATTR-CM的病理原因,有望治疗晚期ATTR-CM患者。临床前模型证明,该产品可诱导病理性ATTR的清除。
2022年3月,阿斯利康旗下专注于罕见病领域的Alexion公司宣布完成与Neurimmune公司就ALXN2220达成的独家全球合作和许可协议。根据协议条款,在1期临床试验结束后,Alexion公司将负责该候选疗法进一步的临床开发和商业化。Neurimmune公司将获得3000万美元的预付款,还有资格获得高达7.3亿美元的开发、监管和商业里程碑付款。
本次阿斯利康在中国启动的是一项在ATTR-CM成人受试者中评价淀粉样蛋白耗竭剂ALXN2220的有效性和安全性的3期、随机、双盲、安慰剂对照、多中心研究。在该研究中,ALXN2220注射液的用法为每月一次给药,用药时程为24月。主要终点指标为24月时全因死亡(ACM)和总心血管(CV)临床事件的复合终点差异。
ALXN2220治疗ATTR-CM的1期临床研究已于去年6月发表在《新英格兰医学杂志》。在这项1期、双盲试验中,研究人员将40例野生型或变异型ATTR心肌病和慢性心力衰竭患者随机分配接受ALXN2220或安慰剂静脉输注,每4周一次,持续4个月。患者序贯入组接受递增剂量的6个队列。4次输注后,患者入组开放标签扩展期,在该扩展期接受8次ALXN2220输注,逐步增加剂量。
研究结果显示,ALXN2220的安全性在最高测试剂量下依然良好,未观察到明显的剂量限制毒性或与药物相关的严重不良反应。该产品的药代动力学特征与IgG抗体一致,未检测到抗药抗体。在至少10mg/kg的剂量下,患者心脏淀粉样蛋白沉积(通过闪烁扫描仪或心脏磁共振成像检测)在12个月内显著减少。用于测量心脏压力的和心肌细胞死亡的生物标志物NT-proBNP和肌钙蛋白T的水平也有所降低。
参考资料:
[1]中国药物临床试验登记与信息公示平台官网. Retrieved Apr 30 , 2024. From http://www.chinadrugtrials.org.cn/clinicaltrials.searchlistdetail.dhtml
[2]Pablo Garcia-Pavia. et al. (2023)Phase 1 Trial of Antibody NI006 for Depletion of Cardiac Transthyretin Amyloid.N Engl J Med. DOI: 10.1056/NEJMoa2303765

 CPhI制药在线
CPhI制药在线
 2018.07.24
2018.07.24
 49870
49870

 艾美仕
艾美仕
 2018.07.09
2018.07.09
 34839
34839


 2014.03.11
2014.03.11
 31197
31197