 产业资讯
产业资讯
 瞪羚社
瞪羚社  2026-03-25
2026-03-25
 6
6
暴跌之际,美诺华今天创下了在2025年8月以来的历史新高。
尽管公司股价今天在短暂创下新高后,并没有扛住今天大盘的抛压反馈,但其股价在3月以来逆势上涨超过20%,可以说表现跑赢了医药行业98%以上的公司。
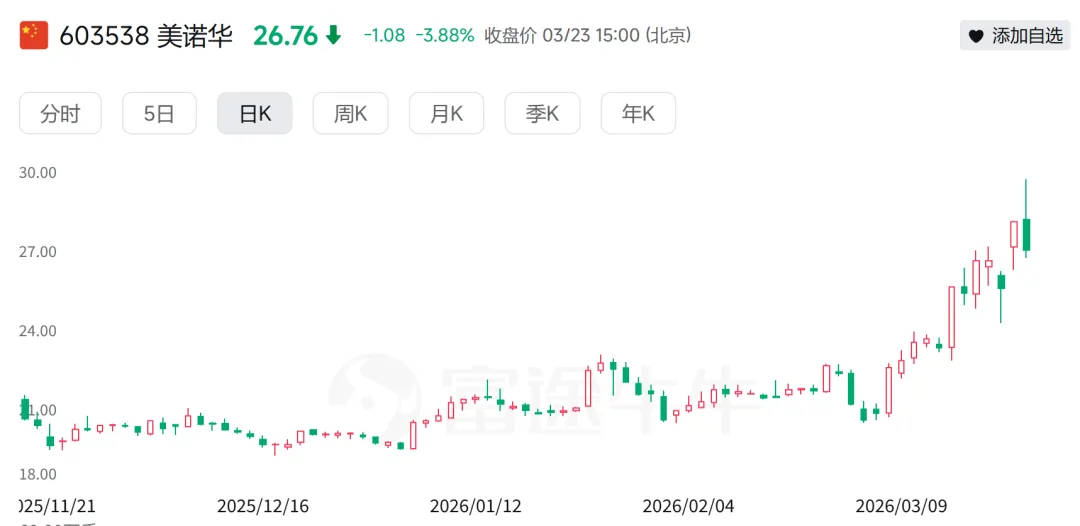
美诺华作为一家“原料药+CDMO+制剂一体化”的公司,你说原料药行业有β带动吗?3月以来原料药行业分类(884143)跌幅超过12%,负β倒是不少,而市场关心的公司比较核心的客户链条无非是KRKA和默沙东的合作,并无更重大的订单情况透露(当然也可能是默沙东合作的第三款产品商业化放量),不过公司逆势飙升的原因大概率来自——减肥药JH389的海外进展和人体数据的披露。
为什么说是“野路子”减肥药,说是药物可能不准确,说JH389是益生菌或保健品更为准确,这是一款基于工程化益生菌递送平台的产品(益生菌在肠道定点递送GLP-1类似物),以及它的首选商业化路径并不是以药物进行申报,而是以膳食补充剂进行申报。
去年公司管理层介绍这款药物的时候,单一适应症市场潜力给出至少9个亿美元的市场峰值(75万潜在用户,费用100美元/月,对应GLP-1用药结束后的缓冲期人群),另外有减肥需求并且不愿意打针吃药人群的潜在市场空间,大到无法具象化。
简而言之,计算器都快摁冒烟了,反正你别问,问就是牛逼。
01
吊打现有GLP-1口服药物?
恰逢在3月19日,美诺华JH389公布了28例受试者的为期8周,采用单中心、开放、自身对照设计的临床结果,数据显示:
● 受试者平均减重2.5kg,减重比例3.2%,并且在BMI<28的受试者减重效果更优,平均减重4.26%;
● 受试者平均减脂2.2kg,改善成都为7.07%;皮下脂肪厚度平均减少3.9mm,改善程度为12.86%;
● 所有受试者临床全程无产品相关的不良反应;
需要明确的是,美诺华JH389与目前其他在研的口服GLP-1药物并不可比,不可比的点在哪里呢?
一是目前的试验数据是自身对照设计(缺乏安慰剂组),数据置信度较差;
二是JH389的8周3.2%减重幅度对比其他在研的口服GLP-1药物疗效较弱,罗氏CT-996的4周减重幅度7.3%、诚益生物ECC5004的4周减重幅度5.8%远超JH389;
最后JH389更强的减重疗效发生在BMI<28的受试者,这类患者属于轻度肥胖人群,而目前主流在研GLP-1药物普遍入组排除了BMI<27(无合并症)的受试者。
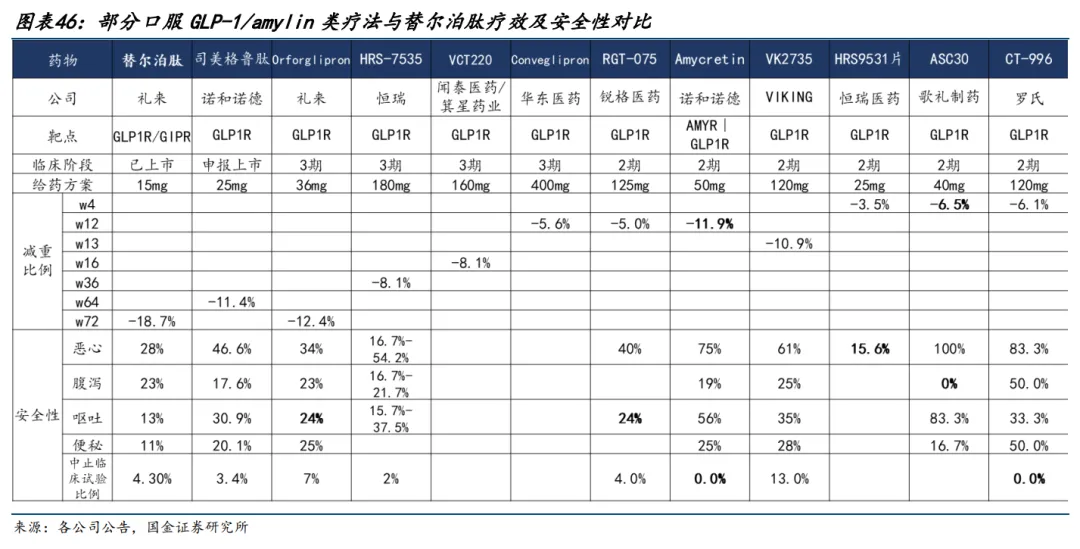
JH389真正的亮点在于安全性优势突出,试验全程无产品相关不良反应,对比大量在研小分子药物较高的胃肠道不良反应发生率(恶心、腹泻等)以及部分分子较高的停药率,JH389对患者的依从性良好,未来消费级市场或许非常友好。
只能说产品有亮点以及差异化生存空间,但效果确实要打个问号。
02
规避药品申报路径,快速商业化
在海外,美诺华就JH389与意大利老牌头部益生菌合作方(市场猜测是Coswell SpA)已达成协议:目前正开展欧洲上市所需的安全性实验研究,有机会在2026年商业化。
从申报复杂度和难度而言,在欧盟的膳食补剂(又叫新型食品)上市并不需要进行人体临床,可以通过体外的毒理学代替,但有一点疑惑,美诺华JH389由于含活菌类(虽然是欧盟广泛食用的传统益生菌-枯草芽孢杆菌进行微小修饰,合作方采用通知制备案即售申报路径,判定可以受到豁免),如果一般判定会属于高风险的新型食品范畴,这可能会触发EFSA需要补充人体临床数据,以及申报时长更久。
相比于药物的临床I期,EFSA新型食品人体安全研究样本量更小且接受单臂试验设计,无论是试验成本和随访时间都比药物临床I期都少得多。
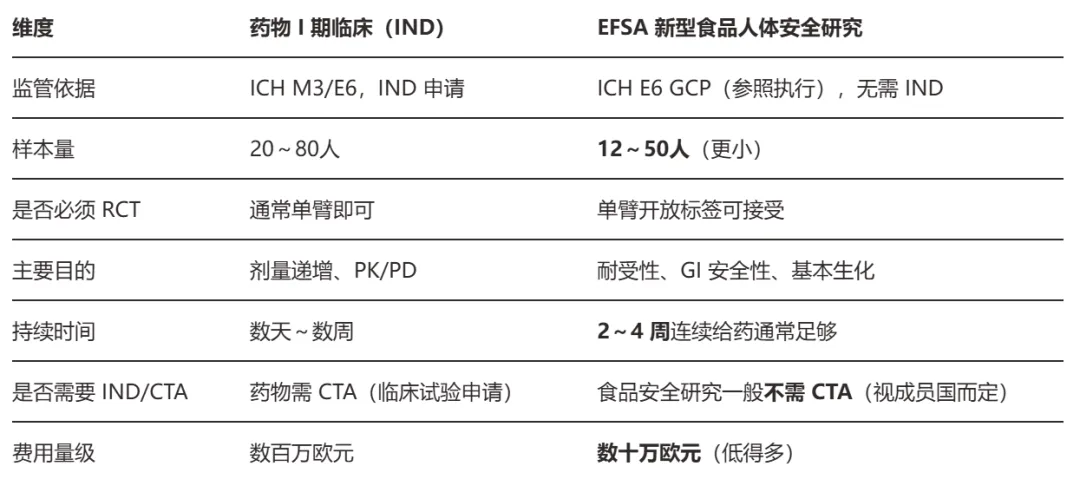
而目前美诺华公布的28人临床数据初步满足人体安全性的初步要求,但缺乏规范要求的安全性终点(包括:定植持久性、易位风险、微生物组影响等),需要等待意大利合作方完成安全性试验进行上市备案申报。

从目前公开得到信息来看,美诺华的意大利合作方对JH389的申报路径判断是"通知制备案即售",这条路径如果按照目前情况(假设4月如期备案),那么正如上述提到最快2026年内在欧洲商业化放量。
但如果上述路径豁免判定无效,仍作为新型食品认定路径,可能需要额外1-2年的审批时间。
03
乱入和疑点
虽然是膳食补剂,没法对这个产品像药物一样有太多的苛刻要求,但从技术路线上还是有很多迷惑和疑点的地方,同时单臂开放研究可参考性也非常弱。
由于服用的是“活的工程菌”,菌体在肠道分泌GLP-1类似物,可控性存在一个巨大的问题:菌体的存活、繁殖、分泌效率存在极大的个体差异。另外一点,JH389的优势在于它在胃酸环境下保持极强的存活率(约70%),它安全优势在于菌体的长期缓释(不像口服GLP-1采取激进的滴定策略),而目前人体数据随访数据在8周,长期服用安全性可能需要进一步的数据。
更重要的是工程菌直接递送GLP-1这个技术方向,学术界研究了十多年,有不少的文献和研究出来,但产业转化接近于0,问题出在哪?
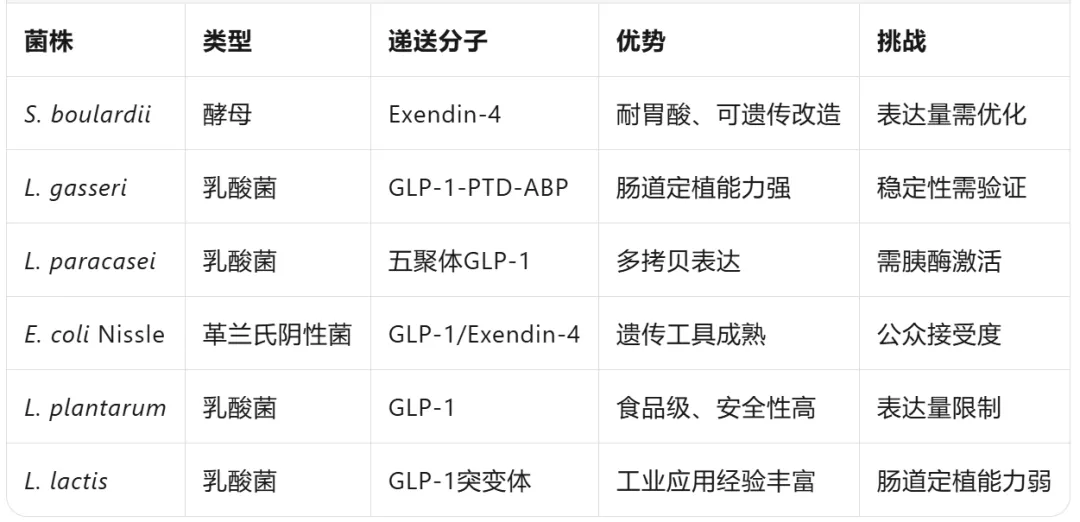
(过往技术研究汇总)
值得注意的是,2024年3月美国公司Pendulum推出了"GLP-1 Probiotic"(65美元/月),其与美诺华JH389区别在于Pendulum是通过调节肠道菌群间接促进内源性GLP-1分泌,并非让工程菌体生产,但它同样是膳食补充剂的路径商业化,这个产品似乎在美国市场也是不温不火。
美诺华JH389这个产品也算是膳食补剂减肥产品的FIC了,但当前来看,这产品不及预期的可能性也不小,风险也不低。
结语:减重市场的魅力就是如此,即便是减重停药维持期的假设10%渗透率市场都能诞生10亿美元的重磅品种,让美诺华JH389拥趸们按计算器“10亿美元对应2亿美元净利润”约等于再造几个美诺华而疯狂,但似乎这个时候开香槟,确实有点早。

 产业资讯
产业资讯
 动脉网
动脉网  2026-03-25
2026-03-25
 2
2
 产业资讯
产业资讯
 MedTrend医趋势
MedTrend医趋势  2026-03-25
2026-03-25
 2
2

 产业资讯
产业资讯
 同写意
同写意  2026-03-25
2026-03-25
 2
2