 研发追踪
研发追踪
 药时代
药时代  2026-02-06
2026-02-06
 1373
1373
百亿美元押注,能否物超所值?
当地时间2026年2月3日,辉瑞宣布其长效GLP-1受体激动剂PF'3944(原MET-097i)关键IIb期VESPER-3试验取得积极顶线结果。

截图来源:辉瑞官网PF'3944是辉瑞百亿美元收购Metsera的核心资产,相较于目前已上市的GLP-1产品,该分子具有“偏向性激动”的差异化优势。推荐阅读:辉瑞胜出!100亿美元收购Metsera以司美格鲁肽为例,当该药物被激活时,会通过多个细胞内通路启动信号(包括G蛋白通路与β-arrestin通路)。而PF'3944则被设计为优先激活治疗性的G蛋白通路,同时最小化β-arrestin的招募,理论上该机制可减少受体脱敏、延长治疗时间,同时提高耐受性,减少胃肠道的毒副作用。因此,辉瑞/Metsera在VESPER-3试验中该研究设定了两个目标:
(1)证明PF'3944在从每周一次转为每月一次皮下注射后能持续减重,并保持疗效;
(2)证明PF'3944可转为等效月剂量的同时,维持良好耐受性和安全性。
结果显示,用药28周后,安慰剂调整后的平均减重幅度最高达12.3%(采用疗效估计值),具有统计学显著性。只是这样的结果,或许无法让投资者满意。消息公布当天,辉瑞股价小幅跌去3.34%(不排除辉瑞同日公布2025年全年报影响)。
截图来源:雪球
VESPER-3研究是一项为期64周的随机、双盲、安慰剂对照试验,受试者为肥胖或超重但不伴有2型糖尿病的成人(n=250)。该研究旨在评估QW PF'3944在第28周转用QM与安慰剂的四个剂量方案疗效。
受试者被随机分配至四种剂量递增方案:第1组(0.4mg QW/0.8mg QW/3.2mg QM);第2组(0.8mg QW/3.2mg QM);第3组(0.4mg QW/0.8mg QW//1.2mg QW/4.8mg QM);第4组(0.6mg QW/1.2mg QW/4.8mg QM);或第5组(安慰剂,生理盐水)。前12周为PF'3944周剂量治疗,随后转为月剂量治疗至第28周。
结果显示,第28周时所有剂量的治疗组减重效果均显著优于安慰剂(P < 0.001)。其中,计划用于III期研究的低剂量组(第一组:3.2mg/月)和中剂量组(第二组:4.8mg/月)在28周时分别实现了10%和12.3%的体重减轻。
辉瑞在新闻稿中表示,受试者转为PF'3944月剂量治疗后减重效果显著且持续,第28周时未观察到平台期,这表明随着研究持续进行至第64周,预计减重将继续。
安全性方面,至第28周,观察到的胃肠道不良事件主要为轻度或中度,任何剂量组中仅有一次严重恶心或呕吐,无严重腹泻病例。在第1组和第3组中,周剂量治疗期共有5名受试者因不良事件中止治疗,月剂量治疗期也有5名受试者因不良事件中止治疗。安慰剂组无受试者因不良事件中止治疗。
具体详细结果将于今年年中在美国糖尿病协会上公布。
为何数据积极,投资者却不愿买账?
一是,不如中期试验数据。在VESPER-1研究(n=239)中,PF'3944 1.2mgQW组经安慰剂组调整后的平均体重降幅为-14.1%。此外,1.2mg剂量组个体最高体重降幅达到-26.5%。
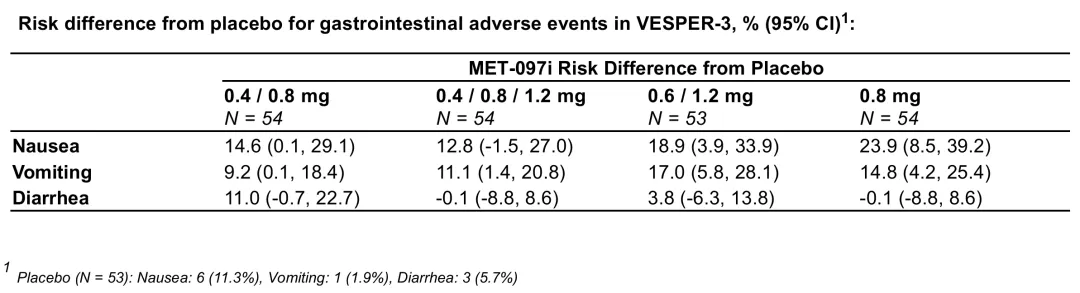
截图来源:Metsera官网
二是,货比货。12.3%的数据读出,是采用更宽松的疗效估计分析(类似按方案分析);而在治疗策略估计分析中(类似意向治疗分析,纳入所有可用体重数据而不考虑治疗依从性),第3组安慰剂调整后的减重幅度为10.5%。而第1组该数据为8.4%。
与礼来的Zepbound进行横向数据对此,使用疗效估计分析,Zepbound在治疗28周时安慰剂调整减重幅度约为13%。
安全性方面,PF'3944试验组共有10名患者因不良反应退出(周治疗期5人,月治疗期5人)。副作用停药率约为10%,而Zepbound在关键试验中的该数据为6.2%。
三是,在数据尚不明朗的情况下,辉瑞重仓PF'3944。按规划,辉瑞年内将启动多项关键试验:包括评估周疗方案的VESPER-4(肥胖患者)、VESPER-5(肥胖合并2型糖尿病患者),以及继续验证月疗方案的VESPER-6,以及已规划的至少7项其他III期研究。
小结:
要真正评估PF'3944的商业潜力,需要VESPER-3研究的完整数据。辉瑞目前仅公布了四组剂量方案中两组(第1、3组)的减重数据,采用稍不同给药方案的第2、4组数据尚未披露。
安慰剂组的减重数据也未公布。缺乏这些信息,将难以评估PF'3944后续三期试验的预期。
不过,辉瑞首席科学官Chris Boshoff 在财报会议上透露,即将开展的III期临床将测试更高剂量(9.6mg/月),模型预测可能达到近16%的减重效果。

 研发追踪
研发追踪
 医药时间
医药时间  2026-05-04
2026-05-04
 457
457

 研发追踪
研发追踪
 药讯随说
药讯随说  2026-05-04
2026-05-04
 460
460

 研发追踪
研发追踪
 医药笔记
医药笔记  2026-05-04
2026-05-04
 442
442
 热门资讯
热门资讯