 产业资讯
产业资讯
 药事纵横
药事纵横  2026-02-11
2026-02-11
 1674
1674
1月30日,康哲药业宣布磷酸芦可替尼乳膏获国家药监局批准上市,用于治疗12岁及以上儿童和成人患者伴面部受累的非节段型白癜风。
治疗组主要疗效指标第24周达到F-VASI 75的患者比例为49.5%,显著高于目标值14.1%(P<0.0001),研究达到了主要终点。所有的次要疗效指标均显示出与主要疗效指标一致的获益趋势,且治疗时间越长,患者的白癜风治疗效果持续改善。不良反应的严重程度大部分均为1级或2级,未发生导致停药或退出的不良事件(AE),未发生研究药物相关的严重不良事件(SAE)。
我国白癜风患者人群庞大,约1400万人,磷酸芦可替尼乳膏作为国内首款且唯一用于白癜风治疗的靶向药,有望为广大白癜风患者带来治疗曙光。
(一)白癜风:患者群体庞大,且治疗选择极其有限
白癜风是一种慢性自身免疫性疾病,其特征是皮肤色素脱失,常见于指背、腕、前臂、颜面、颈部等,其发病原因为产生色素的细胞即黑素细胞的缺失。根据《白癜风诊疗共识(2021版)》,中国白癜风患者约1400万,且好发于青少年人群。鉴于患者人群庞大且好发于年轻人群,白癜风的治疗需求巨大且急迫。
白癜风治疗药物十分有限,目前主流的白癜风治疗药物包括钙调磷酸酶抑制剂(TCI)、糖皮质激素(TCS)、维生素D3衍生物(卡泊三醇软膏),但糖皮质激素不良反应发生率较高,钙调磷酸酶抑制剂及维生素D3衍生物缺少长期使用风险的证据,大部分指南及共识持谨慎态度。
目前,国际指南及中国共识认为,JAK抑制剂有望成为白癜风治疗的新手段。2022年7月,芦可替尼乳膏获美国FDA批准上市,用于12岁及以上非节段型白癜风患者的局部治疗。芦可替尼乳膏上市后,销售额快速攀升,2024年收入达5.1亿美元,较2023年增长50.9%,反映出白癜风患较大未满足的临床需求。
图:芦可替尼乳膏销售额(亿美元)
数据来源:Incyte年报

(二)白癜风国内布局
目前,全球布局白癜风新药研发的企业较少。Incyte是白癜风领域的佼佼者,手握唯一一款上市的白癜风新药——芦可替尼乳膏,此外;Incyte旗下另一款白癜风潜力药物——Povorcitinib已推进至临床Ⅲ期,康哲药业在国内则是引入Incyte两款白癜风药物。除了康哲药业外,泰恩康、诺诚健华等亦在白癜风赛道你追我赶。天量白癜风市场,预计即将迎来变局。
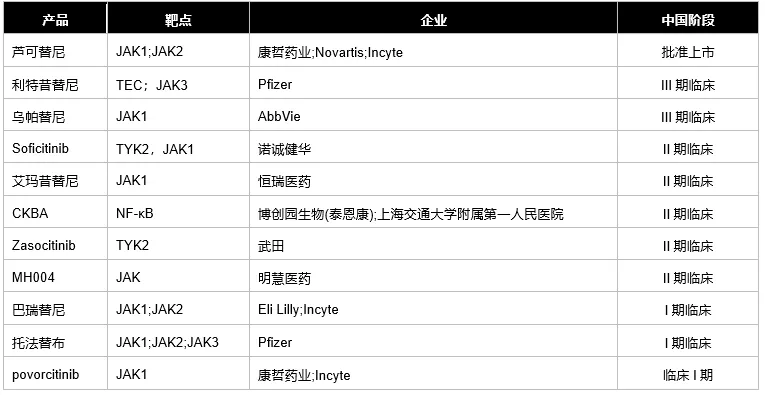
表:白癜风药物竞争格局
表来源:医药魔方
(1)芦可替尼乳膏(OPZELURA)由Incyte研发。基于两项三期临床试验数据(TRuE-V1 and TRuE-V2),FDA于2022年7月批准了OPZELURA芦可替尼乳膏用于局部治疗成人和12岁及以上儿童患者的非节段性白癜风。TRue-V1共纳入330例患者,使用芦可替尼乳膏的患者在治疗24周后,有29.9%的患者达到面部白癜风面积评分指数相对基线改善至少75%(F-VASI 75);而安慰剂组仅为7.5%。TRue-V2研究纳入344例患者,使用芦可替尼治疗的患者在24周时,F-VASI 75的应答率为29.9%,安慰剂组为12.9%。

图:芦可替尼乳膏治疗白癜风数据优异
数据来源:康哲药业官网
康哲药业于2022年12月通过附属公司康哲美丽与Incyte就用于芦可替尼乳膏订立合作和许可协议,将这一潜力产品收入囊中。凭借中国真实世界研究中取得的积极结果,康哲药业迅速芦可替尼乳膏的上市进程。2024年9月, 芦可替尼乳新药上市许可申请(NDA)获得中国国家药品监督管理局(NMPA)受理,将成为首个国内上市的白癜风治疗处方药。
(2)瞄准白癜风市场,康哲药业加速布局了第二款白癜风产品——Povorcitinib。2024年4月,康哲药业与Incyte就开发和商业化选择性口服JAK1抑制剂povorcitinib订立合作和许可协议,获得其在中国大陆、香港、澳门、台湾及东南亚十一国的研究、开发、注册及商业化产品的独家许可权利,以及在区域内生产产品的非独家许可权利。
Povorcitinib是由Incyte研发的一种小分子选择性 JAK1 抑制剂,目前处于临床Ⅲ期。Ⅱb期研究显示,在24周时,Povorcitinib与安慰剂相比,总体和面部白斑面积评分指数(T-VASI;F-VASI)指标在统计学上显著改善。171 名白癜风患者随机分配到每日一次口服剂量为 15、45 或 75 毫克的povorcitinib 或安慰剂组,持续 24 周。主要结果显示,24周T-VASI 50分别为10.5%(Povorcitinib 15mg)、15.2%(Povorcitinib 45mg)、5.6(Povorcitinib 75mg)和3%(安慰剂)。24周F-VASI 50分别为18.4%(Povorcitinib 75mg)、45.5%(Povorcitinib 15mg)、27.8%(Povorcitinib 45mg)和9.1%(安慰剂)。24周F-VASI 75分别为13.2%(Povorcitinib 75mg)、18.2%(Povorcitinib 15mg)、13.9%(Povorcitinib 45mg)和3%(安慰剂)。
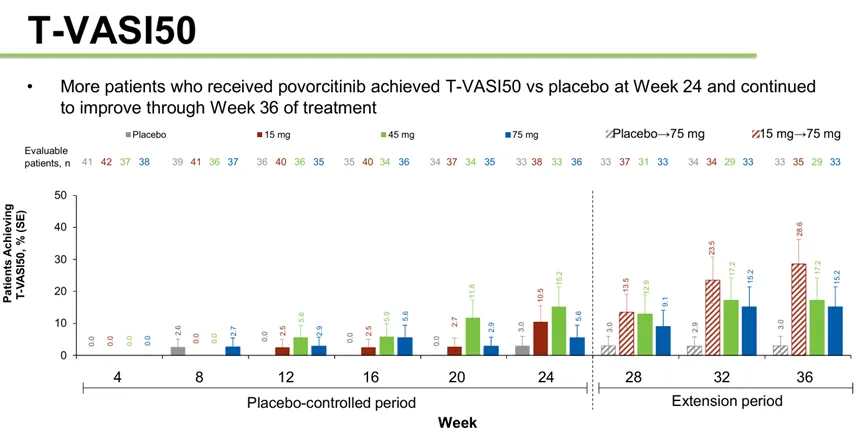
图:povorcitinib治疗白癜风的T-VASI 50数据
数据来源:Incyte
(3)利特昔替尼是由辉瑞研发的一种激酶抑制剂,能够不可逆地抑制 JAK3和酪氨酸激酶家族。利特昔替尼首个适应症——重症斑秃于2023年6月在美国批准上市。
利特昔替尼白癜风适应症处于临床Ⅲ期。Ⅱb研究结果显示,与安慰剂相比,在有负荷剂量(-21.2 vs 2.1;P<0.001)或无负荷剂量(-18.5 vs 2.1;P<0.001)的利特昔替尼50 mg组和30 mg组(-14.6 vs 2.1;P=0.01)中,面部白癜风面积评分指数的变化百分比相比基线有显著改善(n=187)。
(4)CKBA软膏由泰恩康研发,可通过靶向ACC1和MFE2调控细胞脂代谢,抑制CD8+T细胞产生效应分子与发挥效应功能。CKBA软膏治疗白癜风处于临床II期。
2025年8月,泰恩康宣布CKBA软膏在非节段型白癜风患者中表现出积极的疗效和良好的安全性,支持继续开展III期确证性临床试验。高剂量组CKBA软膏1.5% BID剂量组的面颈部白癜风评分指数达到F-VASI 50和F-VASI 25的受试者比例均优于安慰剂组,其中疾病好转及不同程度复色患者占比为36%(18/50)。CKBA软膏1.5% BID剂量组和溶媒组(安慰剂组)的药品相关不良事件(TEAE)发生率分别为18%和12%;未发生与试验用药品相关的严重不良事件(SAE),CKBA 软膏具有良好的安全性和耐受性。
(5)Soficitinib(ICP-332)是一款由诺诚健华在研的高效、高选择性的新型口服TYK2抑制剂,正在被开发用于治疗各种T细胞相关的自身免疫性疾病,包括白癜风、特应性皮炎、结节性痒疹等。TYK2/JAK1抑制剂通过阻断IFN-γ和IL-15等细胞因子介导的JAK-STAT信号通路,抑制自身免疫性T细胞对黑色素细胞的攻击,从而促进白癜风皮损恢复。
2025年5月16日,诺诚健华宣布,Soficitinib治疗非节段型白癜风的2/3期临床试验在中国完成首例患者给药。截至2026年1月,Soficitinib治疗白癜风的II期临床试验也已经完成患者入组。
(三)小结
作为一种慢性、毁容性自身免疫性皮肤疾病,白癜风治疗迫切性强;此外,我国白癜风患者达1400万,白癜风市场潜力巨大。随着芦可替尼乳膏的上市,我国白癜风患者迎来治疗的新手段,芦可替尼乳膏全球销售额已突破5亿美元,期待未来在国内市场的放量。
 产业资讯
产业资讯
 摩熵医药
摩熵医药  2026-05-07
2026-05-07
 260
260

 产业资讯
产业资讯
 生物药大时代
生物药大时代  2026-05-07
2026-05-07
 295
295

 产业资讯
产业资讯
 药渡
药渡  2026-05-07
2026-05-07
 269
269
 热门资讯
热门资讯