 研发追踪
研发追踪
 医道社创新药新前沿
医道社创新药新前沿  2026-03-02
2026-03-02
 1437
1437
大家好,我是你们的创新药博主老汤。作为专注罕见病领域的从业者,我每天刷PubMed和FDA公告,总能被那些真正触及病根的突破震撼到。今天,我想和各位临床医生和药品研发同行聊聊一个可能重塑弗里德赖希共济失调(Friedreich’s Ataxia,简称FRDA或FA)治疗格局的消息:Larimar Therapeutics的核心候选药Nomlabofusp(前身为CTI-1601)刚刚斩获FDA的突破性疗法认定(Breakthrough Therapy Designation,BTD)。这不是简单的“加分项”,而是基于开放标签临床数据,FDA对它作为潜在“疾病修饰”疗法的最高认可。更关键的是,在START试点会议中,FDA还“愿意考虑”皮肤Frataxin(FXN)水平作为新型替代终点,支持加速审批路径。
为什么这事儿让业内人眼前一亮?FRDA这种遗传性“隐形杀手”折磨着全球约2万患者,美国就有5000人(FRDA国家基金会数据),发病高峰在儿童期,导致行走困难、肌肉萎缩、心肌病、脊柱侧弯,甚至早发性心脏衰竭。平均寿命缩短到30-40岁,生活质量评分(FARS)每年恶化5-10分。到现在,治疗还停留在对症支持阶段——物理疗法缓解共济失调,β受体阻滞剂管心脏症状,Idebenone(欧盟批准)试着抗氧化。但这些都治标不治本,无法逆转核心病因:线粒体蛋白FXN的严重缺乏(患者水平仅正常人的21%-32%,《Molecular Genetics and Metabolism》2010年研究)。
Larimar这家临床阶段生物技术公司,总部在宾夕法尼亚州巴拉辛维德,正用一套“细胞内蛋白递送”黑科技直击痛点。基于FDA 2026年2月24日公告、Larimar新闻稿,以及2025年《The AAPS Journal》那篇机制论文,我来和大家深度拆解Nomlabofusp的技术细节、临床证据、公司策略和潜在风险。咱们一步步来,看看它为什么不是“又一个FRDA药”,而是一次平台级押注,能否真把FRDA从“无药时代”拉出来。
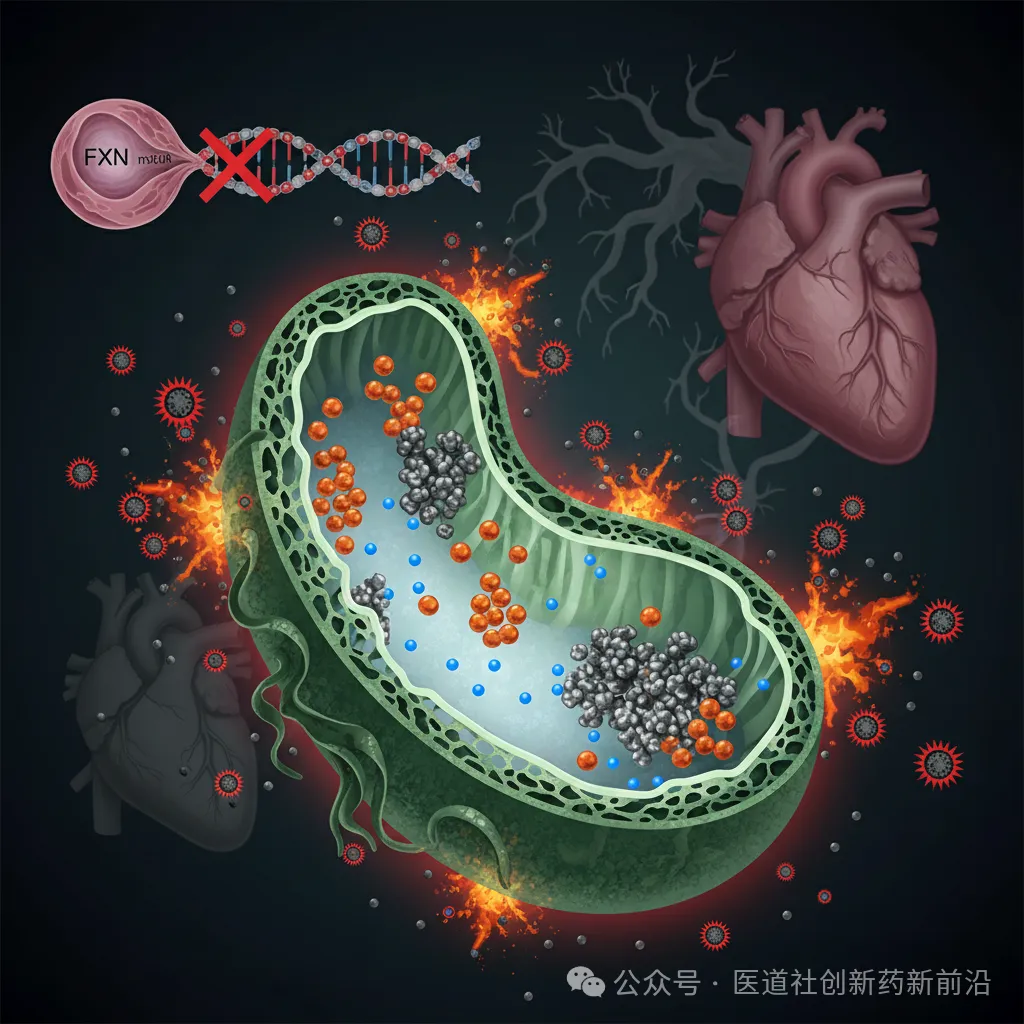
第一部分:FRDA的“病根”剖析——为什么传统疗法总在外围打转?
先说说FRDA的核心病理,这对临床医生和研发人员来说是基础,但也最容易被忽略的痛点。FRDA 97%的病例由FXN基因GAA三核苷酸重复扩增引起,导致转录阻滞,FXN蛋白产量锐减。FXN是一种核编码的线粒体蛋白:在细胞质合成后,通过N端线粒体靶向序列(MTS)导入线粒体,经线粒体加工肽酶(MPP)裂解成成熟形式(mFXN,约14kDa)。它的关键作用?调控铁硫簇(Fe-S cluster)生物合成,这是线粒体呼吸链酶(如琥珀酸脱氢酶)和柠檬酸循环酶(如异柠檬酸脱氢酶)的“prosthetic group”。缺了它,铁过载、氧化应激爆发、能量代谢崩溃,最终波及神经、心脏和骨骼系统。
想象一下:一个10岁孩子从蹒跚学步到轮椅依赖,只用几年时间。这不是科幻,而是FRDA的残酷现实(《The Lancet Neurology》2023年综述)。FXN水平与发病年龄、进展速度、严重程度呈强相关——越低,发病越早、越重(AAPS Journal 2025年引述)。当前疗法?仅对症:Idebenone缓解氧化应激,但改善率<20%,无法触及根源。基因疗法有潜力,但递送效率<50%、安全隐患大。蛋白替代听起来直接,但面临两大“天堑”:
·细胞膜屏障:蛋白是大分子,难穿越“城墙”进入细胞。
·线粒体膜屏障:进了细胞质,还得穿过双层膜进基质发挥作用。
《Journal of Multidisciplinary Healthcare》2021年综述强调,FRDA的“未满足需求”巨大——没有疾病修饰疗法。这就是FDA授予BTD的基础:Nomlabofusp的初步数据在临床终点上“显著优于现有疗法”。
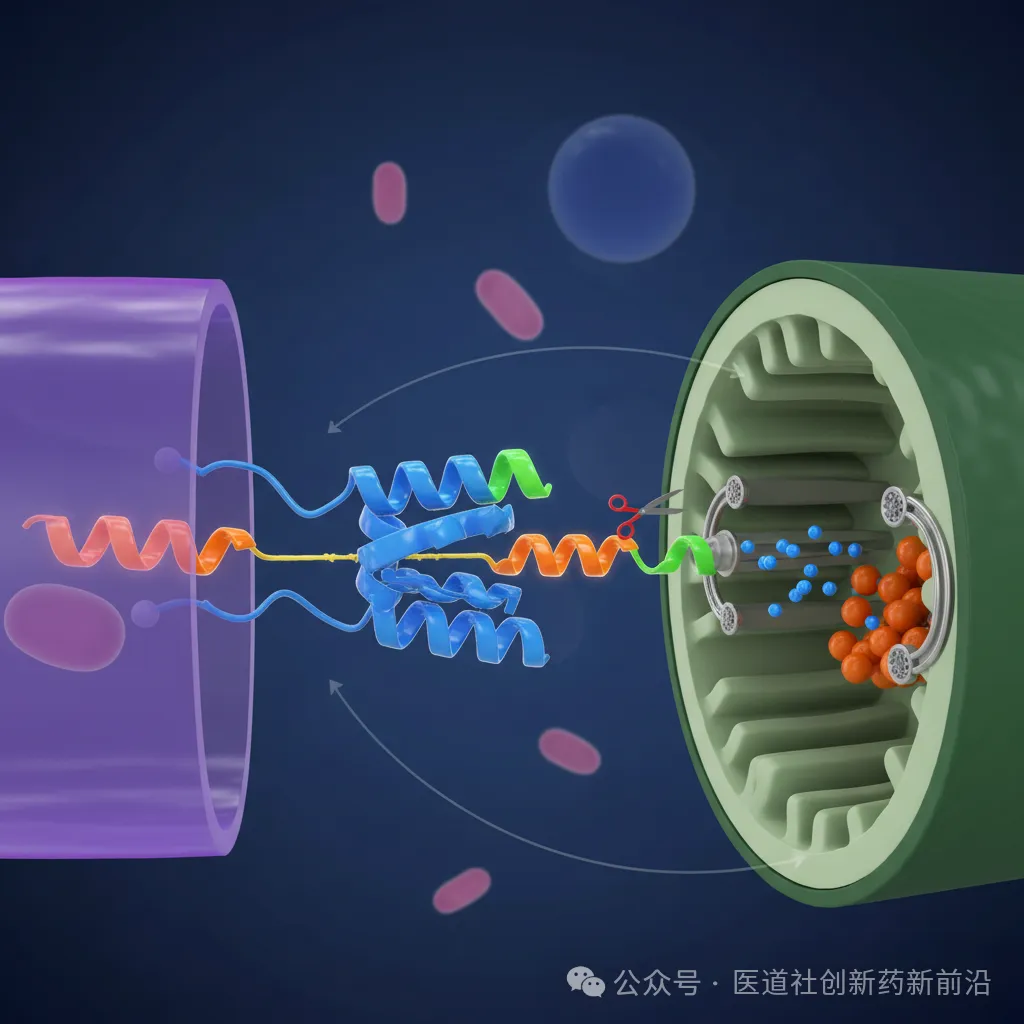
第二部分:Nomlabofusp的“三位一体”设计——从“进门”到“解锁”的蛋白钥匙
Nomlabofusp不是简单FXN补充,而是Larimar专有平台的巅峰:一种224氨基酸的融合蛋白(24.9kDa),核心是人类完整FXN(含MTS和成熟序列),N端通过二甘氨酸连接器融合阳离子细胞穿透肽(CPP),基于HIV TAT序列(YGRKKRRQRRR)。这套设计像一把精妙“蛋白钥匙”,完美复刻内源路径,解决递送难题。咱们从机制论文(AAPS Journal 2025)一步步拆。
1. 突破细胞膜:TAT-CPP的“万能钥匙头”
传统蛋白药(如胰岛素)只能在外游荡。TAT-CPP利用阳离子特性,通过脂筏介导的胞吞(caveolar endocytosis)和巨胞饮(macropinocytosis)高效入胞。2004年《Nature Medicine》研究显示,TAT融合效率>80%,广谱分布神经、心肌、骨骼组织——对FRDA全身缺陷正合适。非临床数据显示,小鼠模型中组织分布均匀,皮下注射半衰期约24小时。
体外证据:在H9c2心脏肌母细胞和SH-SY5Y神经母细胞,10μM暴露3天,免疫荧光显示人类FXN与线粒体标志Tomm20共定位(白箭头指向信号强度提升5倍)。即使FXN敲低模型(模拟FRDA,内源<10%),摄取不变。点状内体和核信号也符合TAT特征,论文据文献解释。
2. 精准线粒体导入与加工:MTS+MPP的“导航+拆箱”闭环
进了细胞,MTS像GPS引导穿越外/内膜进基质。MPP裂解CPP-MTS,释放纯净mFXN——与内源路径100%一致,避免免疫原性。Western blot证实:处理后~14kDa mFXN带仅在线粒体馏分(细胞质无信号)。在HEK293和C2C12细胞,mFXN剂量依赖升高(10μM时2倍,20μM时4倍)。
亮点:TAT不干扰MTS,MPP后CPP-MTS排出,防“逆流”。《Human Molecular Genetics》2012年报道,类似TAT-FXN在FRDA小鼠延长寿命20%、改善心脏——Larimar优化后,生物活性恢复>90%(公司数据)。亚细胞分离证明:nomlabofusp本体25-30kDa,成熟FXN~14kDa出现在线粒体组分(H9c2/SH-SY5Y均如此)。
在FXN敲低肌细胞/HEK293,nomlabofusp仍剂量依赖补回成熟FXN——回答了“低FXN背景影响摄取/加工”的担忧。
3. 功能验证:不止递送,还“活起来”
不止运货,它恢复FXN生物学。论文显示,在FRDA患者口腔拭子,13天100mg皮下注射,mFXN 4.7倍升高(LC-MS/MS,pg/μg总蛋白;个体4.5、3.6、6.1倍),停止后回落。免疫沉淀+WB:pool样本Day13成熟FXN明显增强,fold-change与LC-MS一致。
转录组:Nanostring nCounter面板(243基因),BTG2、EGR1、SOD2、XPO6从FRDA基线低水平向健康人趋近(SOD2与FXN相关r=0.75,《Antioxidants & Redox Signaling》2013年;EGR1涉神经可塑性)。一年治疗,皮肤FXN达无症状携带者~50%正常,mFARS改善趋势(vs. FACOMS自然史恶化5分/年)。
Phase 1 MAD(NCT04519567,2024年《Annals of Clinical and Translational Neurology》):n=30,FXN皮肤/口腔4.5-6.1倍升高(100mg组),临床终点(ADL、9-HPT、MFIS)持续改善,无严重不良事件。相比Idebenone,这直击病因。
第三部分:临床与机制证据链——从细胞到人体的“硬核”闭环
证据不是空谈。开放标签研究(n≈20)显示暴露-反应关系(FXN升高与mFARS改善r>0.6)。皮肤FXN作为可重复采样,反映全身效应——口腔/皮肤样本证明成熟FXN上升+转录“拨乱反正”。
震撼数据:Phase 1安全优秀,耐受好。一年治疗,四项量表均改善,与自然史对比鲜明。论文强调:这些是“药效学活动(intracellular PD activity)”信号,虽非临床获益证明,但加分明显。FRDA缺分子PD标志物,这套证据填补空白。
第四部分:Larimar的公司实力——专注罕见病,监管“快车道”全开
成立于2018年,Larimar专注“细胞内生物活性化合物缺乏”的遗传病,核心源于印第安纳大学R. Mark Payne博士发现。市值约3亿美元(2024年2月),但效率高:IND到Phase 2仅3年。生产由KBI Biopharma GMP级负责。
1. 平台扩展性:不止FRDA,还瞄准更多“蛋白黑洞”
TAT-CPP+MTS模块化,可定制融合蛋白,针对范可尼贫血等。知识产权覆盖20年,已生成5+候选。非病毒、非基因编辑,更安全、低成本。相比Biogen基因疗法(效率<50%),Larimar精准可控。
2. 监管金字塔:BTD+多重资格,加速上市
BTD(2026年2月基于OL数据)允许优先审查、滚动提交。另有罕见儿科药(RPDD)、Fast Track、孤儿药(FDA/EMA),EMA PRIME加速欧盟。START中,FDA支持皮肤FXN作为surrogate endpoint,预测临床获益——绕过漫长3期。
里程碑:2024 Q2 OL数据;2024 Q2启动全球Phase 3(法国/加拿大/UK/澳洲);2026年6月BLA,优先审评;2027 H1美国上市。覆盖90%患者。团队强:CEO Carole Ben-Maimon(前Teva罕见病专家),CMO Rusty Clayton(神经遗传)。“患者优先”如Uncommon Cures合作,确保数据真实。
商业潜力:FRDA市场>10亿美元(GlobalData 2023),定价10-20万USD/年。用FACOMS匹配自然史比较,监管友好——FDA确认人群选择和统计计划。
第五部分:风险直面——专业视角下的不确定性
作为医生和研发者,我们得把风险说透,不能只看利好。基于材料,主要有四点:
·外周 vs 靶器官:口腔/皮肤FXN升,能否代表DRG/小脑/心肌?多细胞系证明入胞入线粒体,但人体组织暴露效率待证。
·基因表达相关性:BTG2等变化是信号,但临床相关性需进一步研究;出现晚(Day 22),持续未知。
·安全数据库:Phase 1/2好,但BLA时FDA审查充分性。
·替代终点命运:“愿意考虑”非背书。FXN提升对临床获益的因果链需说服监管;暴露-反应分析正确,但最终取决于证据。
这些风险真实,但Larimar的机制证据“可监管化”(WB区分分子量、亚细胞分离、PD追踪),让路径更稳。
结语:Nomlabofusp点亮FRDA“线粒体之光”——一个新时代的黎明
朋友们,FRDA患者诊断后5年内50%丧失行走,30岁前心衰风险高。但Nomlabofusp如一道光:CPP+MTS+MPP工程化,把成熟FXN精准送入“铁硫工厂”,逆转基因诨咒。基于4.7倍FXN升高、成熟加工证据、基因正常化、临床改善——我坚信,这是首个FRDA疾病修饰药,2027上市将救5000美国患者。
Larimar不只做一个药,而是推“细胞内/线粒体内蛋白缺失”向平台化和监管化。科学上,攻克“不可成药”堡垒;临床上,开放标签趋势逆转自然史;监管上,皮肤FXN创新终点重塑罕见病审批。从绝望到希望,这或许是治疗新时代的教科书。
临床医生们,这对患者管理是福音;研发人员们,平台扩展值得借鉴。关注Larimar(LRMR),盘前+30%是市场投票。欢迎留言交流你的看法,我们下期见!
原文链接:

 研发追踪
研发追踪
 医药时间
医药时间  2026-05-04
2026-05-04
 457
457

 研发追踪
研发追踪
 药讯随说
药讯随说  2026-05-04
2026-05-04
 460
460

 研发追踪
研发追踪
 医药笔记
医药笔记  2026-05-04
2026-05-04
 442
442
 热门资讯
热门资讯