 产业资讯
产业资讯
 医药魔方Pro
医药魔方Pro  2026-03-10
2026-03-10
 272
272
对于创新药研发而言,新靶点的发现堪称撬动行业突破的 “金钥匙”。 历史上,TNF-α、PD-1、GLP-1R、IL-4Rα、IL-12p40等里程碑靶点的成功转化,不仅为患者带来了全新的突破性治疗选择,重塑了相关疾病领域的格局,同时催生了多款年销售额超百亿美元的超级重磅炸弹药物,书写了生物医药领域的一个又一个传奇。
2021、2022、2023及2024年,医药魔方Pro连续推出《100个新靶点》年度盘点文章,受到了行业的持续关注。
刚刚过去的2025年,新靶点依旧不断涌现。本文梳理并筛选出了2025年值得关注的100个新靶点(详见文末表格),为国内创新药研发提供参考(本文新靶点定义为针对各类适应症的全新靶点以及发现新适应症、新应用的“老靶点”)。
从疾病领域来看,癌症相关靶点占比最高(占50%),包括VDAC2、EPO/EPOR、PPP2R1A、SERT、AOAH、GLUD1 等多个癌症免疫治疗新靶点,以及RUNX2、CD21、IFN-γR、LARP4等CAR-T细胞疗法相关新靶点。
在神经退行性疾病领域,FAM171A2、TIM-3、MEK1/2、TMEM119、GADD45G、ZBP1等新靶点值得关注。代谢性疾病相关的新靶点包括ALKBH5、FGF13、G3BP1、TCPTP等。
除此之外,过去一年,肥胖、多发性硬化症、动脉粥样硬化、肺纤维化、骨关节炎、杜氏肌营养不良症、慢性肾病、高血压、缺血性心肌损伤、移植物抗宿主病等疾病领域在新靶点发现方面也有积极进展(详见文末表格)。
值得一提的是,2025年值得关注的100个新靶点中,超半数靶点由中国科学家团队发现(文末表格加粗靶点),多项原创性成果登上Cell、Nature、Science等顶级期刊。这些成果不仅彰显出中国科研团队在全球靶点发现与转化研究中的重要贡献,也体现了我国在生物医药源头创新方面日益提升的硬实力及影响力。
从突破性角度,在这100个新靶点中,有近30个靶点具有重要意义,部分入选医药魔方NextPharma转化医学里程碑成果,以下选择其中的15个里程碑靶点做详细介绍:
里程碑靶点①:PELO
杂志:Nature
领域:癌症(合成致死)
论文:DOI: 10.1126/scitranslmed.adp8913
成果:来自Broad研究所及哥伦比亚大学的一个科学家团队发现,大约5%的成人癌症严重依赖一种名为PELO的基因存活,而这种基因的失活能够杀死FOCAD或TTC37基因突变的癌细胞。这项成果于2025年2月5日发表在Nature杂志上,是合成致死领域的新发现。科学家们认为,PELO是一个很有希望的合成致死新靶点,基因检测有望鉴定出携带FOCAD或TTC37突变的癌症患者,这类患者将获益于PELO靶向药物。(详细报道)
里程碑靶点②:CGRP
杂志:Nature
领域:癌症(胃癌)
论文:DOI: 10.1038/s41586-025-08591-1
成果:2025年2月19日,发表在Nature杂志上的一项研究中,来自哥伦比亚大学欧文医学中心、南通大学附属医院等机构的一个科学家团队发现,小鼠的胃癌会与附近的感觉神经产生电连接,并利用这些恶性回路刺激癌症的生长和扩散。这是首次发现大脑之外的癌症与神经之间产生电连接。
迷走神经中包含许多不同类型的神经元,在这项研究中,科学家们主要关注感觉神经元,因为这类神经元对小鼠胃癌的存在反应最为强烈。其中一些感觉神经元延伸到胃肿瘤深处,以响应癌细胞释放的一种叫做神经生长因子(NGF)的蛋白质。在建立这种联系(两者靠近)后,肿瘤向感觉神经发信号,使其释放一种名为CGRP的肽,在肿瘤内诱发电信号。进一步研究显示,这种电回路的形成促进了胃癌的发展和转移。
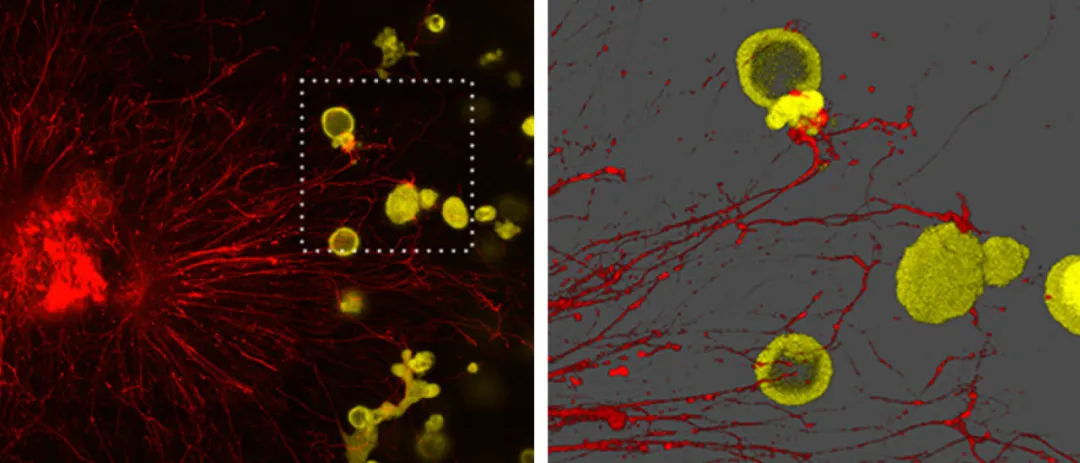
当感觉神经元(红色)与胃癌类器官(黄色)一起培养时,神经元和癌细胞建立了类似突触的连接,并在细胞之间建立了电回路。(来源:Timothy Wang /
Columbia University Vagelos College of Physicians and Surgeons)
对于胃癌来说,目前用于治疗偏头痛的CGRP抑制剂可能会使肿瘤和感觉神经元之间的电回路短路。该研究显示,用CGRP抑制剂治疗胃癌小鼠能够缩小肿瘤的大小,延长生存期,并阻止肿瘤扩散。(详细报道)
里程碑靶点③:FAM171A2
杂志:Science
领域:帕金森病
论文:DOI: 10.1126/science.adp3645
成果:2025年2月21日,发表在Science杂志上的一项研究中,复旦大学附属华山医院郁金泰教授团队联合复旦大学脑科学转化研究院袁鹏教授及中国科学院上海有机化学研究所刘聪教授团队全球首次发现了帕金森病全新治疗靶点FAM171A2,并找到了具有潜在治疗作用的小分子化合物。此次研究发现的全新治疗靶点和候选药物有望从疾病早期对帕金森病进行干预,延缓疾病进展。结合现有的对症治疗手段,将会实现帕金森病病因治疗与症状缓解的双重突破,造福数百万患者。(详细报道)
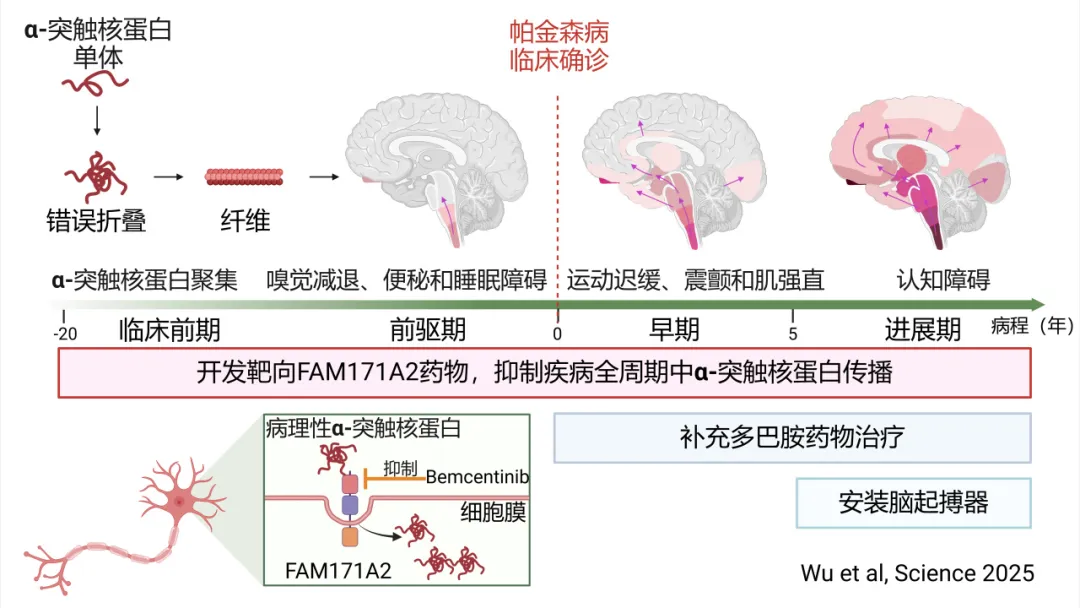
帕金森病病程进展机制及干预手段
里程碑靶点④:ALKBH5
杂志:Science
领域:糖尿病、代谢相关脂肪性肝病
论文:DOI:10.1126/science.adp4120
成果:2025年2月28日,哈工大生命科学中心陈政课题组在糖脂代谢稳态整合调控和代谢性疾病发病机制方面取得重要进展。研究成果发表在顶级期刊Science杂志上。该研究表明,ALKBH5在肥胖期间上调,并通过不同的途径调节葡萄糖和脂质稳态。肝细胞特异性缺失Alkbh5可通过抑制GCGR–cAMP和EGFR-PI3K-AKT-mTORC1信号通路改善糖耐量,减轻肥胖小鼠的代谢相关脂肪性肝病。靶向敲低Alkbh5可逆转糖尿病小鼠的2型糖尿病和代谢相关脂肪性肝病,强调其治疗潜力。(详细报道)
里程碑靶点⑤:VDAC2
杂志:Nature
领域:癌症(免疫疗法)
论文:DOI: 10.1038/s41586-025-08732-6
成果:2025年3月19日,来自St. Jude Children’s Research Hospital的科学家团队发表在Nature杂志上的一项研究揭示了一些癌细胞如何利用一种名为VDAC2的蛋白阻止身体的抗癌系统与免疫系统交流。
正常情况下,T细胞发现癌细胞,会释放干扰素-γ,这是一种阻止肿瘤生长的有效细胞因子。然而,在许多癌症中,干扰素-γ对直接杀死肿瘤的作用有限,这阻碍了抗癌治疗。在这项新研究中,科学家们发现,VDAC2在其中发挥了破坏作用。在干扰素-γ存在的情况下去除VDAC2直接增加癌细胞的死亡,且使肿瘤更加“炎性”,从而使肿瘤更容易受到各种免疫治疗的影响。这些发现揭示了VDAC2可作为克服肿瘤免疫逃避的新靶点。(详细报道)
里程碑靶点⑥:TIM-3
杂志:Nature
领域:阿尔茨海默病
论文:DOI: 10.1038/s41586-025-08852-z
成果:小胶质细胞是大脑中的常驻免疫细胞,在神经发育和神经炎症中起着关键作用。全基因组关联研究(GWAS)表明,许多与迟发性阿尔茨海默病(AD)相关的基因在小胶质细胞中特异性表达。
TIM-3是一种免疫检查点分子,参与免疫和炎症,最近被发现与迟发性阿尔茨海默病有关,但其在大脑中的具体作用尚不明确。2025年4月9日,来自Brigham and Women’s Hospital的一个科学家团队在Nature杂志发表最新成果。研究使用临床前模型揭示了TIM-3在小胶质细胞中的作用,并将其确定为阿尔茨海默病的一个有前途的治疗靶点。(详细报道)
里程碑靶点⑦:EPO/EPOR
杂志:Science
领域:癌症(免疫疗法)
论文:DOI: 10.1126/science.adr3026
成果:2025年4月25日,发表在Science杂志上的一项研究中,来自斯坦福大学的一个科学家团队发现,近40年前发现的一种能够刺激红细胞生成的蛋白质——促红细胞生成素(EPO)——在抑制抗癌免疫反应方面发挥着令人惊讶的关键作用。
研究发现,肿瘤细胞需要分泌EPO来逃避免疫攻击。在肝癌模型中,肿瘤来源的EPO水平增加与免疫抑制肿瘤微环境有关。阻断肿瘤分泌的EPO或巨噬细胞上的EPO受体均可促进T细胞浸润,改善肝癌的控制。这些发现表明,EPO/EPOR轴是一个有希望的癌症免疫治疗靶点。鉴于EPO高表达与多种实体肿瘤的不良预后相关,靶向EPO/EPOR轴可能对多种肿瘤有效。(详细报道)
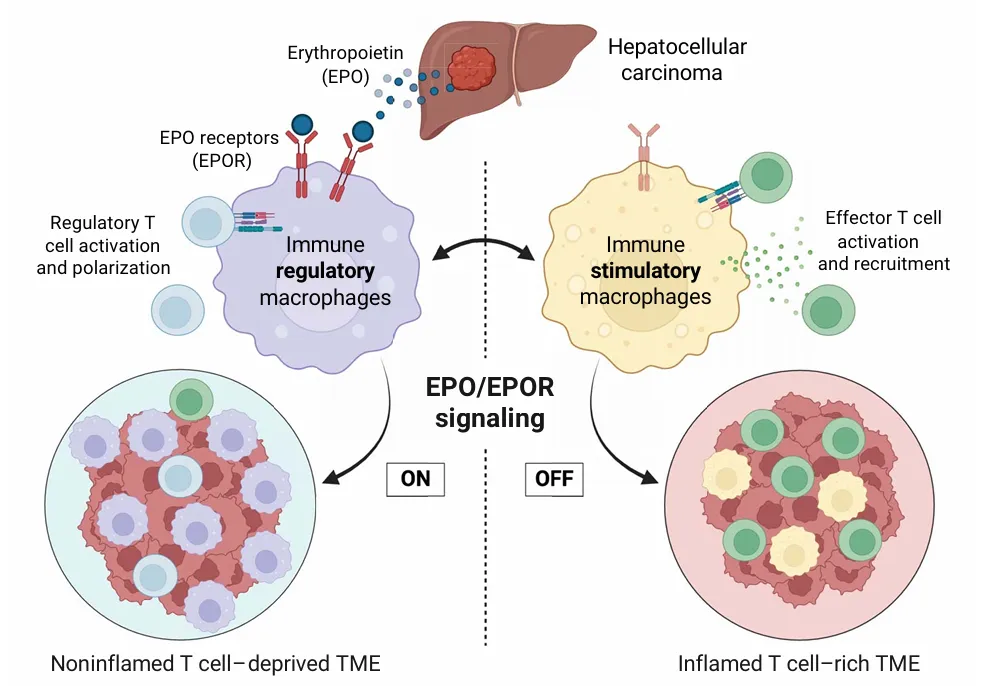
肿瘤来源的EPO与肿瘤相关巨噬细胞上的EPOR结合,阻止其分化为驱动效应T细胞(绿色)激活和募集的免疫刺激巨噬细胞。EPO刺激的巨噬细胞还会促进reg细胞(蓝色)激活,维持非炎性(T
cell–deprived)的肿瘤微环境(TME)。靶向巨噬细胞中的EPO/EPOR轴可将非炎性TME转化为炎性TME。(来源:Science)
里程碑靶点⑧:CREM
杂志:Nature
领域:癌症(CAR-NK细胞疗法)
论文:DOI: 10.1038/s41586-025-09087-8
成果:CAR-NK细胞能够特异性地识别并结合癌细胞表面的抗原,进而激活自身的杀伤功能来攻击肿瘤。然而,尽管CAR-NK细胞疗法展现出巨大潜力,但其活性调控的分子细节仍需深入探索。
2025年6月4日,Nature杂志上线了一篇论文,来自德克萨斯大学MD Anderson癌症中心等机构的研究团队揭示了一种名为cAMP反应元件调节因子(cyclic AMP response element modulator,CREM)的蛋白质。研究发现,CREM在CAR-NK细胞中扮演着关键的检查点调节因子角色,其表达水平一旦上调,就会显著限制CAR-NK细胞的有效性,对其进行的基因敲除能够显著增强CAR-NK细胞的抗肿瘤活性。(详细报道)
里程碑靶点⑨:PPP2R1A
杂志:Nature
领域:癌症(免疫疗法)
论文:DOI: 10.1038/s41586-025-09203-8
成果:2025年7月2日,发表在Nature杂志上的一篇论文中,来自德克萨斯大学MD 安德森癌症中心的一个科学家团队发现,肿瘤中具有特异性 PPP2R1A 突变的卵巢透明细胞癌(ovarian clear cell carcinoma, OCCC)患者在接受免疫检查点阻断治疗后总生存期(OS)和无进展生存期显著延长。
基于在OCCC患者中的发现,研究人员还调查了另外两个独立的队列,一个由子宫内膜癌患者组成,另一个包括9000多名接受免疫治疗的多种癌症患者。分析同样证实了PPP2R1A突变肿瘤患者在接受免疫治疗后OS的改善。
与此同时,临床前研究表明,在接受多种免疫治疗(包括免疫检查点阻断疗法和CAR-T细胞疗法)的体外和体内模型中,通过药理学抑制或遗传修饰靶向PPP2R1A均与生存改善有关。这些结果表明,靶向PPP2R1A可能是改善免疫检查点阻断或其他形式免疫治疗患者预后的有效策略。(详细报道)
里程碑靶点⑩:SERT
杂志:Cell
领域:癌症(免疫疗法)
论文:DOI: 10.1016/j.cell.2025.04.032
成果:鉴定阻碍抗肿瘤 T 细胞反应的其他免疫检查点,是开发新一代癌症免疫疗法的关键所在。2025年7月10日,来自加州大学洛杉矶分校等机构的科学家在Cell杂志发表最新成果,研究发现,在肿瘤浸润CD8 T细胞中存在血清素转运蛋白(SERT)的诱导表达。SERT是一种调节大脑及周围组织中血清素水平和生理功能的物质。进一步的研究显示,通过使用SSRIs(selective serotonin reuptake inhibitors,最常被使用的抗抑郁药物)抑制SERT,显著抑制了多种小鼠同种异体和人类异种移植肿瘤模型中的肿瘤生长,并增强了 T 细胞的抗肿瘤免疫能力。此外,SSRI治疗与PD-1阻断具有显著的协同治疗效果。
临床数据关联研究表明,在多种癌症中,肿瘤内SERT的表达水平与患者生存期呈负相关。机制方面,SERT 起到一种负反馈调节的作用,它通过减少肿瘤内 T 细胞自分泌的血清素来抑制 CD8 T 细胞的反应性。总结来说,这些发现将 SERT 识别为一种新的免疫检查点。
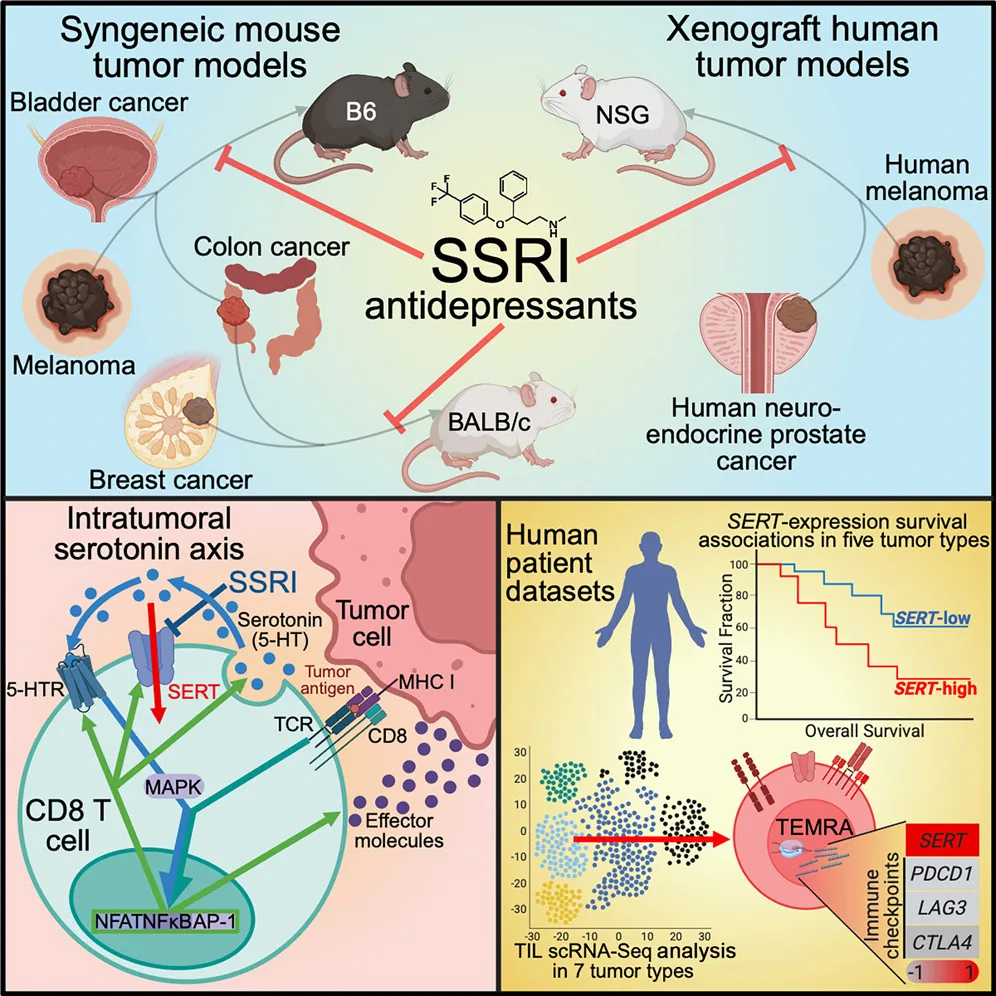
来源:Cell
里程碑靶点⑪:AOAH
杂志:Cell
领域:癌症(免疫疗法)
论文:DOI: 10.1016/j.cell.2025.07.004
成果:分泌蛋白(如细胞因子、生长因子、可溶性酶)是细胞间通讯的核心介质,在免疫反应中起关键作用,是重要的治疗靶点。人类基因组约有1903种编码分泌蛋白的基因,但其中61%在癌症中的功能未知。
2025年9月4日,美国NIH/NCI姜鹏实验室,联合香港大学关新元实验室在Cell上发表论文。通过自主研发的癌症免疫大数据平台CIDE,研究人员首次系统解析了人体中1900余种编码分泌蛋白的基因在肿瘤免疫微环境中的调控作用。
依托体内外模型,研究人员进一步发现,AOAH(acyloxyacyl hydrolase)能特异性清除免疫抑制性卵磷脂及其氧化产物,解除肿瘤免疫抑制,显著增强T细胞受体识别弱抗原的能力并保护树突状细胞的抗原递呈和共刺激功能。此外,该研究同时鉴定出CR1L、COLQ和ADAMTS7等潜在新调控因子和靶点,为实体瘤免疫治疗开辟全新路径。(详细报道)
里程碑靶点⑫:FPR1
杂志:Science
领域:多发性硬化症
论文:DOI:10.1126/science.adq1177
成果:2025 年11 月 13 日,天津医科大学总医院/北京天坛医院施福东课题组在Science杂志发表重要研究成果。该研究聚焦中枢神经系统自身免疫性疾病多发性硬化,揭示了甲酰肽受体1(FPR1)驱动脑区域性炎症和神经退行的新机制,充分验证了甲酰肽受体1(FPR1)能够作为治疗靶点,研发了全新小分子化合物T0080并在临床前确定其疗效,为多发性硬化症等许多神经疾病的治疗带来了新曙光。
里程碑靶点⑬:CCKBR-Gq signaling
杂志:Cell
领域:阿尔茨海默病
论文:DOI: 10.1016/j.cell.2025.10.034
成果:2025年11月20日,北京大学孙金鹏教授与香港城市大学贺菊芳教授,北京大学张勇教授,铁璐副教授,香港中文大学(深圳)杜洋教授,北京宣武医院唐毅主任通力合作,在Cell杂志上发表了题为“Elucidating pathway-selective biased CCKBR agonism for Alzheimer's disease treatment”的研究论文。
该研究从临床问题出发,结合临床样本分析与动物模型,系统阐明了CCKBR下游不同G蛋白信号通路在AD进程中的作用;通过解析内源性激动剂CCK8s激活CCKBR不同G蛋白(Gs、Gq、Gi)的分子机制,揭示了其信号偏向性的结构基础,并以此为基础成功设计出具有治疗潜力的Gq偏向性激动剂3r1。进一步通过动物实验与转录组分析,研究团队证实3r1可通过CCKBR-Gq-Plcb4-Adam10信号轴减轻神经/突触损伤、清除Aβ沉积,为阿尔茨海默病的精准治疗提供了全新策略。(详细报道)
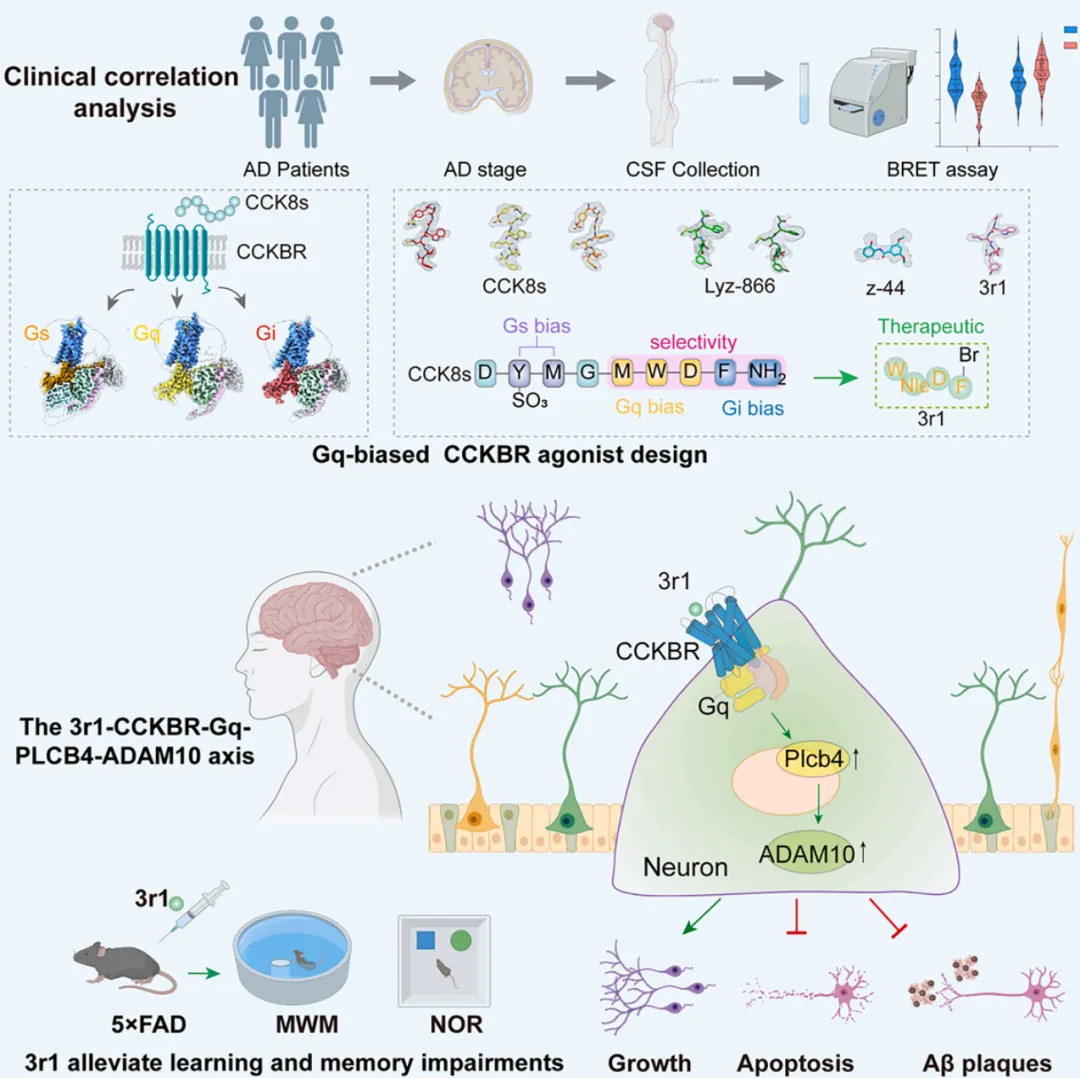
来源:Cell
里程碑靶点⑭:TFAP2β
杂志:Cell
领域:癌症(食管鳞状细胞癌)
论文:DOI: 10.1016/j.cell.2025.11.019
成果:2025年12月16日,四川大学华西医院消化内科、消化系统肿瘤与肝病研究室、四川大学-牛津大学华西消化道肿瘤联合研究中心姜昊教授、杨锦林教授、杨丽教授联合英国牛津大学DavidJ. Kerr教授和华西医院麻醉学研究所柯博文研究员,在Cell杂志发表创新成果。该研究利用多组学联合分析,首次发现食管鳞状细胞癌治疗新靶点TFAP2β,并开发出全球首个以相分离为作用机制、直接靶向TFAP2β相分离行为与功能的小分子化合物A6,突破了食管鳞癌治疗无特异性靶向药物的临床瓶颈。
里程碑靶点⑮:GLUD1
杂志:Cell
领域:癌症(免疫疗法)
论文:DOI: 10.1016/j.cell.2025.11.034
成果:2025年12月24日,徐州医科大学吕凌教授团队联合南京医科大学第一附属医院在Cell杂发表突破性成果。该研究表明,肿瘤产生的氨会被调节性 T 细胞(Treg 细胞 )代谢,增强Treg 细胞,从而进一步阻碍抗肿瘤免疫反应。
研究还发现,抗PD-1治疗诱导的肿瘤细胞死亡可通过转氨反应进一步释放氨,反过来强化肿瘤局部Tregs的免疫抑制功能,促进免疫治疗耐受。在多种肿瘤模型中,靶向抑制氨生成关键代谢酶GLUD1,可显著降低肿瘤内氨水平,削弱Tregs的免疫抑制作用,并明显增强免疫检查点抑制剂的治疗效果。
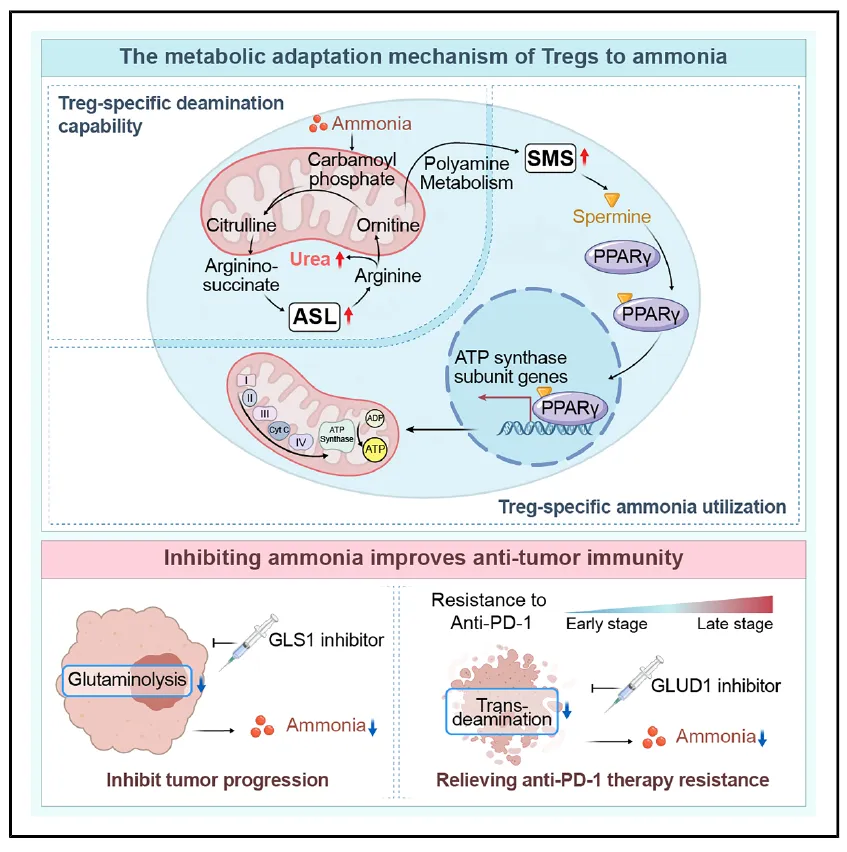
来源:Cell
该研究从代谢角度系统阐明了肿瘤免疫抑制的新机制,提出了“肿瘤来源氨—Tregs代谢适应—免疫逃逸”的全新理论模型,不仅深化了对肿瘤免疫微环境的认识,也为优化肿瘤免疫治疗策略、提高临床疗效提供了重要科学依据。(详细报道)
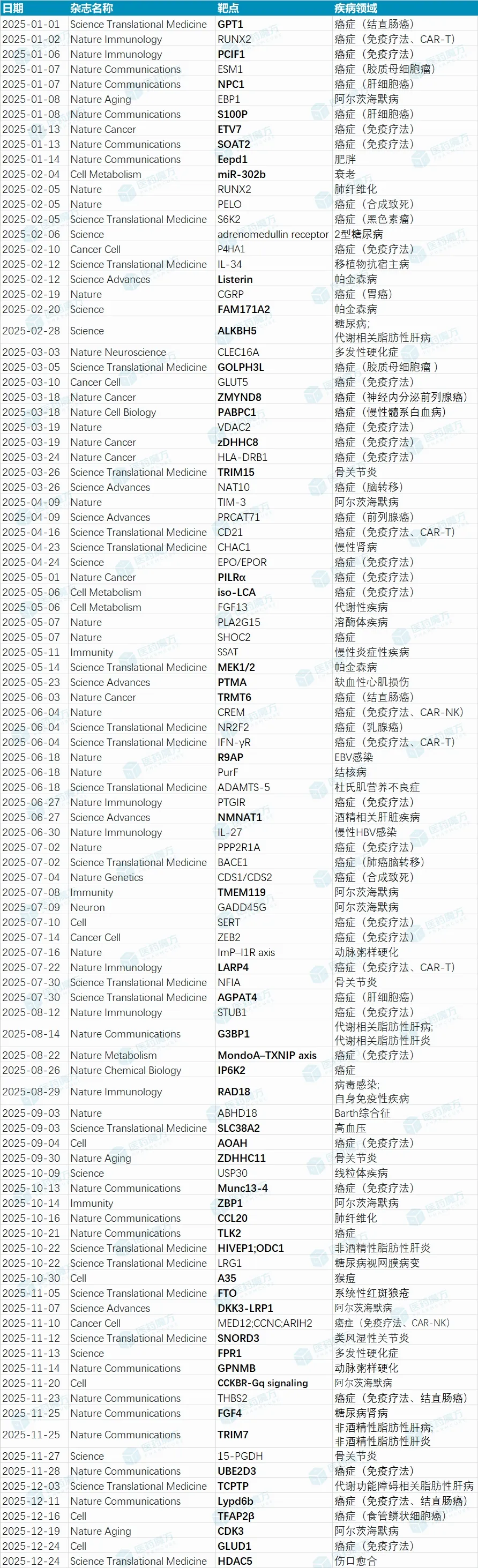
附:2025年值得关注的100个新靶点

 产业资讯
产业资讯
 Innodrugs
Innodrugs  2026-03-23
2026-03-23
 91
91

 产业资讯
产业资讯
 药渡
药渡  2026-03-23
2026-03-23
 83
83

 产业资讯
产业资讯
 药融圈
药融圈  2026-03-23
2026-03-23
 78
78