 产业资讯
产业资讯
 动脉网
动脉网  2026-03-26
2026-03-26
 5
5
进入2026年,RDC领域又有了新的变化。
在过去的一年里,镥-177类核药无疑成为了RDC领域最热的研究方向,诺华重磅产品Pluvicto销售额的持续增长引爆了镥-177类核药的研发热情,包括先通医药、蓝纳成、纽瑞特、通瑞生物、远大医药在内的核药企业都在布局这一方向,甚至百利天恒等ADC企业也加入了镥-177类核药的研发行列之中。
此外,镥-177核素的供应链也取得了突破,这解决了核药的生产瓶颈。2025年,和福一号的核心产品镥-177上市,该项目依托秦山核电基地的商用重水堆,实现了镥-177的规模化生产。四川海同则依托夹江反应堆成功实现镥-177的生产。
随着镥-177核素的商业化问题被突破,以往依赖进口的局面得到改善,镥-177的来源将更加稳定。国内镥-177类核药的研发随即进入爆发期,在研管线数量持续增长。业内预计镥-177类核药的市场竞争也将日趋激烈。
在这种情况下,研究人员开始把目光投向了新型α核药。这一领域成了2026年的研发重点。
01
核药企业看好α粒子
相较于β粒子,α粒子质量更大、能量更高。这一特性使得它能破坏双螺旋链,摧毁DNA,造成局部细胞的毁灭。α粒子的另一个关键优势是其有限的穿透距离,通常只能穿透大约50到100微米,一张纸即可阻挡。因此采用α粒子的疗法可以实现高度局部的效果,即在破坏肿瘤组织的同时避免对附近健康细胞造成伤害。
在肿瘤治疗过程中,相较于β核药,α核药主要有两大优势:一是起效剂量低。以常用的锕-225核药为例,其使用量大概是β核药的千分之一左右,就能达到相同的轰击效果;二是毒性相对较低,主要是α粒子的半径比较短叠加更小的使用剂量,因而带来的细胞毒性也更低。
整体来看,α核药与β核药在肿瘤治疗领域的区别,体现了两种不同的治疗思路。β核药通过相对温和,作用范围广的射线杀伤肿瘤;α核药则凭借其猛烈、范围极短的能量定点清除目标。这两种特性决定了它们各自在对抗癌症时拥有不同的特点,也同时拥有各自的局限。
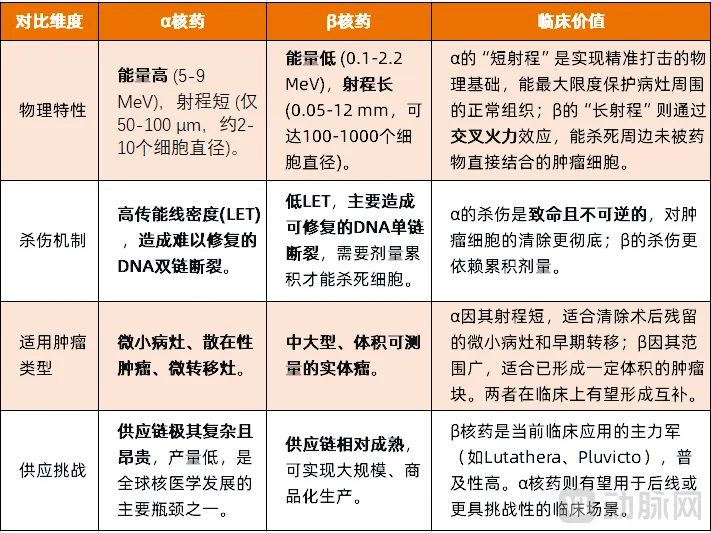
图1. α核药与β核药的区别(动脉网整理)
位于核药产业链上游的CRO企业已经率先感受到了这种变化。据夸克医药创始人苑大为透露,核药领域发生的变化主要体现在几个方面:
1)项目类型变化:过去放射性药物CRO更多是镥-177、诊断核素,现在逐渐出现锕-225、铅-212、砹-211等α核素相关项目。
2)需求更复杂:与β核素(如¹⁷⁷Lu、⁹⁰Y、¹³¹I)相比,α核药的研发链条显著更长、更复杂、更专业化,涉及多个β核素几乎无需考虑的环节,例如:对于偶联反应特异度更高,辐射剂量采集难度更大,因此对同时具备核医学深度认知与药物研发全链条能力的CRO需求激增。
3)产业链提前布局:一些CDMO或核素生产企业开始建设专门的α核素生产和标记平台,就是因为看到了未来的管线增长潜力。
但从整体市场规模来看,α核药的商业化仍处于爆发前夜,真正的大规模外包需求预计要到临床后期或临近商业化阶段才会明显放大。
02
锕-225核药成为研发重点
目前在研的α核药管线主要集中在锕-225,范恩柯尔CEO习宁博士告诉动脉网。锕-225与镥-177的半衰期接近,离子半径接近,络合过程接近,在人体内的分布情况也比较接近。锕-225与镥-177在四个核心维度上的相似性,成为核药领域实现从“β时代”向“α时代”跨越的桥梁。这四大相似性为锕-225核药的研发带来了从实验室到临床、从技术到商业化的全面便利。
1)半衰期接近:简化临床方案与物流体系
镥-177的半衰期为6.7天,锕-225为10天,两者半衰期接近,这在临床转化中至关重要。
在核药研发中,载体的生物半衰期必须与核素的物理半衰期相匹配。由于镥-177已成功验证了大量靶向分子的体内动力学行为是可行的,当换成锕-225时,这些旧载体依然能与新核素完美配合,无需重新在海量化合物中大海捞针。
此外,医院针对镥-177类药物(如诺华的Pluvicto)已经建立了成熟的“预约-给药-住院观察-出院的标准化流程”。锕-225的半衰期与其接近,意味着医院无需对现有核医学病房管理体系进行大幅改造。患者住院周期、医护人员辐射防护规范都可以大量借鉴现有经验。
2)离子半径接近:螯合化学的“即插即用”
镥-177和锕-225的离子半径非常接近,三价离子的离子半径均在100皮米量级。
核药开发中关键的一步是找到一个能牢牢抓住金属离子、不让其在体内泄露的“笼子”(螯合剂)。经典的DOTA螯合剂对Lu³⁺有极强的亲和力。由于Ac³⁺的尺寸与Lu³⁺接近,DOTA同样能高效地螯合Ac³⁺。这意味着,基于DOTA螯合镥-177的经验(包括标记温度、pH值、反应时间、质量控制方法)可以直接平移到锕-225上,极大地降低了化学开发的难度。
3)络合过程接近:保证体内稳定性
¹⁷⁷Lu-DOTA复合物在体内的稳定性已经被临床治疗所证实,脱靶风险低。基于络合过程的相似性,我们可以合理推断,²²⁵Ac-DOTA也具有类似的稳定性。这为新药的安全性论证提供了强有力的背书。
而且检测核药是否稳定的方法也是通用的。研发人员可以沿用为镥-177建立的那一套质控标准来评估锕-225药物,这大大加速了临床前研究的进程。
4)体内分布情况接近:利用影像学数据实现“精准桥接”
这是四个相似性中最具战略价值的一点。镥-177不仅是治疗核素,它还能释放γ射线,因此可以进行显像,能够比较方便地观察药物在体内的分布、代谢情况。而锕-225几乎无法显像。
虽然无法直接看到锕-225去了哪里,但由于连接的是同一个靶向分子,医生可以使用镥-177的影像来指导锕-225的治疗。镥-177的影像成了锕-225的“眼睛”。
锕-225与镥-177的这四大相似性,构成了完善的技术平移路径。
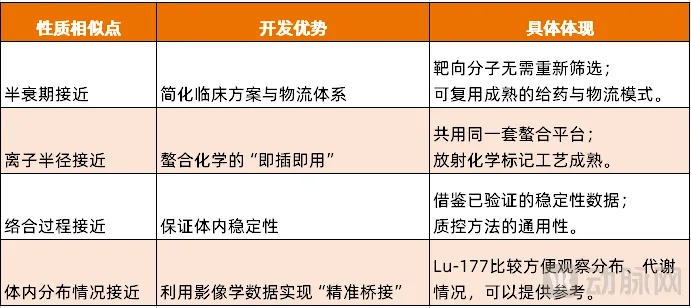
图2. 锕-225与镥-177的性质接近并形成了开发优势(资料来源:动脉网整理)
除了锕-225,另一类α核药铅-212也在开发中。铅-212在供应稳定性和成本上占明显优势。而且铅-212的观测比锕-225更容易,这是由于铅-212衰变过程中释放的γ射线可用于SPECT成像,从而实现“所见即所治”。
铅-212与锕-225核心的差异点在于半衰期,铅-212的半衰期仅有10.6小时,而锕-225的半衰期长达10天。铅-212的半衰期短,意味着辐射作用快、可能更安全。但铅-212的短半衰期同时意味着其与靶分子在体内的循环时间不匹配,在镥-177上积累的开发经验也很难被应用在铅-212类核药的开发中。
此外,由于铅-212的半衰期短,因而其生产不能采用类似锕-225与镥-177的集中式生产方式,铅-212类核药需要在靠近医院的设施中生产并提供给患者使用。
锕-225半衰期长,能够释放更多的能量;铅-212具有更好的安全性,供应更充足。这两种核素成为α核药当前的主流研发方向。
03
诺华的α核药有望率先冲刺上市
目前核药企业在α核药领域的研发集中在锕-225和铅-212两个主要方向上,在研管线也在快速推进。据动脉网统计,截至2026年3月4日,全球进入临床Ⅰ期之后的处于活跃状态的锕-225核药管线有28条,铅-212管线有11条。
其中锕-225核药的管线数量更多,临床推进速度更快,²²⁵Ac-PSMA-617和RYZ101两款产品已经推进到临床Ⅲ期阶段,即将冲刺上市。
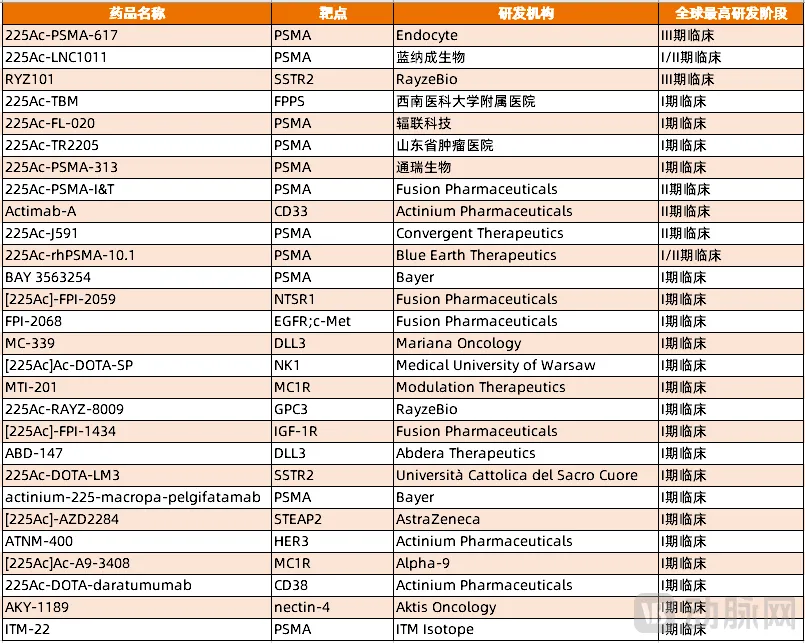
图3. 进入临床Ⅰ期阶段之后的锕-225核药管线(资料来源:医药魔方)
诺华的²²⁵Ac-PSMA-617(AAA817)注射液是目前关注最高的锕-225核药产品。与诺华的重磅药物Pluvicto相比,AAA817用放射性核素锕-225替换了镥-177,然后与PSMA-617连接在一起。
AAA817作为诺华的下一代RDC产品,其使用的锕-225核素发射的α粒子具备高能量、短射程的独特优势,能够诱导更严重的癌细胞DNA损伤,同时减轻了对健康组织和疾病周围组织的脱靶毒性。AAA817能够精准杀伤肿瘤细胞、最大程度减少对正常组织的损伤,与发射β粒子的¹⁷⁷Lu-PSMA-617相比,其治疗潜力更为强大。
此前,一项对标准疗法(包括新一代抗雄激素疗法和基于类固醇的化疗)产生抗药性的 mCRPC患者采用AAA817治疗的临床试验中,AAA817表现出对治疗晚期mCRPC患者较好的效果。这些符合条件的患者接受AAA817治疗,剂量为100-150 kBq/kg。最初入组的63例患者中,共有56例完成了至少两个疗程的AAA817治疗,并被纳入本研究。
结果显示,91%的患者PSA水平有所下降,其中67.8%的患者PSA下降幅度达到50%或以上。PSA(前列腺特异性抗原)是一种由前列腺细胞产生的蛋白质,通常用于检测和监测前列腺癌。PSA值的大幅下降通常表明对肿瘤负荷的有效控制。在另一项针对诺华¹⁷⁷Lu-PSMA-617的Ⅲ期临床研究中,57.6%的患者PSA下降幅度达到或超过50%。AAA817实现了更大比例的患者PSA下降。
疲劳是AAA817治疗中最常见的治疗突发不良反应之一,70%的患者会出现1/2级疲劳,3.5%的患者会出现3级或以上疲劳。这种疲劳是一过性的,在下一个治疗周期之前就会缓解。此外,约三分之一的患者出现口腔干燥症(1/2 级:32.1%)。
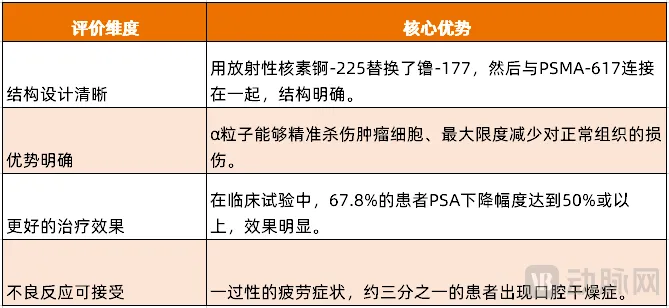
图4. AAA817的核心优势(资料来源:动脉网整理)
整体看来,AAA817靶向α疗法耐受性良好,不良反应可接受,对治疗晚期mCRPC患者有效。目前该产品正在进行Ⅲ期临床试验,并有望成为首款上市的α核药。
同样针对PSMA靶点,国内管线的进展紧随AAA817之后,并显示出优势:1)²²⁵Ac-LNC1011在早期的动物试验中显示出更好的治疗潜力,此外¹⁷⁷Lu-LNC1011的开发经验也将为蓝纳成生物的²²⁵Ac-LNC1011的开发提供经验;2)²²⁵Ac-PSMA-CY313获得同行高度认可。在去年10月份的欧洲核医学大会(EANM 2025)上,由通瑞生物支持的两项关于²²⁵Ac-PSMA-CY313在mCRPC领域的研究,凭借其创新性与重要价值,获大会评审委员会高度认可,被评选为 “Top Rated Oral Presentation”(最受欢迎的口头报告);3)辐联科技²²⁵Ac-FL-020注射液被FDA授予快速通道资格。
在PSMA靶点,国内管线紧跟诺华的AAA817,并形成了强劲的追赶态势。
锕-225核药另一款进入Ⅲ期临床的产品为RYZ101,一款靶向SSTR2的RDC药物。但是受到上游核素锕-225的供应问题,RYZ101的Ⅲ期临床试验进度受影响。
铅-212类核药是另一个备受关注的α疗法。此前不久,赛诺菲终止了AlphaMedix(²¹²Pb-DOTAMTATE)的开发,这是一款靶向SSTR的α核药。这给后续推进的铅-212类核药研发带来较大的压力。目前已进入临床Ⅰ期阶段之后的铅-212核药管线已达到11条。
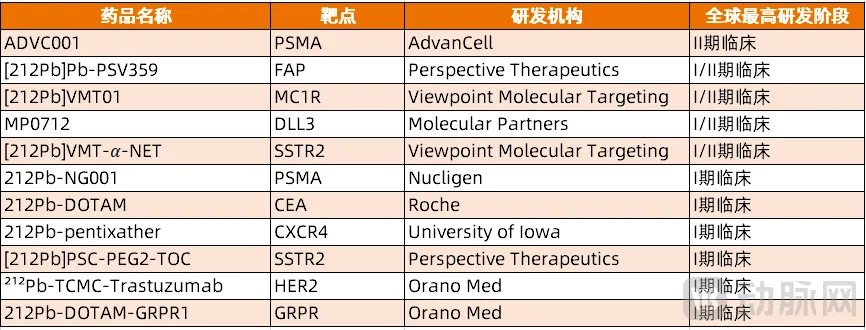
图5. 进入临床Ⅰ期阶段之后的铅-212核药管线(资料来源:医药魔方)
虽然铅-212的研发进展落后于锕-225,但资金仍在持续进入这一领域。核药公司Perspective Therapeutics在今年2月初通过股份发行筹集了约1.75亿美元,以加速其基于铅-212的技术平台和临床项目。其在研管线中VMT-α-NET与VMT01已经进入临床Ⅰ/Ⅱ期阶段,分别靶向MC1R和SSTR2。
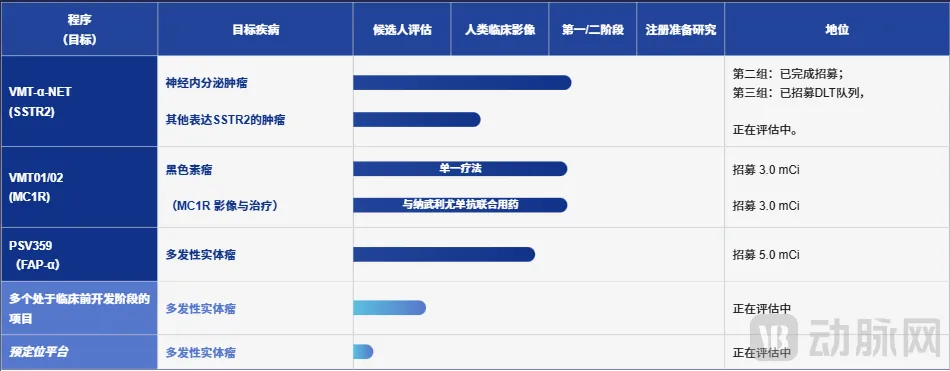
图6. Perspective的在研管线情况(资料来源:公司官网)
铅-212具有半衰期短,供应更充足的特点,这使得此类核药展现了较大的开发潜力。
04
α核药与β核药的结合
虽然α核药当前发展势头强劲,但并不代表着α核药以后要取代β核药,事实上,二者应是互为补充、协同发展的关系。范恩柯尔CEO习宁博士如此阐述这两类药物的关系。
一方面来看,β核药仍是当前核药的基石,凭借成熟的供应链和更为确切的临床数据,β核药将继续在多种肿瘤的治疗中发挥核心作用。而α核药则以其精准性和更强的打击能力有望在微转移灶清除方面展现优势。从另一方面来看,对于某些经β核药治疗后发生转移的肿瘤患者,α核药有望进一步发挥更大的临床价值。
当前α核药的研发还处于早期阶段,还需要积累更多的临床数据。随着研究的进一步深入,α核药有望发挥更大的临床价值。

 产业资讯
产业资讯
 深蓝观
深蓝观  2026-03-26
2026-03-26
 4
4

 产业资讯
产业资讯
 动脉网
动脉网  2026-03-26
2026-03-26
 5
5

 产业资讯
产业资讯
 生物药大时代
生物药大时代  2026-03-26
2026-03-26
 5
5