 产业资讯
产业资讯
 阿基米德Biothech
阿基米德Biothech  2026-05-07
2026-05-07
 53
53
CAR-T的好日子来了。
全球头部CAR-T公司同步进入估值修复周期。自体CAR-T 2025年销售额59亿美元,同比增长30%,最关键的是,制造简化、成本便宜的下一代CAR-T,即将重新定义肿瘤治疗格局,受到资本和MNC的争抢。Allogene 4月13日公布通用型CAR-T疗法MRD转阴率,股价盘中涨超60%;礼来4月20日以70亿美元收购Kelonia,刷新in vivo CAR-T领域收购金额纪录。
Allogene一点就燃,说明通用型CAR-T血仍未冷,依然受到MNC和欧美投资人的关注,只是这个赛道经历的技术验证期较长,筛选剩下的强者寥寥无几,但只要出现催化剂,立刻爆燃全场。
in vivo CAR-T开始变得拥挤。据Insight,目前全球在研的体内CAR-T管线有182条,其中有50%来自中国。in vivo CAR-T也将面临技术验证期的压力,安全性、持久性,可重复输注等问题待解。
下一代CAR-T剩者为王。科济药业拥有12年底层技术功底,敢于攻克行业内核心技术难题,已成为通用型CAR-T的领跑者,一枝独秀输出过硬的临床数据,CT0596、CT1190B随访数据更新将亮相EHA 2026年会,全球瞩目。当前in vivo CAR-T热度虽高,但敢于上实体瘤项目的还极为稀缺,CARvivo™是科济药业自研的慢病毒载体in vivo CAR-T平台,转导效率10倍于同行且特异性高,有望填补实体瘤空白。
通用型+in vivo,科济药业手握全球唯一横跨下一代CAR-T两大赛道的核心资产。
01
两种技术路线的博弈
有一种博弈不是你死我活,而是殊途同归。
无论通用型还是in vivo,其实都是现货型CAR-T技术路线,以更简单的生产和使用过程、更低的成本,破解自体CAR-T的可及性困局。
两种技术路线互补共存,各有优劣,会在不同的适应症和临床情景下有不同的应用。
异体通用型CAR-T技术门槛更高,需要挑战的创新性环节更多,经过大浪淘沙,仅剩下少数玩家,所以显得略冷清,而in vivo CAR-T尚处早期概念阶段,掀起一场资本狂欢。据Insight数据库,2024年in vivo CAR-T领域交易数量仅有3起,2025年飙升至12起,披露交易总金额49.5亿美元,2026年以来交易总额高达94亿美元。CAR-T老玩家诺华、吉利德、BMS、强生,后来者艾伯维、阿斯利康、礼来,争相押注in vivo CAR-T。
但是,异体通用型CAR-T每一步进展,仍牵引万千目光。这是因为通用型CAR-T是接近成熟的产品形态,科济药业、Allogene、Wugen已取得瞩目的临床疗效数据,并有大规模多中心数据证实零GvHD。
如前所述,Allogene公布其通用型CAR-T产品cema-cel的ALPHA3试验首批数据,在一线化疗后仍存在微小残留病灶(MRD)的大B细胞淋巴瘤患者中,治疗第45天cema-cel组MRD转阴率达58.3%,对照组仅16.7%,绝对差异41.6个百分点,显著超过文献公认25%-30%的临床有意义阈值。安全性方面,未出现任何级别的CRS、ICANS或GvHD,12例患者中10例在门诊完成输注。这些数据进一步夯实通用型CAR-T的安全有效性证据链。
虽然Allogene股价在增发利空下冲高回落,但今年以来累计上涨约60%。
在成本方面,据南京康和细胞基因工程研究院,由于采用健康供者细胞,“一批供百人”的规模化生产模式,国内异体通用型CAR-T的生产成本可控制在万元以下。in vivo CAR-T理论上可省去体外细胞工程化改造步骤,大幅缩短制备周期、降低成本,但这一优势建立在“载体精准递送、体内高效编辑”的技术前提之上。目前LNP和病毒载体的生产效率、靶向特异性、以及规模化生产质量控制仍面临挑战,成本优势尚未在真实世界中得到验证。
in vivo CAR-T的技术路径里也分出两条路。
in vivo CAR-T的技术路线差异主要在于载体,其决定装载物大小和类型,其中慢病毒和LNP是最常用的技术路线。
慢病毒载体产品治疗血液瘤的短期疗效确切,与自体CAR-T相当,需关注给药后长期疗效持续性和安全性;LNP载体产品需多次给药但安全性表现出色,在自免疾病中已观察到初步疗效信号,未来在自免领域可能会有不俗表现。
宇宙大药企礼来有钱任性,2个月内通过2起(24亿美元+70亿美元)大额收购交易全面布局in vivo CAR-T两大主流技术路线。
02
in vivo CAR-T进入淘汰赛
礼来对Kelonia的收购,可能标志着资本狂欢到达巅峰,in vivo CAR-T将从早期概念进入技术验证阶段。
in vivo CAR-T无需体外改造T细胞和清淋,是接近完美的现货型细胞疗法,但长期安全性未知,有效性、持久性仍需长期随访和大样本验证。
in vivo CAR-T将慢病毒载体或LNP直接注入人体,存在载体免疫原性、CAR基因整合至非目标细胞(肝细胞、生殖细胞)的潜在危害,以及载体诱导的插入突变风险。被礼来收购的Kelonia核心技术是体内基因定位系统(iGPS),核心管线KLN-1010(BCMA in vivo CAR-T)采用的是一种改良的第三代慢病毒载体,ASH 2025披露的I期临床数据显示,在接受治疗的4例R/R MM患者中,ORR和MRD阴性率均达100%,同时无ICANS和3级或以上CRS发生,但考虑到其潜在的脱靶基因整合可能,需要关注给药后长期疗效和安全性。
阿斯利康此前以10亿美元收购的EsoBiotec的ESO-T01也是靶向BCMA的in vivo CAR-T。Nature Medicine今年3月发表ESO-T01在华中科技大学同济医学院附属同济医院进行的治疗复发或难治性多发性骨髓瘤(r/r MM)一期临床试验数据,在中位随访6个月时,ORR=80%,CR=60%,与自体CAR-T具备疗效可比性,传奇生物Carvykti在中位随访8.8个月时,ORR达95%,CR率为56%,≥3 级CRS 发生率为4%。
但ESO-T01安全性风险触目惊心。
5例患者中4例发生CRS,其中3例为3级重度的CRS,研究中还观察到两名患者在30天内出现2级单纯疱疹病毒和一名患者在输注后6个月出现肺部感染。更严重的是,有1例患者发生ICANS,并最终因髓外病灶进展导致脊髓压迫死亡。
去年7月,华中科技大学同济医学院附属协和医院血液科团队在《柳叶刀》上报告ESO-T01治疗r/r MM的ORR达到100%,但接受治疗的4例患者均出现CRS,有3例都出现3级CRS。3例患者出现了低血压且需要使用升压药的情况,2例患者需要补氧,≥G3血液毒性均有发生。
LNP技术路线in vivo CAR-T的持久性,在自体CAR-T“一针治愈”神话前则可能不堪一击。
虹信生物基于LNP载体的HN2301(CD19 In vivo CAR-T),在治疗5例SLE患者的IIT临床试验中,每名患者接受1-3次给药(第0/2/4天给药),CAR-T细胞在给药后6小时达峰,持续时间仅维持2-3天,显著短于慢病毒载体in vivo CAR-T。据兴业证券统计,在SLEDAI-2000评分方面,自体CAR-T、通用型CAR-T与三抗TCE均实现评分的清零,其中自体CAR-与通用型CAR-T均实现ds-DNA的大幅下降与免疫调节和免疫抑制药物的停药。In vivo CAR-T (HN2301)目前读出的数据在1 月的随访期时,多名ds-DNA发生了反弹,且未实现SLEDAI-2000评分的清零和免疫药物停药。
今年预计将有多款in vivo CAR-T管线首次披露临床数据,必然有惊有喜,残酷的淘汰赛开始了。
欲戴王冠,先承其重,剩下的都是强者。
03
通用型CAR-T一枝独秀
科济药业是通用型CAR-T赛道剩下的强者。
通往胜利之路同时铺满了鲜花与荆棘。与in vivo CAR-T一样,通用型CAR-T早前也是一片欢呼声,有明星公司临床数据高开惊艳,但随即遭遇重大挫折。
科济药业自主研发的THANK-u Plus®平台,有效解决了通用型CAR-T的最大挑战——宿主抗移植物反应(HvGR)引起的疗效持久性问题,目前持续读出的通用型CAR-T临床数据在全球肿瘤领域处于领先水平,表现亮眼,一枝独秀。科济药业两款通用型管线CT0596(靶向BCMA)、CT1190B(靶向CD19/CD20)的临床疗效和体内扩增,显著优于海外通用型CAR-T,可媲美自体CAR-T。
CT0596在ASH 2025发表的首次人体研究中,展现出良好的安全性及令人鼓舞的疗效信号。截至2025年8月31日,8例接受CT0596输注的R/R MM患者均为可评估疗效人群,中位随访时间为4.14个月。6例患者达到部分缓解(PR)及以上疗效:3例达到完全缓解/严格意义的完全缓解(CR/sCR)(均属于全剂量清淋的患者),1例达到非常好的部分缓解(VGPR),2例达到PR。PT01截至第8 个月仍持续达到sCR且MRD阴性。4例患者出现1级细胞因子释放综合征(CRS),无2级及以上CRS发生。未观察到免疫效应细胞相关神经毒性综合征(ICANS)或GvHD。未观察到剂量限制性毒性、治疗中断或死亡事件。
CT1190B扩增水平惊艳。CAR-T细胞在体内的扩增水平是决定疗效持久性的关键因素,据去年11月披露的数据,在推荐剂量下(足量清淋、细胞剂量达到66×10⁸),共6例患者CT1190B的扩增水平,远超目前全球上市的自体CAR-T产品和在研的通用型CAR-T产品。
CT0596、CT1190B将在EHA 2026年会上进行数据更新,有望带动全球通用型CAR-T迈出历史性的一步。
04
填补in vivo CAR-T实体瘤空白
科济药业在通用型CAR-T一枝独秀的能力,也将复制到in vivo CAR-T。
实体瘤是细胞治疗的珠穆朗玛峰,当前in vivo CAR-T管线集中于血液瘤和自免疾病,对实体瘤从0到1的开荒使命,还有待破局者。CREATE Medicines基于mRNA-LNP的MT-302(TROP2 in vivo CAR-T)已读出I期18例晚期实体瘤患者临床响应数据,仅观察到1例确认的部分缓解(cPR),并且接受了20次给药,堪称灾难级别。
攻克实体瘤,可能希望在于慢病毒载体路线。
慢病毒载体路线主要优势在于装载能力强,转导效率较高,能够整合基因无需重复给药。与对照病毒载体相比,科济药业自研CARvivo™病毒载体的T细胞转导效率提升10倍,并实现更强劲的CAR-T细胞扩增能力,有底气拿下实体瘤。
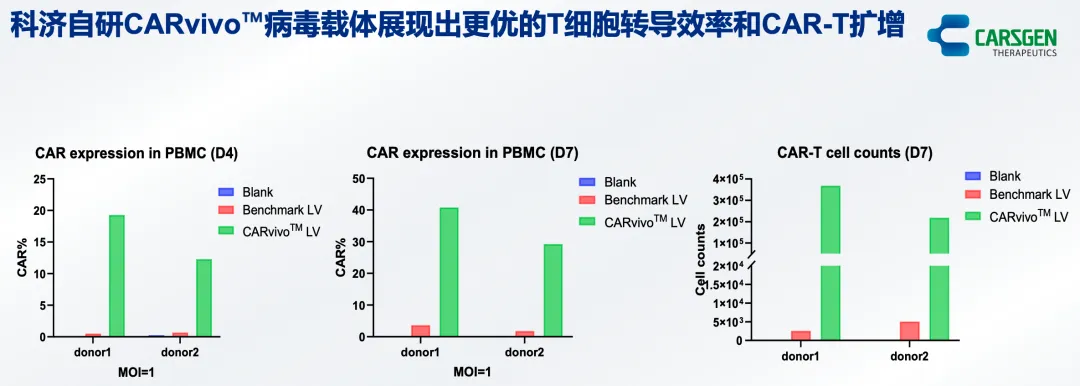
对于in vivo
CAR-T,转导效率是决定临床成功的关键,尤其是在高侵袭性疾病的治疗中。为解决这一问题,科济药业开发出一种具有更强融合能力的专有融合蛋白。这一设计即使在较低的感染复数(MOI)下也能实现显著更高的转导效率,同时保持高度的细胞类型特异性。
CARvivo™平台还整合科济专有的T细胞特异性启动子CARpro。该启动子将CAR的表达限制在T细胞内,从而最大程度降低肿瘤细胞中发生脱靶转导的风险,并减少抗原掩蔽或治疗耐药的可能性。
科济药业是实体瘤领域的老玩家,有着深厚的Know-how积淀,靶向CLDN18.2的舒瑞基奥仑赛注射液(CT041)是全球首款进入NDA阶段的实体瘤CAR-T,有望今年获批上市。基于对于实体瘤靶点的深刻认知,已筛选出多个具备BIC潜质适合装载CAR-T的肿瘤抗原抗体,包括CLDN18.2、GPC3等。
科济药业CAR-T技术平台延展性强,追求的是在现有基础上实现重大突破,而不是只局限于某一条路线。我们可以畅想,未来科济药业的通用型和in vivo CAR-T将广泛覆盖血液瘤、实体瘤、自免疾病和抗衰老领域。
两大关键催化事件将至,一是EHA 2026年会上异体通用型CAR-T的数据读出,二是in vivo CAR-T KJ-C2529(靶向CD19/CD20)临床试验启动。
结语
CAR-T已经成为血液瘤疗效天花板和“一针治愈”的代名词,试想把这种神力扩大到实体瘤和自免疾病,将有多么震撼。
下一代CAR-T的景气度正快速上升,随着成本下降和治疗领域拓宽,将释放巨大的增量市场。
下一代CAR-T标的稀缺性显著提升,目前,全球临床进度第一梯队的4家海外in vivo CAR-T企业,除Umoja外已悉数被MNC 收购。
科济药业是同时深度布局异体通用型和in vivo CAR-T的全球最稀缺标的,并且凭借扎实的临床数据与深厚的技术壁垒,有望同时在两个前沿赛道向难度最高的实体瘤领域发起攻坚。
 产业资讯
产业资讯
 摩熵医药
摩熵医药  2026-05-07
2026-05-07
 68
68

 产业资讯
产业资讯
 生物药大时代
生物药大时代  2026-05-07
2026-05-07
 97
97

 产业资讯
产业资讯
 药渡
药渡  2026-05-07
2026-05-07
 81
81
 热门资讯
热门资讯