 产业资讯
产业资讯
 药智数据
药智数据  2026-05-12
2026-05-12
 5
5
01 全球新药2026年4月进展概述
1.1 进展到最新阶段的重点项目
4月全球共868个药物有相关更新动态,其中有402个项目推进到最新的阶段,其中在中国境内进行的项目共290个,境外项目有112个。
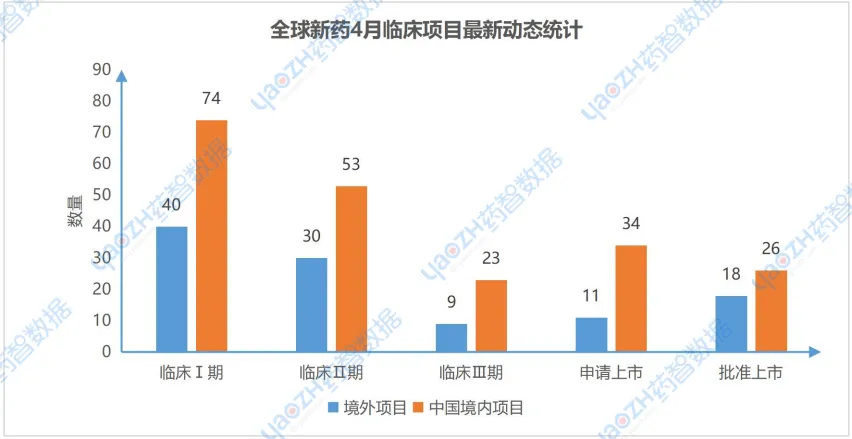
数据说明:最新阶段的临床阶段只统计该项目最高阶段数据,申请上市和批准上市数据包括项目的新适应症数据;临床1+2期统计为临床2期,临床2+3期统计为临床3期,即按较大临床期数统计。下方统计维度若无特殊说明,即保持一致。
1.2 研发前十靶点
4月全球有更新动态的868个项目中,涉及最多的靶点是GLP-1R,其次是CD3和PD-1。
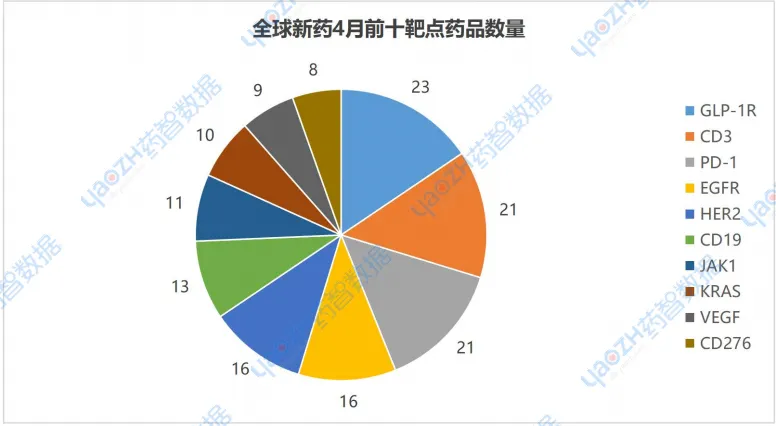
1.3 研发前十适应症
4月全球有更新动态的868个项目中,涉及最多的适应症是实体瘤,其次是非小细胞肺癌和肿瘤。
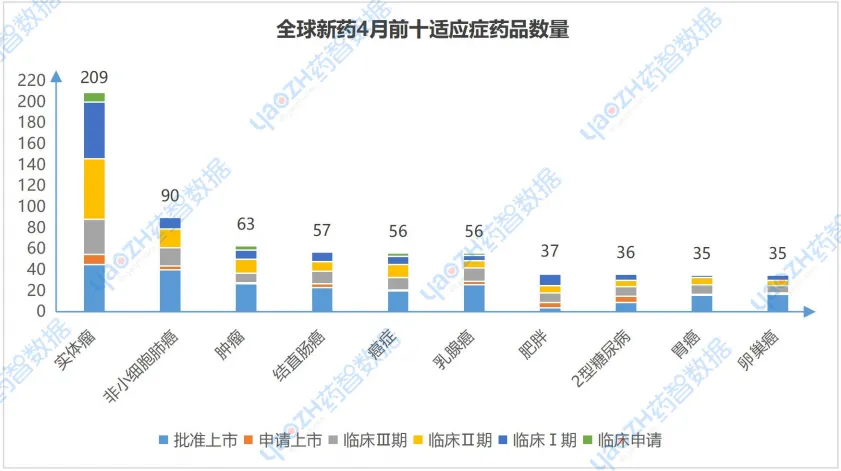
1.4 研发前十药品类别
4月有最新进展的402个药品中,药品类别占比前三的分别是化药53%,单克隆抗体10%,ADC疗法7%。
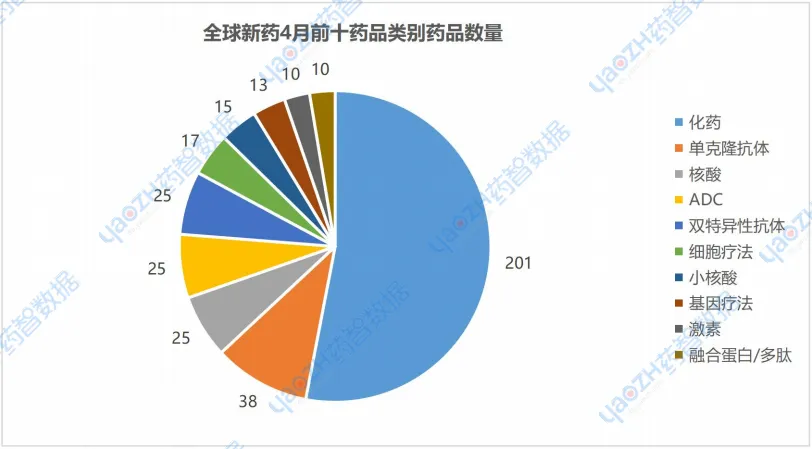
02 全球新药2026年4月重点项目
2.1 全球获批的新药
据全球药物分析系统数据库统计,4月全球共44款新药获批上市(包括新获批适应症),其中境外18个上市药品,中国境内26个药品(含一个药品多个地区上市),下表展示部分重点上市药物,文末附完整清单,更多药品信息可通过全球药物分析系统进行查看。
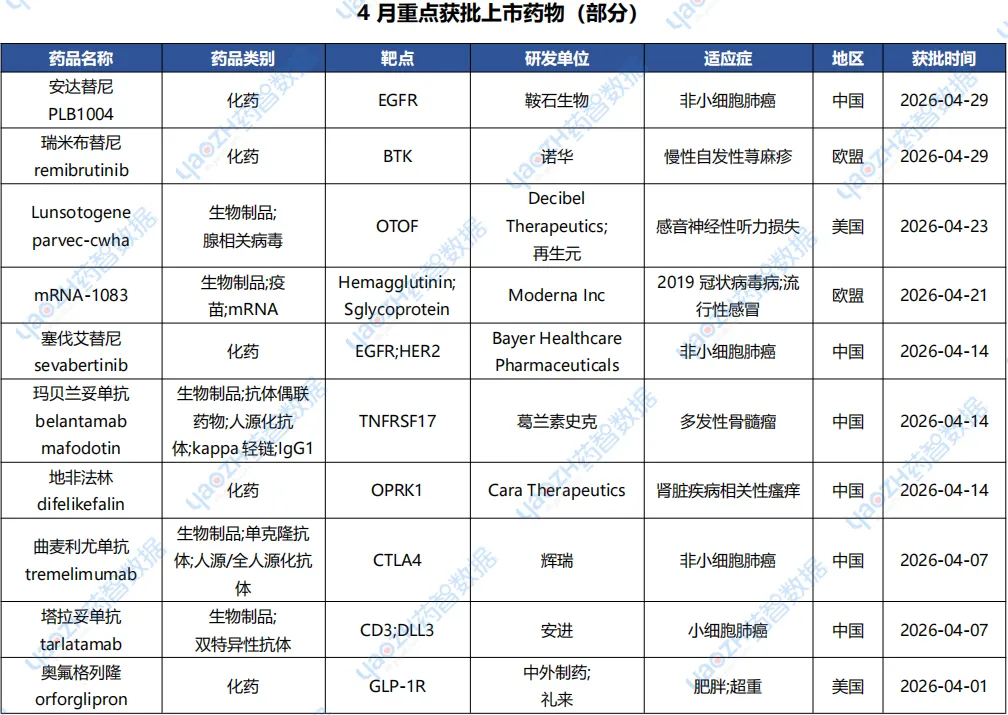
2.1.1 Lunsotogene parvec-cwha(Otarmeni)——全球首个遗传性听力损失基因疗法FDA获批上市
2026年4月23日,再生元宣布,美国食品药品监督管理局(FDA)已加速批准了Lunsotogene parvec-cwha(Otarmeni,DB-OTO)的上市,这是首个基于双腺相关病毒载体的基因疗法。Otarmeni适用于治疗由OTOF基因双等位基因变异引起的重度至极重度以及极重度感音神经性听力损失的儿童和成人患者。Otarmeni是首个获得FDA局长国家优先凭证计划(CNPV)批准的基因疗法,也是目前唯一一个用于治疗OTOF相关听力损失的体内基因疗法,在此之前,尚无针对OTOF相关耳聋的疾病改善疗法,再生元将在美国免费提供Otarmeni,患者仅需支付给药相关费用。
2.1.2 Orforglipron(奥氟格列隆)——全球首个口服小分子GLP-1药物获批上市
2026年4月1日,礼来宣布,美国FDA已批准其小分子口服GLP-1R激动剂奥氟格列隆(Orforglipron、Foundayo)在上市,用于治疗成人肥胖症或伴有体重相关疾病的超重症。这是目前全球唯一一种无需进食或饮水限制即可在一天任何时间服用的口服小分子GLP-1减肥药。除此之外,Orforglipron目前正被研究作为2型糖尿病、阻塞性睡眠呼吸暂停、骨关节炎膝关节疼痛、高血压、外周动脉疾病和压力性尿失禁的潜在治疗疗法。
2.2 全球申请上市的新药
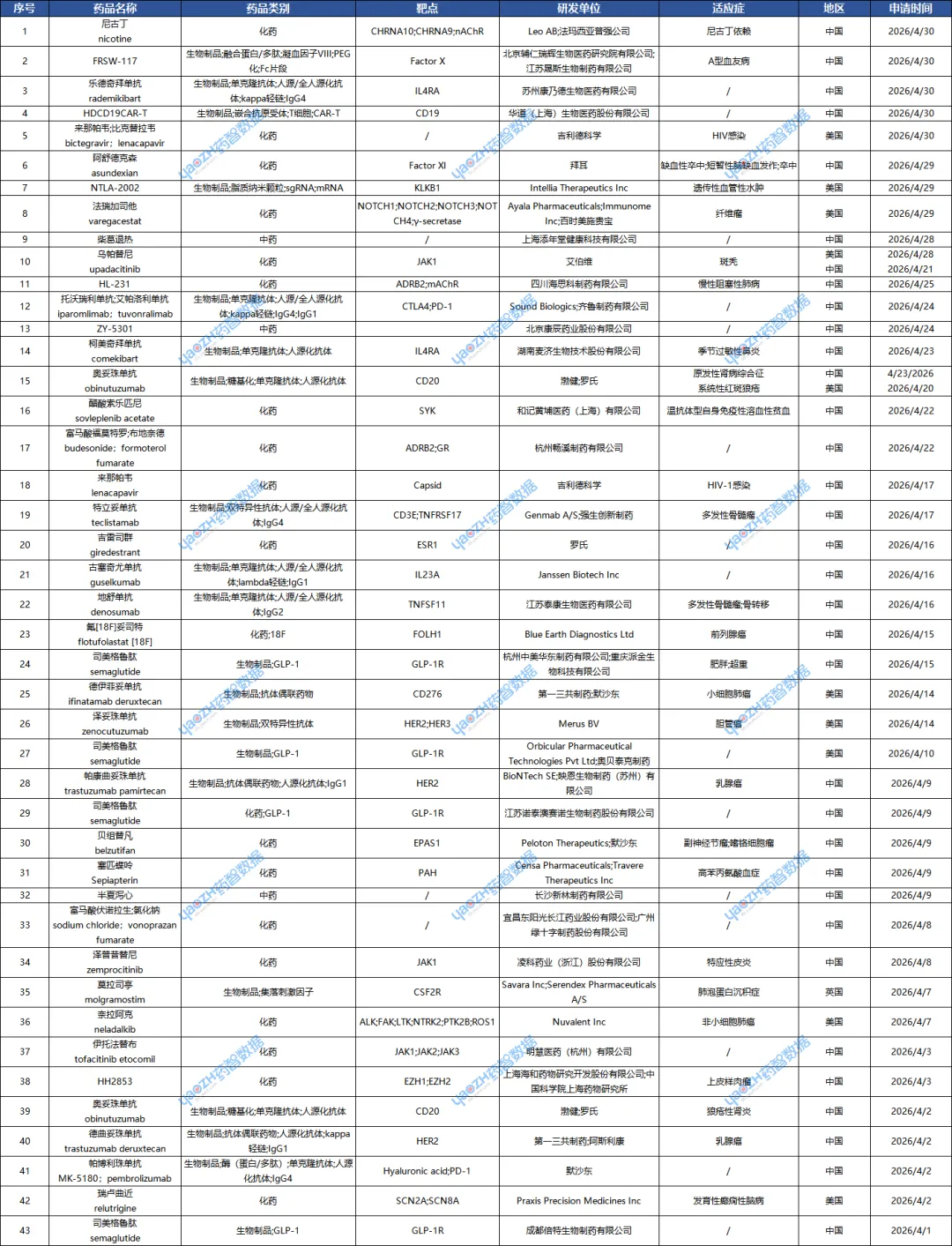
据全球药物分析系统数据库统计,4月全球共43款药物申请上市(包括首次申请、再次申请和一个药品多地区申请)下表展示部分重点申请上市药物,文末附完整清单,更多药品信息可通过全球药物分析系统进行查看。
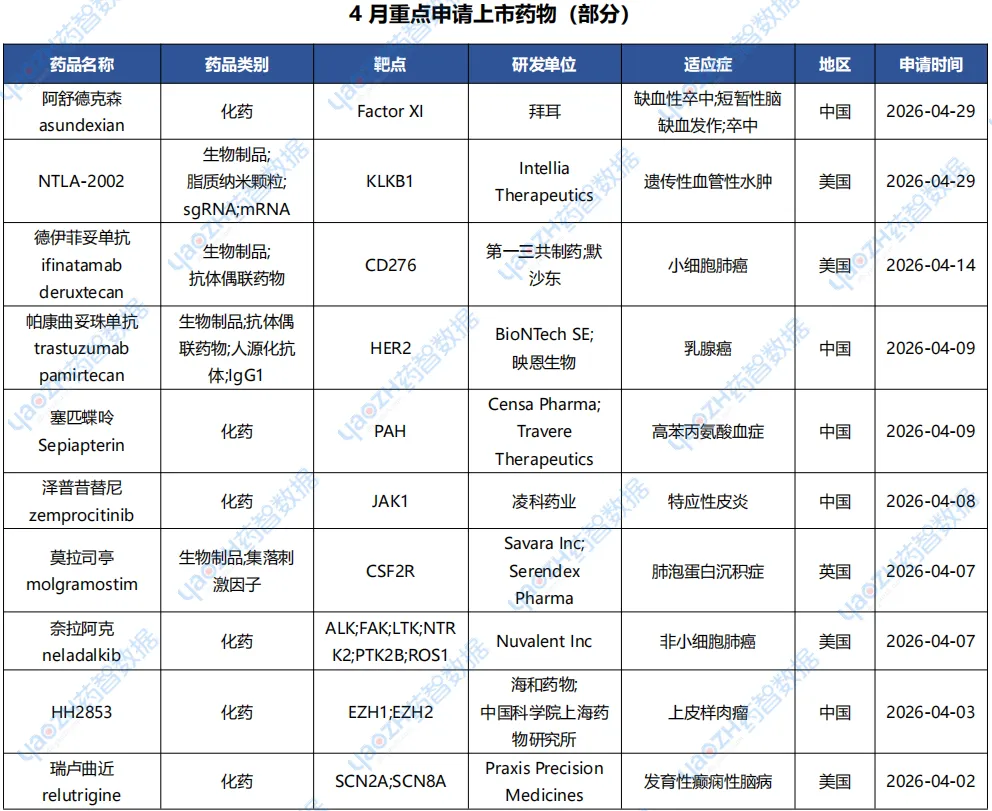
2.2.1 Asundexian——全球首个FXIa抑制药物申报上市
2026年4月29日,拜耳宣布,CDE已受理活化凝血因子XI(FXIa)抑制剂Asundexian(BAY 2433334片)用于降低缺血性卒中或短暂性脑缺血发作(TIA)成人患者的卒中(复发)风险,不包含心源性栓塞性卒中患者的上市申请。如果成功获批,Asundexian有望成为全球首个FXIa抑制剂药物,成为一种更安全、低出血风险的新型抗凝药,为心脑血管疾病及血栓高风险患者提供重要治疗选择,也会进一步巩固拜耳在抗血栓/抗凝药领域的地位。
2.3 全球重点临床试验的新药
据全球药物分析系统数据库统计,2026年4月首次进入临床三期的新药项目有32个,临床二期有83个、临床一期有114个,下表展示部分重点信息,完整信息可通过全球药物分析系统进行查看。
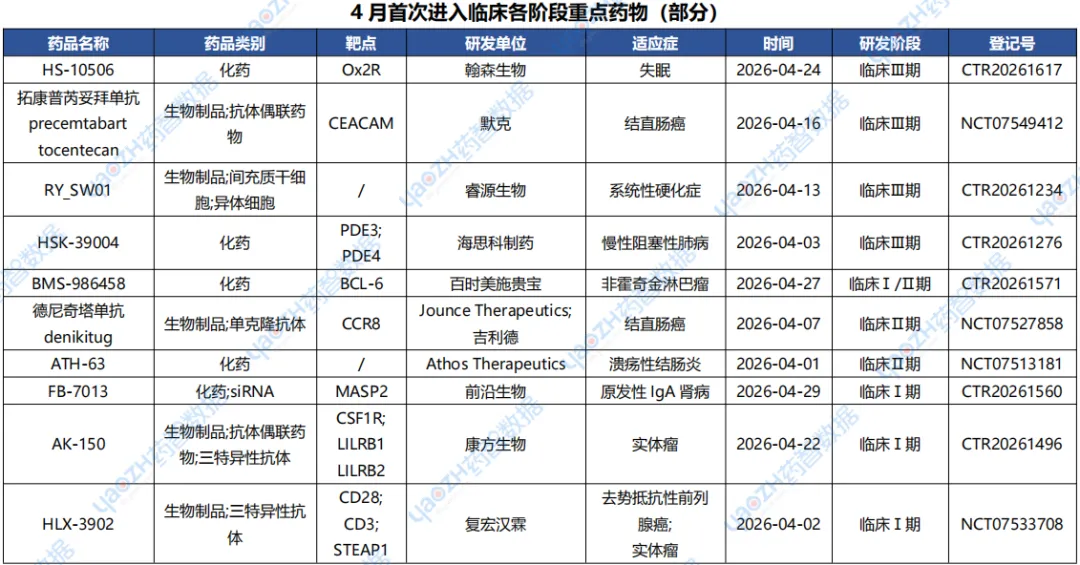
2.3.1 BMS-986458——国内首款进入临床Ⅰ/Ⅱ期的BCL6靶向药物
2026年4月27日,中国国家药品监督管理局药品审评中心(CDE)已批准百时美施贵宝自主研发的1类新药BMS-986458进入临床Ⅰ/Ⅱ期(登记号:CTR20261571),用于治疗复发/难治性非霍奇金淋巴瘤。BMS-986458作为一种潜在的首创药物,是全球进展最快的BCL6靶向药物。
据全球药物分析系统数据库统计,目前全球范围内有34款在研BCL6靶向药物,但尚未有药物能够获批进入市场应用。目前也仅有5款药物进入临床开发阶段,分别来自礼来、海思科、百时美、Treeline Biosciences、Arvinas。海思科医药的HSK-47977作为国产唯一一款BCL6药物,已获得FDA和CDE的药物临床试验批准通知书,目前正在进行非霍奇金淋巴瘤的Ⅰ期临床实验。
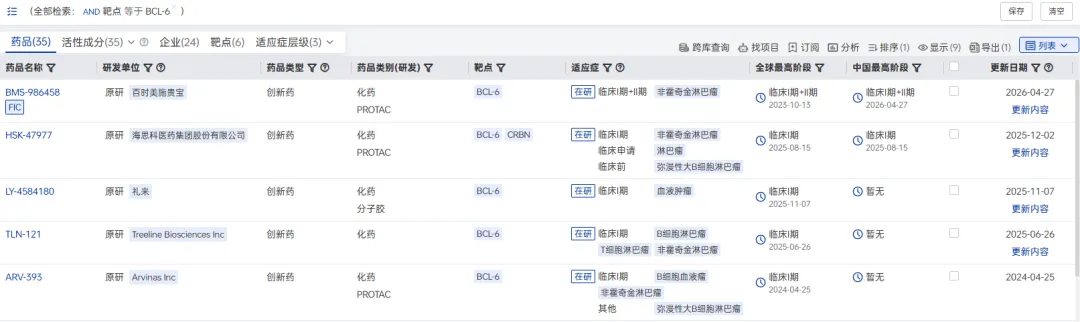
进入临床阶段的BCL6药物(图片来源:药智数据-全球药物分析系统)
03 月度医药交易、投融资及并购事件
据全球药物分析系统情报-交易数据库统计,2026年4月共113条医药交易事件,据市场投资格局统计,2026年4月有154条医药投融资事件和51项企业并购事件发生,重点交易信息如下,完整清单详见市场投资格局数据库。
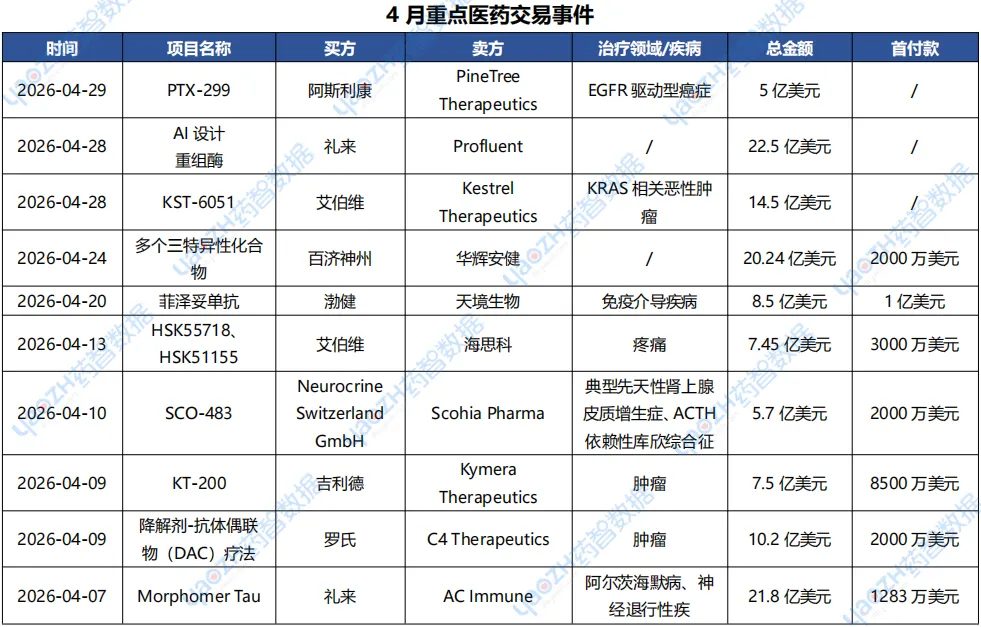
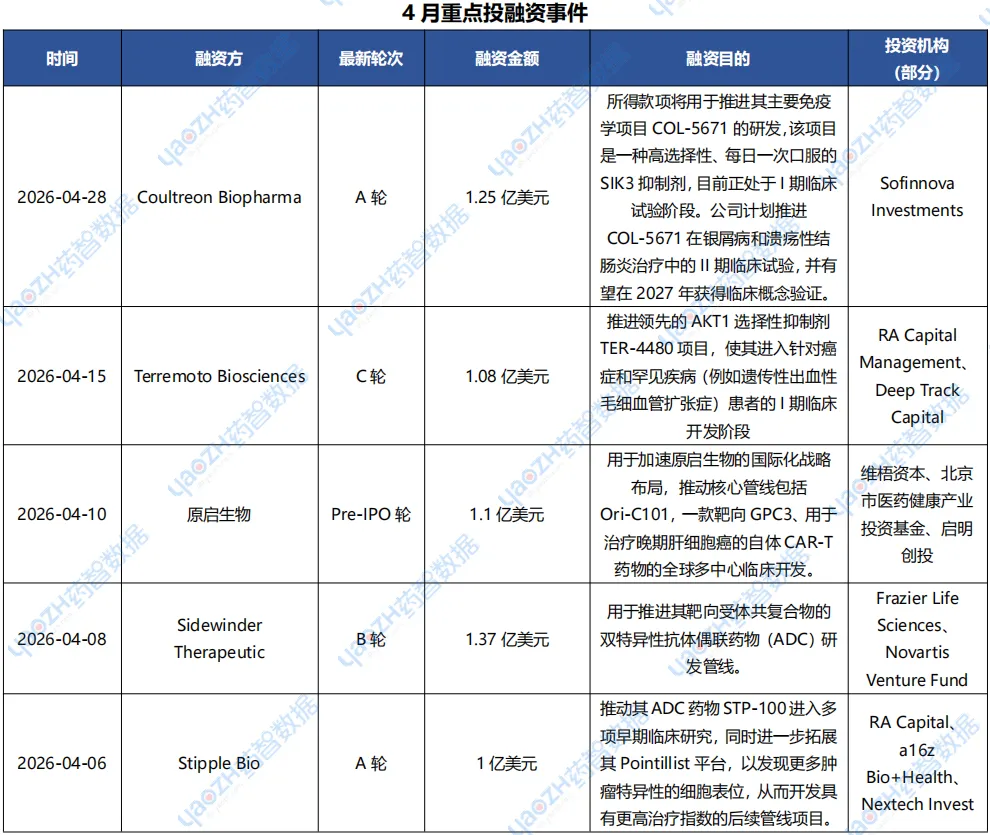
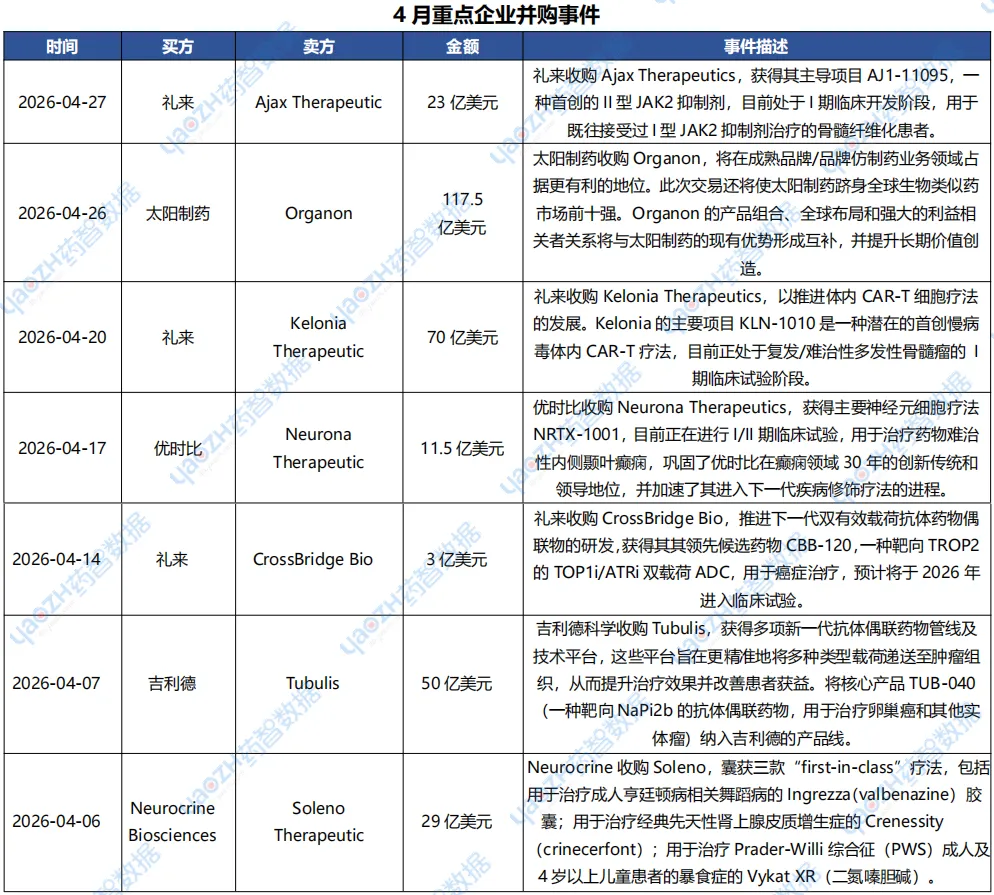
3.1 96亿美元!礼来加快收购步伐
2026年一季度,礼来替尔泊肽的两款核心王牌产品,Mounjaro和Zepbound的营收达到约130亿美元,依靠强大的GLP-1管线,礼来在本月连续收购三家生物技术公司,覆盖骨髓纤维化、免疫肿瘤(CAR-T)和ADC抗癌药物,显示其在罕见病、血液肿瘤与实体瘤领域的全方位布局。礼来在GLP-1的光环下,正在悄悄布局下一个高峰,用今天的利润,赌明天的增长,为五年、十年后的新引擎下注。
2026年4月27日,礼来以总额23亿美元的总金额收购Ajax Therapeutics公司,致力于开发下一代JAK抑制剂,主要候选药物AJ1-11095是一种在研的、每日一次口服的、首创的II型JAK2抑制剂,目前正在一项名为AJX-101的I期临床试验中进行评估,该试验针对的是既往接受过I型JAK2抑制剂治疗的骨髓纤维化患者。
2026年4月20日,礼来以总额70亿美元的总金额(包括32.5亿美元预付款,以及在达到特定临床、监管和商业里程碑后支付的后续款项)收购体内CAR-T疗法公司Kelonia Therapeutics。Kelonia的核心技术是iGPS®(体内基因定位系统)平台,利用特殊工程化慢病毒颗粒,可在体内高效且选择性地进入T细胞,使患者自身在体内生成CAR-T疗法,以治疗相关疾病。其核心管线KLN-1010,是一款靶向BCMA的体内CAR-T疗法,用于治疗复发/难治性多发性骨髓瘤,目前处于一期临床阶段。
2026年4月14日,礼来以总额3亿美元收购CrossBridge Bio公司,此次收购提供了一个创新的协同双载荷平台,用于开发差异化疗法,推进下一代双有效载荷抗体药物偶联物的研发其主要候选药物CBB-120是一种靶向TROP2的TOP1i/ATRi双有效载荷ADC,用于癌症治疗。
04 附表:4月获批/申报上市药物清单
附表1:4月获批上市药物清单
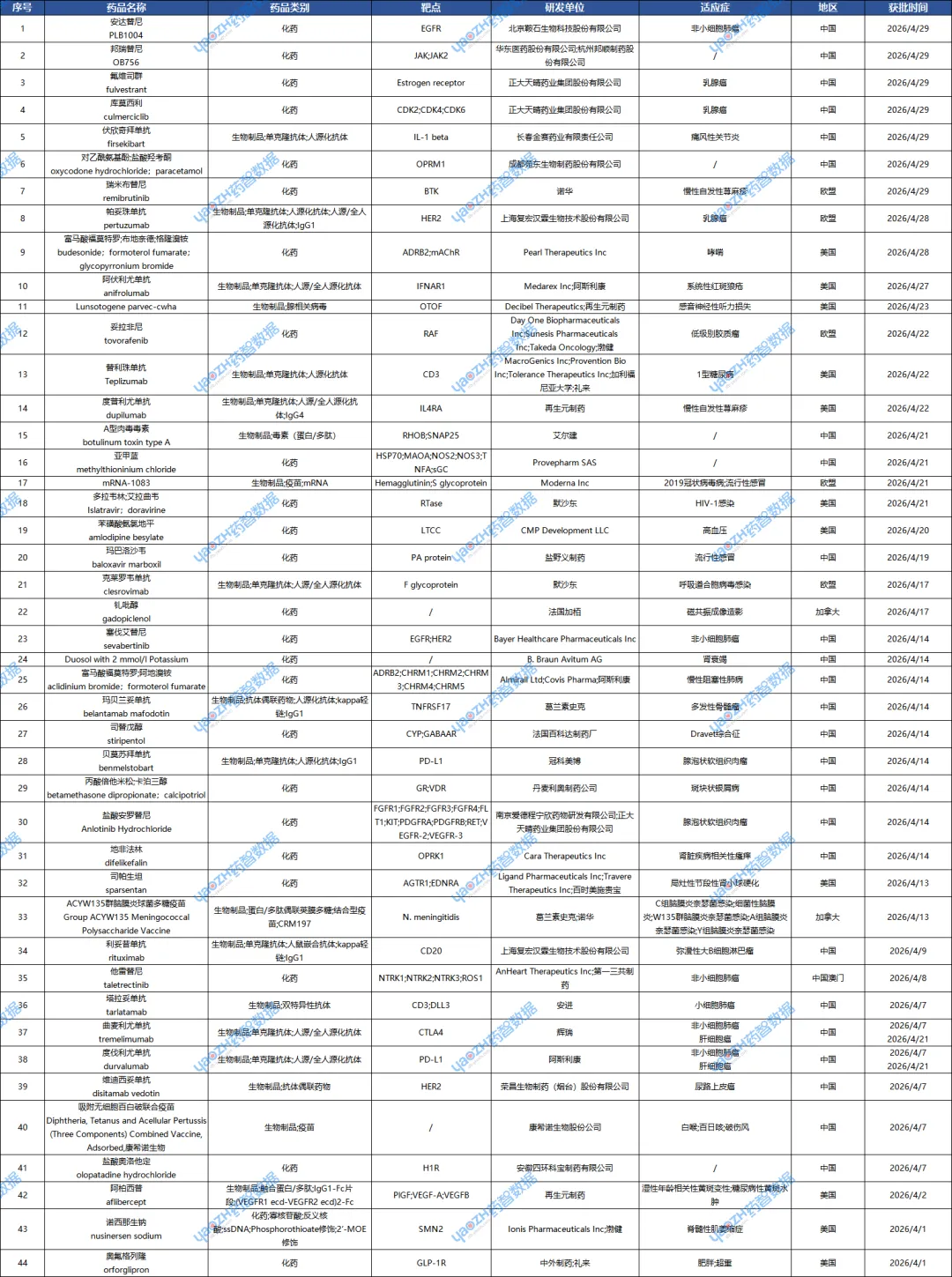
附表2:4月申请上市药物清单

 产业资讯
产业资讯
 赛柏蓝
赛柏蓝  2026-05-12
2026-05-12
 11
11

 产业资讯
产业资讯
 氨基观察
氨基观察  2026-05-12
2026-05-12
 3
3

 产业资讯
产业资讯
 Bio Journey
Bio Journey  2026-05-12
2026-05-12
 5
5
 热门资讯
热门资讯