 产业资讯
产业资讯
 医药魔方
医药魔方  2026-05-12
2026-05-12
 5
5
替尔泊肽的横空出世,将GLP-1/GIP双靶点药物推上了“神坛”。
仅仅4年,它便超越K药与司美格鲁肽,登顶全球“药王”,让整个GLP-1赛道的商业化价值冲到前所未有的高度。一时间,全球制药巨头蜂拥而至,红海竞争已成定局。
但这只是GLP-1下半场开启的序章,作为代谢药物,其背后连接的是肥胖、糖尿病、心血管风险、脂代谢异常,乃至更长期的慢病管理需求。也正因此,GLP-1赛道的竞争逻辑已不再停留在单一减重指标,而是转向代谢综合管理能力的更高维度较量。
在这场GLP-1竞争升级的浪潮中,一匹来自中国的“黑马”正式冲出重围。
5月5日,博瑞医药公布其GLP-1/GIP双重受体激动剂BGM0504减重III期临床顶线数据。它所展现出的,已经不只是替尔泊肽一个强力竞争者的姿态,而是独特的分子设计为基石,将减重、降压、调脂降尿酸、骨密度保护融为一体,以心血管代谢调节综合能力重新定义赛道标准的中国创新力量。
从减肥药到心血管代谢管理工具:
BGM0504重新定义GLP-1价值边界
如果只看减重数据,BGM0504的表现已经进入全球第一梯队。
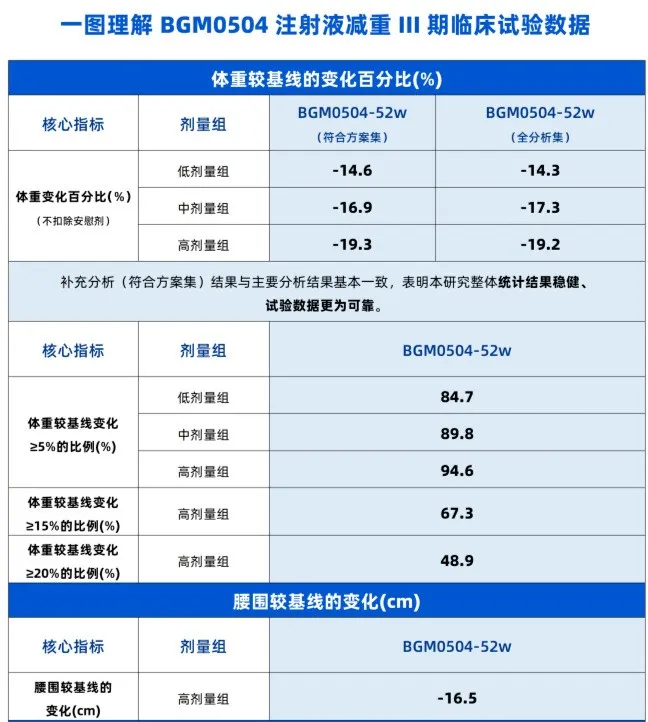
博瑞医药此次公布的III期研究显示,BGM0504在超重或肥胖受试者中,高剂量组减重幅度达到19.3%,腰围下降16.5cm。当前主流的GLP-1产品减重水平大致分布在15%–20%,其中双靶点产品普遍集中在18%–20%左右。放在整个GLP-1赛道来看,19.3%的减重结果已经是非常不错的成绩。
值得注意的是,其减重效果也兼具了广度与深度:体重降低≥5%的受试者比例最高达到94.6%,意味着绝大多数患者都能从中获益;而体重降低≥20%的受试者比例达到48.9%,接近一半受试者实现“深度减重”。
与此同时,BGM0504并没有完全依赖高剂量堆叠疗效,其5mg低剂量组依然实现了14.3%的减重幅度。这其实是一个容易被忽视的信号,但却意味着该药有机会进一步打开不追求极致减重的轻度肥胖及代谢异常人群这一庞大市场。
然而,在GLP-1赛道竞争日趋白热化、产品疗效逐步趋近的当下,减重数字本身已不再是最稀缺的能力。真正让行业聚焦的,是BGM0504区别于此前GLP-1药物的另一重特质——心血管代谢调节综合能力。
过去,血压在减重药研究中更多只是一个伴随观察指标。但本次研究中,BGM0504的降压表现可以说将其转化为了一项具有独立价值的关键疗效信号。数据显示,该药治疗36周,受试者血压达标率接近93%,收缩压下降22.9mmHg,舒张压下降约12.9mmHg。这一降压幅度已经达到甚至超过部分单药乃至双联降压方案的效果区间。
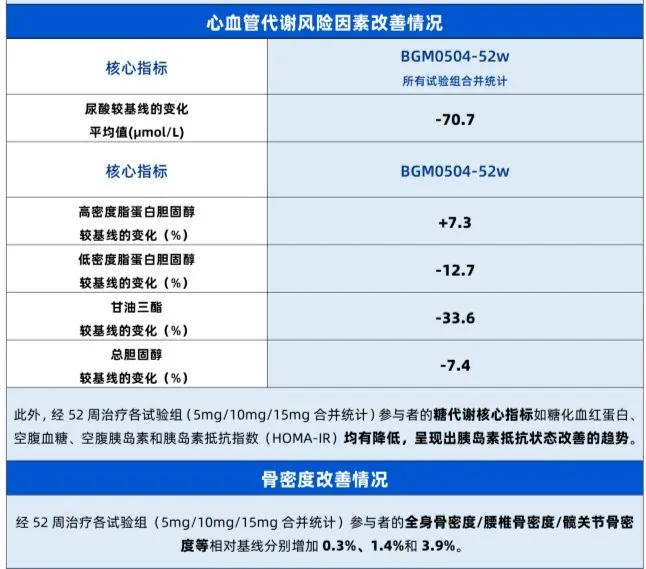
与此同时,BGM0504对血脂、尿酸和糖代谢等多项指标也展现出协同改善趋势,甚至在GLP-1药物长期备受关注的骨量流失问题上,BGM0504也给出了颇具差异化的结果,对于中老年肥胖患者而言,具有非常现实的临床价值。
此外,其整体安全性也表现稳定。高剂量组停药率仅0.7%,胃肠道不良反应多为轻度至中度,且多为一过性,可在短时间内自行缓解,没有出现明显影响依从性的安全问题。
事实上,当前全球GLP-1药物的研发方向正加速向更深维度的代谢管理延伸,包括替尔泊肽、司美格鲁肽在内的头部产品,均在心血管疾病管控上持续发力,不断拓展治疗边界。如果说GLP-1的上半场,是减重和降糖指标的比拼,那么当疗效逐步逼近平台期,下半场真正拉开差距的,可能是对整套代谢系统的重塑能力,以及由此带来的更多差异化获益。
而这,正是BGM0504能够跳出同质化竞争、脱颖而出的核心所在。
如何破局?解开BGM0504
全面获益的关键密码
想要真正理解BGM0504为何能实现全方位心血管代谢获益背后的深层次原因,最终还是要回到底层机制与分子设计本身。
长期以来,GLP-1始终是整个赛道的绝对主角。无论是早期的艾塞那肽、利拉鲁肽,还是后来的司美格鲁肽,GLP-1受体激动剂最初都围绕葡萄糖依赖性促胰岛素分泌这一机制开展降糖研究,随后逐渐发现,其还可通过延缓胃排空、中枢食欲抑制等机制带来显著的减重获益。
GIP虽然是最早被发现的肠促胰素之一,却曾长期处于相对边缘的位置。随着研究深入,GIP的价值才被重新认知。
已有研究表明,GIP可能深度参与脂质摄取、脂肪组织代谢重塑以及能量稳态调节,同时可能涉及炎症反应调控与胰岛素敏感性改善。也就是说,GIP并非是简单的“辅助角色”,其本身可能具有独立于GLP-1之外的代谢调控功能。
实际上,替尔泊肽就是一个典型案例,它对GIP受体的激活程度远高于GLP-1受体,其GIP受体的亲和力与天然GIP相当,而对GLP-1受体的亲和力比天然GLP-1弱约5倍。[1]这种偏向GIP受体的双靶点设计,也被认为是替尔泊肽能够显著超越传统GLP-1单靶药物的重要原因之一。
而BGM0504,则是在这一方向上的进一步加强。
根据发表于Nature子刊《Scientific Reports》的文章[2],博瑞医药研发团队通过分子动力学模拟发现,替尔泊肽原有K20位点的脂肪酸修饰,虽然有助于延长半衰期,但会破坏母肽K20残基与GLP-1R和GIPR外部结构域之间形成的关键“盐桥(salt bridge)”相互作用,从而削弱部分受体激动活性。
BGM0504的核心优化逻辑,就是把这个“损失”的活性重新拿回来。
博瑞医药研发团队选择保留K20位点游离氨基,同时将脂肪酸修饰从K20移动至肽链C端新增的K40位点,并延长linker结构,以解除对受体结合界面的空间位阻,在维持白蛋白结合亲和力和延长血浆半衰期的同时,最大化释放GLP-1R/GIPR激动活性,实现了激动活性与药代动力学特性的更优平衡。
体外实验数据验证了这一设计思路的有效性:BGM0504对GLP-1R/GIPR的激动活性,相比替尔泊肽提高约2-3倍。而在动物实验中,BGM0504对血糖、血脂、肝损伤、MASH纤维化等指标的改善,也更加突出。这也意味着,BGM0504具备进一步向心血管代谢疾病、MASH等更广泛适应症扩展的潜力。
从今天回看,BGM0504底层分子设计的优势,正在系统性转化为临床层面的差异化竞争力。
此前,BGM0504在中国2型糖尿病受试者中开展的头对头挑战司美格鲁肽的II期临床试验,已展现出优异的降糖与减重综合代谢获益,整体表现优于司美格鲁肽。
而此次减重适应症的III期数据进一步证明:更强的双受体协同效应,尤其是GIP通路价值的进一步释放,不仅能够带来高水平的减重效果,同时也可能带来更全面的心血管代谢获益。这也正是BGM0504在血压、血脂、尿酸、骨密度等多个维度同时出现改善趋势的根本原因。
可以说,BGM0504的胜出并非偶然,而是基于对GIP机制的深刻理解与分子设计的精准把控。它所体现的,是一条从源头分子设计出发、系统构建差异化竞争壁垒的创新路径。
总结
替尔泊肽打开了GLP-1/GIP双靶点时代的大门,而BGM0504正在尝试推开下一扇窗。
GLP-1赛道的上半场,是一场围绕减重数字展开的竞赛。从单靶点到双靶点,从百分之十几到百分之二十,数字的攀升曾经是衡量产品竞争力的核心标尺。但当越来越多的同类产品涌入,当减重幅度逐步接近机制的天花板,这场竞赛的游戏规则正在悄然改变。
BGM0504的出现,恰好踩在了这个转折点上。它用一组完整的心血管代谢数据,回应了一个更本质的问题:一款代谢药物,究竟能为患者的整体健康带来什么?从血压到血脂,从尿酸到骨密度,BGM0504所展现出的系统性改善能力,正在重新定义减重药物的价值边界。它不再只是一个帮助患者“瘦下来”的工具,而是一套同时干预多个心血管代谢风险节点的综合管理方案。
从这个意义上说,BGM0504不只是一匹中国黑马,更像一个探路者——为GLP-1下半场的竞争,划出了一条新的起跑线。

 产业资讯
产业资讯
 赛柏蓝
赛柏蓝  2026-05-12
2026-05-12
 11
11

 产业资讯
产业资讯
 氨基观察
氨基观察  2026-05-12
2026-05-12
 3
3

 产业资讯
产业资讯
 Bio Journey
Bio Journey  2026-05-12
2026-05-12
 5
5
 热门资讯
热门资讯