 产业资讯
产业资讯
 MedTrend医趋势
MedTrend医趋势  2026-04-09
2026-04-09
 8
8
近日,全球权威医药数据机构Citeline发布了《2026年医药研发年度回顾》(Pharma R&D Annual Review 2026),这是该机构连续三十余年追踪全球制药研发趋势的年度重磅报告,是行业公认最权威的管线数据来源之一。(后台回复“报告”获取)
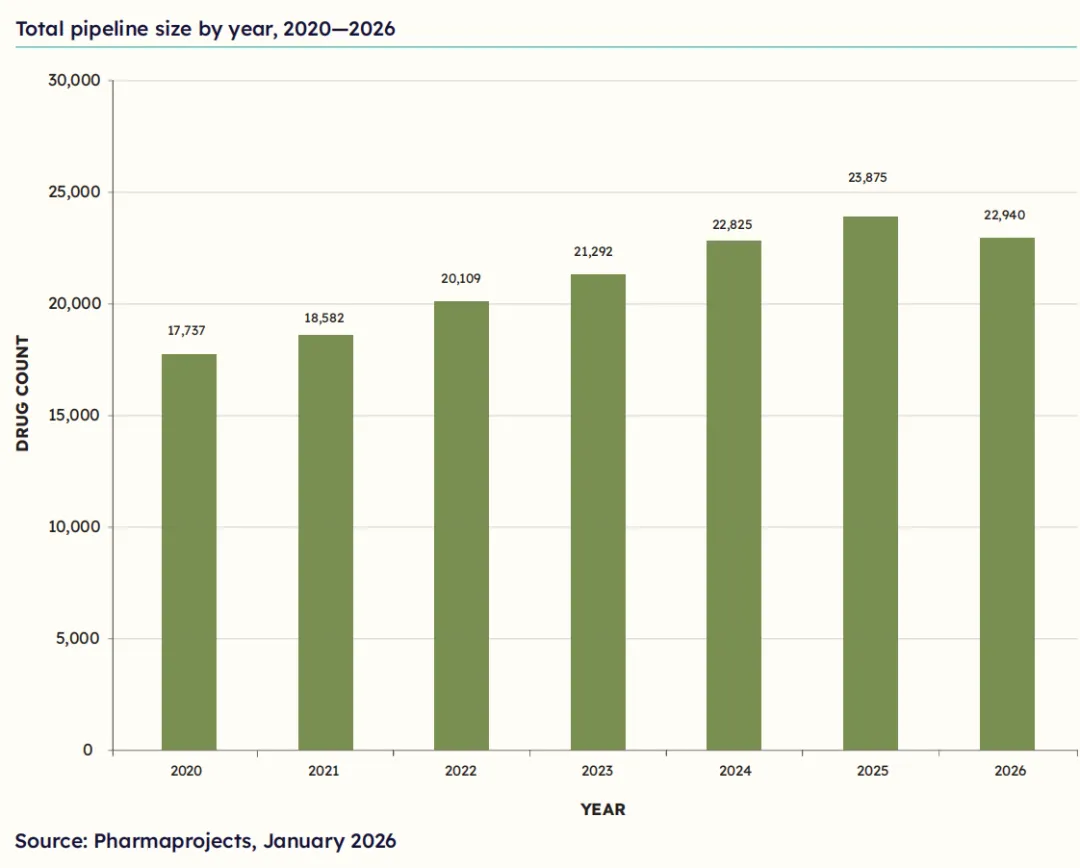
报告显示,截至2026年1月,全球在研药物总数降至22,940个,较上一年的23,875个下降3.9%。这是近三十年来,全球研发管线规模首次出现收缩。尽管统计口径调整被认为是部分原因,但一个更具确定性的信号已经浮出水面——
持续二十余年的扩张周期,正在走向终点。
这种结构变化,并非单一维度的调整,而是一次同时发生在企业格局、国家力量与技术路径上的系统性重构。
第一重变革,是制药巨头的排位洗牌。从企业层面看,大药企之间的竞争逻辑正在悄然改变。罗氏以稳定管线重回首位,阿斯利康凭借ADC与免疫布局快速跃升,而辉瑞则在收缩中重新聚焦核心资产。
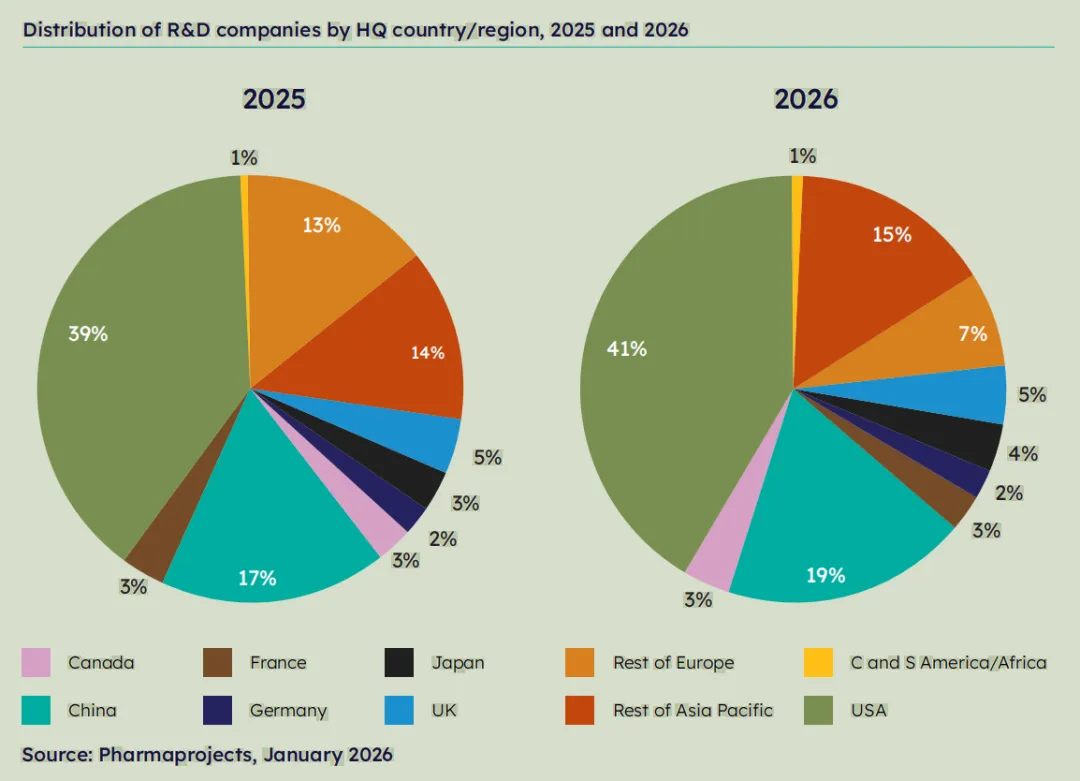
第二重变革,是中美创新速度的此消彼长。中国在全球候选分子中的占比已从2018年的8%跃升至约30%,成为跨国药企最重要的创新来源之一。
第三重变革,是治疗领域的竞争逻辑重构。肿瘤不再是唯一中心,免疫、代谢与神经科学快速崛起;小分子不再主导,而是在与生物技术的融合中寻找新的定位。
站在2026年的十字路口,全球制药研发正在从“规模驱动”走向“质量驱动”。所有这些变化,最终指向同一个问题:当行业从“做多”转向“做精”,谁还能持续胜出?
01
30年来首次降温:
全球研发管线增长按下“暂停键”
根据Citeline旗下Pharmaprojects数据库的统计,2001年,全球在研药物仅为5,995个;此后二十余年间,这一数字一路攀升,几乎未曾中断增长,直至2025年仍保持4.6%的增速。
从结构上看,2026年的回调并非均匀发生。除免疫和心血管领域仍保持增长外,大多数治疗方向均出现不同程度的收缩,其中肿瘤和抗感染领域的下降尤为明显。这意味着,行业并非简单“整体降温”,而是开始出现分化式调整——资源正在从部分拥挤赛道中撤出。
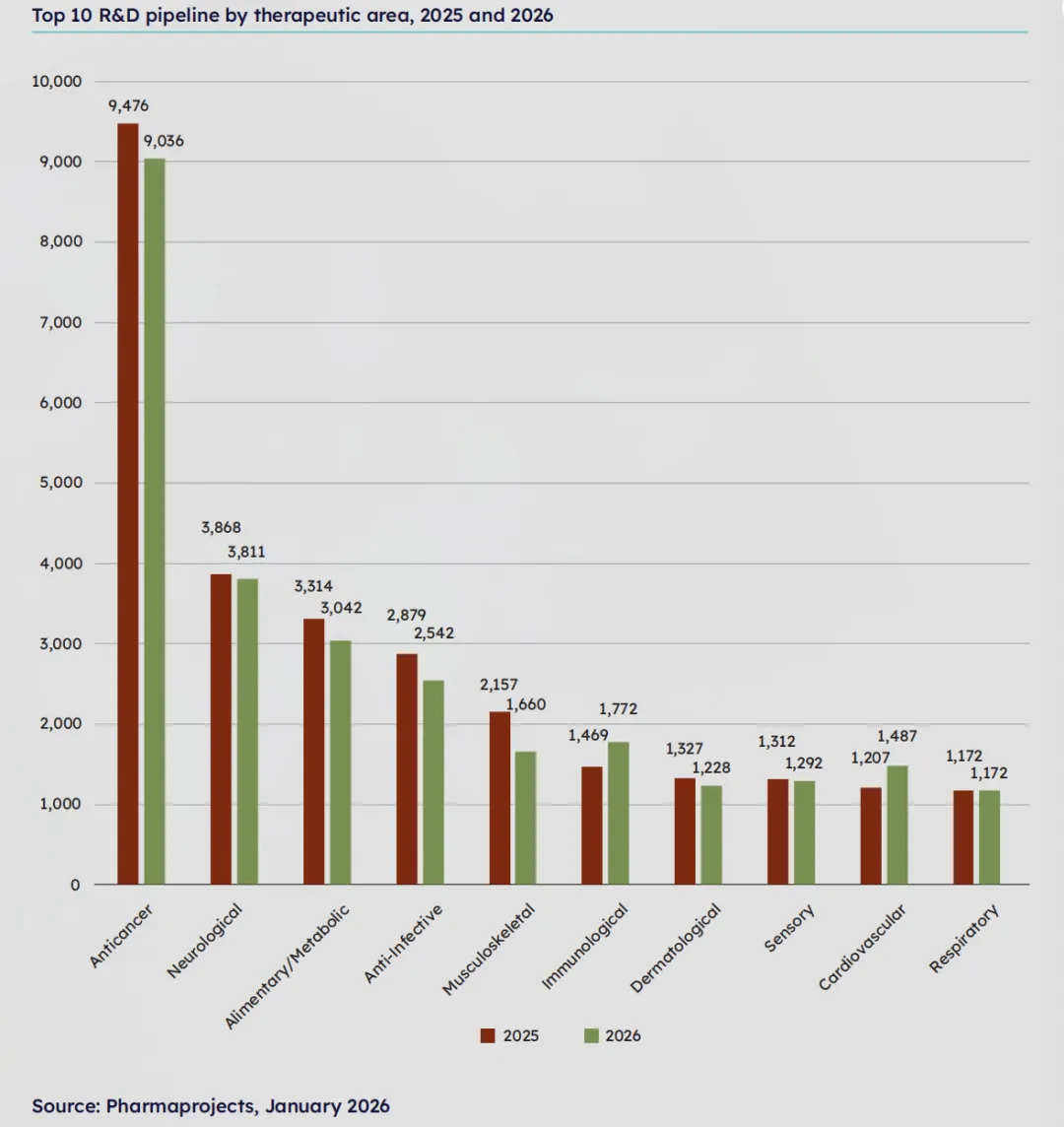
不过,Citeline在报告中也给出了一个重要的修正视角:此次下降,部分源于数据采集方法的变化。新的统计体系可能在一定程度上抬高了2025年的基数,同时压低了2026年的表现。如果剔除这一因素影响,Citeline认为,全球研发管线的规模在过去几年中“很可能保持了相当平稳的状态”,即维持在23000个分子上下的平台水平。
从更长的历史周期来看,研发管线规模从20年前的不到6000个到如今的近23000个,增长了近4倍,基数已然庞大,增速放缓也在情理之中。
02
Top10洗牌:收缩与补位
全球药物研发管线出现这样的下滑,具体原因是什么?
首先驱动变化的,是跨国药企自身的研发逻辑。
过去两年,随着“专利悬崖”临近与资本成本上升,全球大型药企普遍进入降本周期。从裁员、剥离非核心业务,到压缩早期研发投入,几乎成为行业共识。
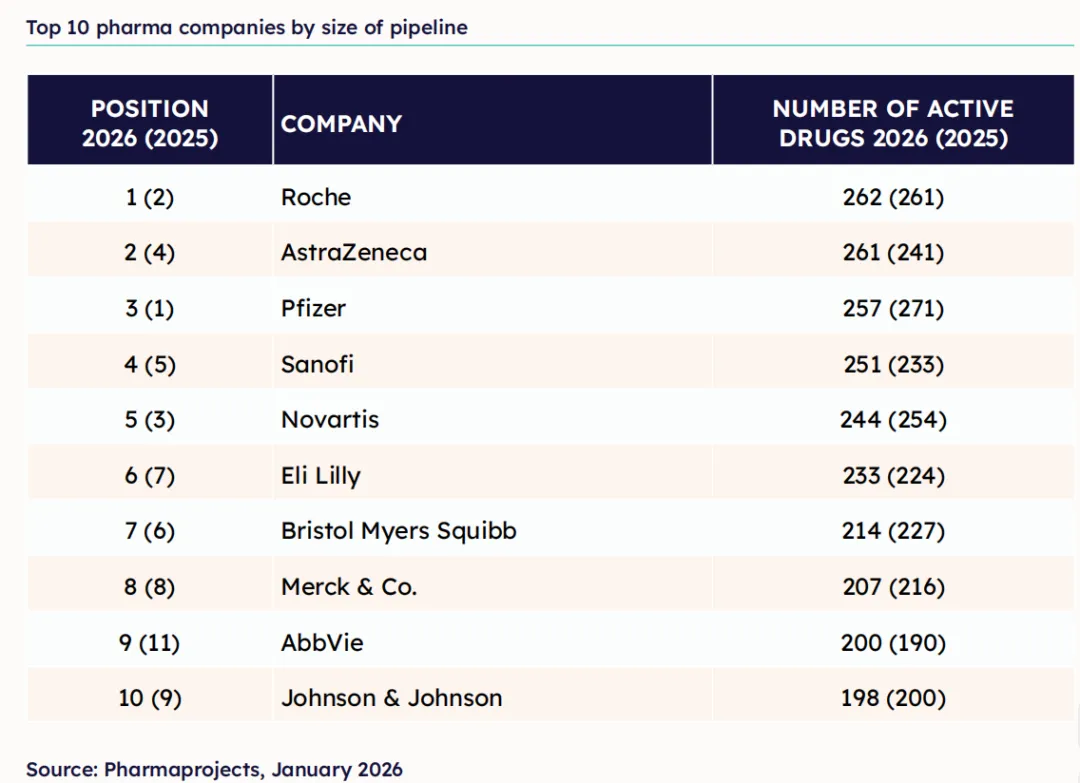
报告显示,2026年,罗氏以262个在研项目重回全球第一,管线规模微增1个至262个,几乎没有增长;曾位居榜首的辉瑞,则因管线调整从271个下降至257个,跌至第三位。
值得注意的是,阿斯利康以新增20个候选药物的表现,超越了辉瑞和诺华,攀升至第二位,成为Top10中增速最快的企业;赛诺菲则凭借管线扩张,超越了进行10个项目削减的诺华,跃居第五位。
与此同时,艾伯维首次进入前十(第9位,200个),而GSK则掉出榜单(从第9降至第11)。
其次,另一股力量正在对这一趋势产生对冲——来自中国的创新供给。
过去一年,全球创新药交易市场出现了一个极具标志性的变化:中国开始成为跨国药企“补充管线”的核心来源。2025年,中国创新药对外授权交易157起,总金额达到1357亿美元,较2024年实现翻倍增长,占全球交易总额约一半;而美国的占比则下降至不足30%。
进入2026年,这一趋势仍在加速。据国家药监局统计,今年前三月,中国创新药对外授权总金额已超过600亿美元。 这也意味着,2026年中国创新药对外授权规模在一季度内已逼近2025年全年总额的二分之一。典型案例包括:
1月,阿斯利康与石药集团达成一项最高价值约185亿美元的授权协议,依托后者专有的缓释给药技术平台及多肽药物AI发现平台,联合开发创新长效多肽药物;
2月,信达生物与礼来达成一项全新的肿瘤及免疫领域创新药物的研发合作,首付款3.5亿美元,里程碑金额最高约85亿美元;
3月,吉利德通过收购康诺亚相关资产(经由Ouro Medicines)推进T细胞衔接器布局,交易总额最高约21.75亿美元。
一个更具象的行业判断是:当前美国大型药企管线中,约三分之一的新分子已源自外部引进,其中相当比例来自中国。
第三个重要原因,是行业风险偏好的整体下降。
报告显示,过去一年,临床前与Ⅰ期项目出现显著收缩,出现了近10%的下滑;而Ⅱ期与Ⅲ期项目则相对稳定,有一定幅度的上涨。
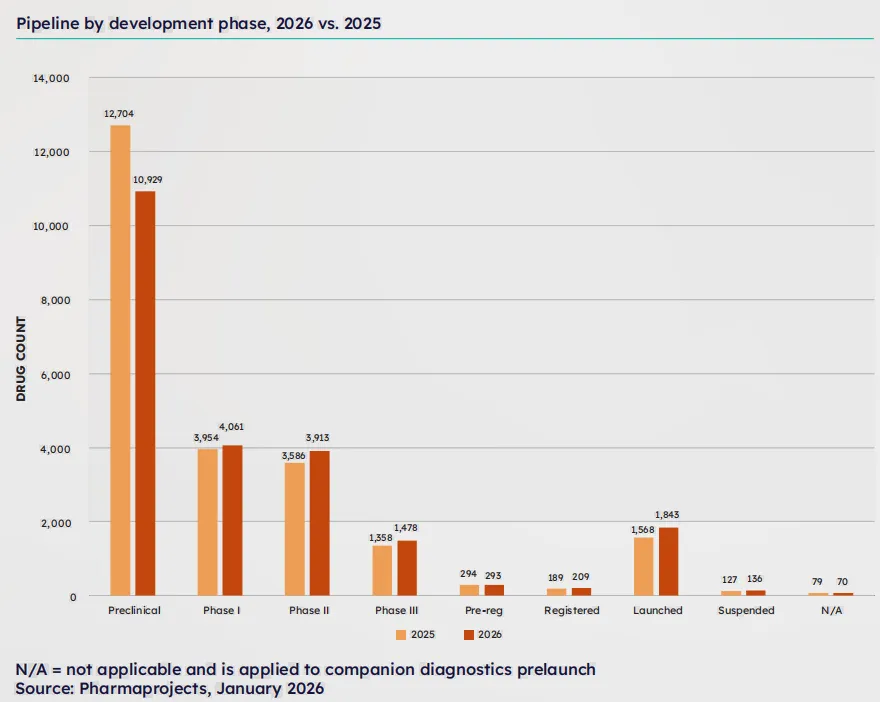
这一变化,在过去一年密集出现的“管线终止潮”中体现得淋漓尽致。
2025年,阿斯利康退出神经科学,终止与礼来合作的AD资产及偏头痛单抗;赛诺菲归还NK细胞衔接器权益;辉瑞一次终止11个项目,含Seagen核心资产;BMS、武田也清理了多笔收购所得管线。
这一定程度上表明,在研发成本持续攀升的背景下,行业已不再愿意为低确定性项目买单。越来越多企业选择在早期阶段就“止损”,避免后期更高昂的失败成本。
与此同时,人工智能等新工具的引入,通过对分子结构与靶点有效性的前期预测,一部分原本需要进入实验阶段的项目,已经可以在“计算中被淘汰”。2026年,Receptor.AI推出覆盖40+ADME-Tox终点的预测模型;ADMETPred则实现高通量早期筛选,为早期药物发现提供更快、更准确的药代动力学和毒性分析。
最后,不可忽视的是资本环境的变化。
过去两年,全球Biotech融资明显收紧,一批中小型公司被迫关停或出售资产,其管线要么终止,要么被并入大型药企体系之中。这种“被动出清”,同样对整体管线规模形成了压制。
根据Fierce Biotech发布的年度“Biotech Graveyard”,2025年共有16家生物科技企业正式关停,另有3家濒临破产,总数达到19家。2025年8月,诺奖得主创办的Appia Bio融资枯竭倒在IND前夕;11月,上海双抗企业同润生物被曝解散团队并成立清算小组。该公司2024年8月刚与默沙东就CD3×CD19双抗CN201达成13亿美元的BD交易,获得约7亿美元首付款。然而核心资产出售后,剩余管线无法支撑原有估值,上市与融资路径均不可行,最终走向清算。
此外,MNC退回权益则使原本有MNC资金支持的管线突然“断供”,中小Biotech无力独立推进,大量早期项目因此终止。比如,2025年Q1,吉利德Kite终止与Shoreline Biosciences价值超过23亿美元的现货型细胞疗法研究合作。2025年9月,诺和诺德在新任CEO主导的“全公司转型”中,终止了与Heartseed价值近6亿美元的心衰细胞疗法合作......
03
走出“堆量陷阱”
如果说全球研发管线的收缩是结构性调整,而中国市场面临的则是更现实的命题:当“数量优势”初步建立,堆量策略还能走多远?
一个典型的观察窗口,是龙头企业的表现。3月25日,恒瑞医药发布2025年报:营收316.29亿元(+13.02%),归母净利润77.11亿元(+21.69%),创新药收入占比首次超过50%。但财报发布后出现明显股价波动,反映出市场对于其“增长质量”的重新评估。
2025年,恒瑞共有7款1类创新药、6个已获批新适应症上市。然而扣除33亿元对外授权收入后,其营收仍在300亿以下,未见海外重磅药物那样的陡峭放量曲线。
背后原因不难理解:一方面,医保谈判机制使得创新药在上市初期即面临价格下探,放量路径更加依赖渗透率提升而非价格驱动;另一方面,国内市场的临床使用习惯、支付能力与分级诊疗体系,也决定了新药的放量周期更长、更平缓。
据Citeline发布报告,2025年已有三家中国药企进入全球研发管线前25。其中,恒瑞医药当前自研管线达到163条,位列中国第一、全球第二;中国生物制药则以125个在研项目排在所有药企中的第十五位;石药集团同样展现出不俗的研发野心,以102个在研项目位列榜单中部。
不过,这种“供给优势”并不意味着全面领先。从结构上看,中国创新仍高度集中于肿瘤与自免等确定性较高的领域,而在神经与精神疾病等高风险赛道上,仍明显落后于美国。波士顿咨询在最新报告中指出,这种差距恰恰存在于未来增长最快的方向之一。数据显示,神经系统疾病新进入管线的占比已从2023年的约12.7%上升至2025年的14%以上,成为增长最快的治疗领域。
头部公司已开始调整,比如恒瑞正逐步降低对单一肿瘤领域的依赖,转向代谢、自免、镇痛等慢病领域。这一策略与全球研发趋势形成呼应。
总体而言,当“堆量”遭遇“放量难”,当License-out尚未转化为全球商业化能力,中国创新药的下一阶段增长,将不再依赖简单的规模扩张,而取决于一个更关键的能力:能否从“做出分子”走向“做成产品”。这,比管线数量更难跨越。

 产业资讯
产业资讯
 研发客
研发客  2026-04-03
2026-04-03
 318
318

 产业资讯
产业资讯
 研发客
研发客  2026-04-09
2026-04-09
 7
7

 产业资讯
产业资讯
 MedTrend医趋势
MedTrend医趋势  2026-04-09
2026-04-09
 8
8