 产业资讯
产业资讯
 药渡
药渡  2026-04-10
2026-04-10
 4
4
近日,信达生物旗下新一代ROS1酪氨酸激酶抑制剂达伯乐®(己二酸他雷替尼胶囊,Taletrectinib)正式获得中国澳门特别行政区药品监管部门批准上市,用于治疗ROS1阳性局部晚期或转移性非小细胞肺癌(NSCLC)患者。
此次获批标志着澳门地区ROS1融合基因阳性肺癌患者迎来了全新的精准靶向治疗方案,也是信达生物继多款创新产品在中国香港、中国台湾及印度尼西亚等地区获批后,在粤港澳大湾区药物布局中取得的又一重要进展。
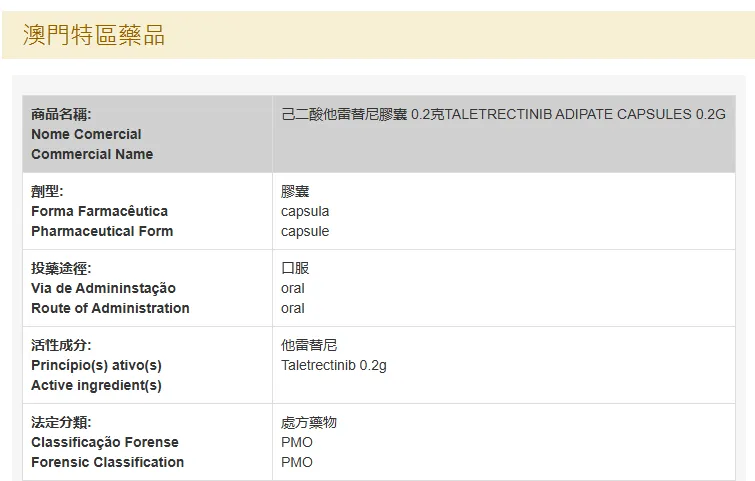
图1. 达伯乐®获澳门药品监管部门批准上市,来源:公司官微
1
关于ROS1阳性NSCLC
非小细胞肺癌是肺癌最常见的病理类型,其中ROS1基因融合阳性约占1%至2%。尽管比例不高,但由于肺癌患者基数庞大,每年新发的ROS1阳性NSCLC患者数量不容忽视。这类患者通常较为年轻、不吸烟,对传统化疗敏感性有限,精准靶向治疗是改善预后的关键。
然而,第一代ROS1抑制剂(如克唑替尼)在临床应用中面临两大挑战:
一方面,患者往往在治疗一段时间后出现耐药突变,尤其是G2032R等耐药位点导致药物失效;
另一方面,药物对中枢神经系统的渗透性不足,而脑转移是ROS1阳性NSCLC患者常见的疾病进展形式。
因此,临床迫切需要能够克服耐药、高效入脑的新一代ROS1抑制剂。
2
药物机制与临床数据
他雷替尼是一种口服、强效、高选择性的新一代ROS1抑制剂,同时具备良好的中枢神经系统活性。该药物能够高效抑制ROS1激酶活性,阻断肿瘤细胞增殖信号,尤其对第一代TKI治疗后出现的G2032R等耐药突变具有显著抑制作用。
他雷替尼的上市获批主要基于在中国ROS1阳性晚期NSCLC患者中开展的关键II期临床试验TRUST-I的优异数据。结果显示,在既往未接受过ROS1-TKI治疗的初治患者中,客观缓解率(ORR)高达90.3%,中位无进展生存期(PFS)达到44.6个月;在既往接受过ROS1-TKI治疗的患者中,ORR为51.5%,PFS为7.6个月。在基线存在可测量脑转移的初治患者中,颅内客观缓解率达87.5%,证实了其优异的血脑屏障穿透能力。
安全性方面,治疗相关不良事件多为1至2级,可通过剂量调整及支持治疗有效管理,未观察到新的安全信号。
基于TRUST-I及全球关键临床研究TRUST-II的积极结果,他雷替尼已获得中国国家药品监督管理局(NMPA)批准,并纳入新版国家医保药品目录;美国FDA也于2025年6月批准该药物用于局部晚期或转移性ROS1阳性NSCLC成人患者。在《2025 CSCO非小细胞肺癌诊疗指南》中,他雷替尼亦获ROS1融合阳性NSCLC治疗推荐。
3
竞品格局
从全球竞争格局来看,目前针对ROS1阳性NSCLC的靶向药物主要包括克唑替尼、恩曲替尼,以及新一代的洛普替尼和他雷替尼。克唑替尼虽率先获批,但受限于耐药和脑穿透力不足;恩曲替尼具备入脑活性,但对G2032R耐药突变无效。洛普替尼作为新一代抑制剂,于2023年获FDA批准,具有广谱抗耐药和强入脑特性。他雷替尼与洛普替尼同属新一代ROS1抑制剂,两者在疗效数据上各有优势。他雷替尼在初治患者中的客观缓解率高达90%以上,中位无进展生存期接近45个月,显示了持久的疾病控制能力;在经治患者中同样表现稳健。
更为重要的是,他雷替尼是首个由中国企业主导并成功在中美两国获批的新一代ROS1抑制剂(该药物最初由第一三共研发,后授权给葆元医药,信达生物于2021年获得其在大中华区的独家开发和商业化权益。葆元医药后于2024年被Nuvation Bio收购),信达生物与Nuvation Bio合作推动其全球开发,彰显了中国创新药企在精准靶向治疗领域的研发实力。
目前,TRUST-III验证性随机三期研究正在进行中,旨在比较他雷替尼与克唑替尼在初治ROS1阳性晚期NSCLC患者中的疗效,有望进一步巩固其一线治疗地位。
结 语
展望未来,他雷替尼在澳门的获批不仅为当地ROS1阳性肺癌患者提供了高效、持久、可入脑且能克服耐药的全新选择,也进一步完善了信达生物在大中华区的商业化版图。
截至目前,信达生物已有18款产品获批上市,覆盖肿瘤、自身免疫、代谢、眼科等重大疾病领域,其丰富管线与强大商业化能力为后续创新药物的可及性提供了坚实保障。
随着他雷替尼在更多国家和地区的获批以及医保覆盖范围的扩大,这一新一代ROS1抑制剂有望惠及更广泛的全球患者。同时,其成功经验也为其他国产精准靶向药物的出海路径提供了有益借鉴。

 产业资讯
产业资讯
 研发客
研发客  2026-04-03
2026-04-03
 387
387

 产业资讯
产业资讯
 生物技术小编
生物技术小编  2026-04-10
2026-04-10
 5
5

 产业资讯
产业资讯
 E药经理人
E药经理人  2026-04-10
2026-04-10
 5
5