 产业资讯
产业资讯
 丁香园Insight数据库
丁香园Insight数据库  2026-04-08
2026-04-08
 7
7
在刚刚过去的 Q1,我们见证了数款全球首创药物在中国落地,包括全球首个偏向型 GLP-1 埃诺格鲁肽(先为达)、病毒性肝炎领域第一款单抗药物立贝韦塔单抗(华辉安健)、全球首个 TSLP 单抗特泽利尤单抗(阿斯利康/安进)、全球首个 PD-L1/TGF-β 双靶点药物瑞拉芙普-α(恒瑞)……
而接下来的 Q2,涵盖肿瘤、罕见病及自免领域的数款「王炸」品种已蓄势待发。本文根据 Insight 数据库「中国上市策略& 时长预测」模块,选出其中 10 款重磅新药(排名不分先后)进行分享,仅供读者参阅。
科济药业:舒瑞基奥仑赛
全球首个实体瘤 CAR-T
2025 年 6 月 26 日,科济药业靶向 Claudin18.2 蛋白的自体 CAR-T 细胞治疗候选产品舒瑞基奥仑赛注射液的新药上市申请获 CDE 受理,用于治疗 Claudin18.2 表达阳性、至少二线治疗失败的晚期胃/食管胃结合部腺癌(G/GEJA)患者。
Insight 数据库显示,这也是全球首款且唯一一款提交 NDA 的用于治疗实体瘤的 CAR-T 细胞产品。
舒瑞基奥的 NDA 申请是基于一项在中国开展的开放标签、多中心、随机对照的确证性 II 期临床试验(CT041-ST-01, NCT04581473)结果,相关数据已在《柳叶刀》和 2025 年 ASCO 大会上正式公布。
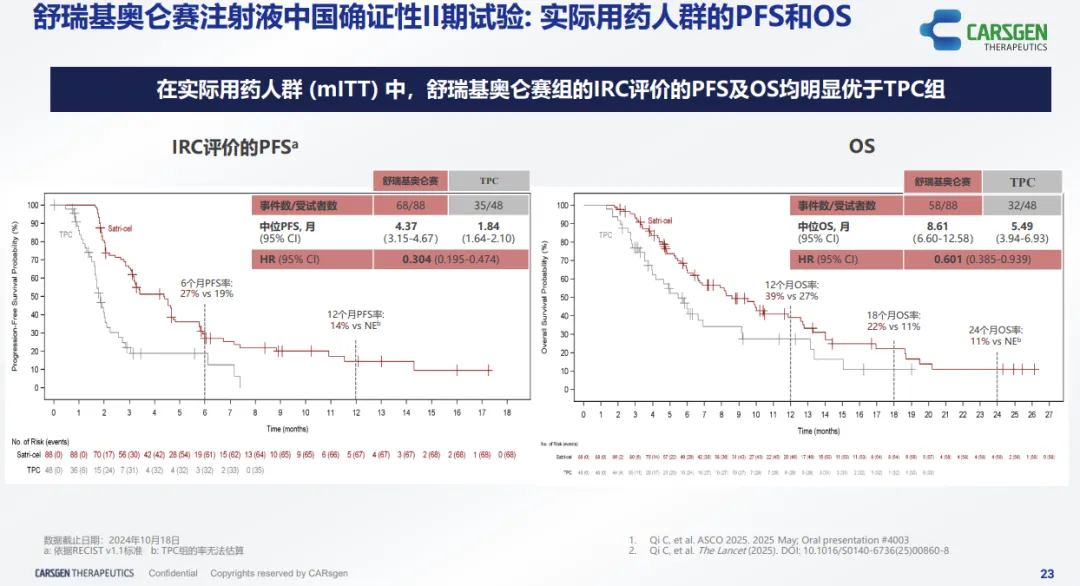
研究结果显示,在 ITT 即所有随机人群中,基于 IRC 评价,舒瑞基奥仑赛较标准治疗可显著延长 PFS(mPFS 3.25 个月 vs 1.77 个月;HR 0.366),达到试验的主要终点,患者疾病进展/死亡风险显著下降达 63%。同时 OS 显示出明显的获益趋势(mOS 7.92 个月 vs 5.49 个月;HR 0.693)。
在 mITT 即实际用药人群中,舒瑞基奥仑赛组 mPFS 为 4.37 个月(vs 1.84 个月,HR 0.304),患者疾病进展/死亡风险下降 70%;mOS 为 8.61 个月(vs 5.49 个月,HR 0.601),死亡风险下降 40%。
截图来源:企业官网
安全性方面,舒瑞基奥仑赛注射液治疗的整体耐受性良好,仅 4 例发生 3 级细胞因子释放综合症(CRS),无 4-5 级 CRS,无任何免疫效应细胞相关神经毒性综合征(ICANS)发生。
恒瑞医药:鲁兹诺雷钠
首个国产 URAT1 抑制剂
2025 年 1 月 9 日,恒瑞高选择性尿酸盐转运体(URAT1)小分子抑制剂鲁兹诺雷钠(研发代号:SHR-4640)的上市申请获 CDE 受理,适用于原发性痛风伴高尿酸血症的长期治疗。
在 2025 年欧洲抗风湿病联盟(EULAR)年度大会上,恒瑞以口头报告的形式公布了一项鲁兹诺雷钠治疗原发性痛风伴高尿酸血症的 III 期研究数据。结果显示:
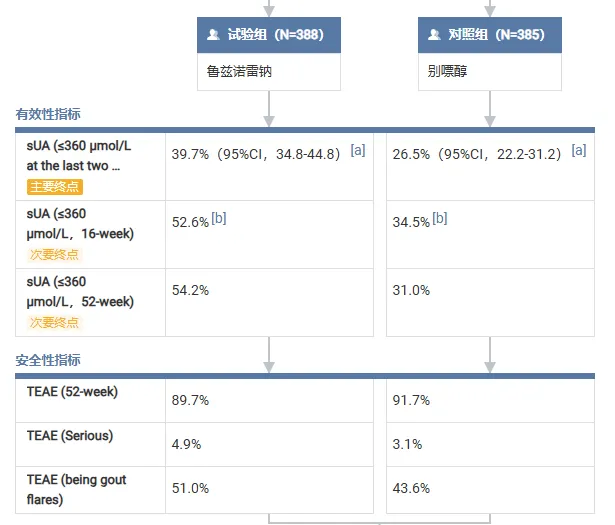
在为期 16 周的核心治疗期后,鲁兹诺雷钠片组 39.7% 的患者最后两次 sUA 水平 ≤360 μmol/L(临床达标阈值),显著高于对照组的 26.5%,治疗差异 13.1%(单侧 p<0.0001)。
第 16 周时 sUA≤360 μmol/L 的患者比例在鲁兹诺雷钠片组更高,分别为 52.6% vs. 34.5%(单侧 p<0.0001),且疗效优势在 52 周的扩展治疗期中持续保持(鲁兹诺雷钠片组 54.2% vs. 对照组 31.0%)。
截图来源:Insight 数据库
据 Insight 数据库统计,目前国内已有 10 余款高选择性 URAT1 抑制剂启动临床试验(不含申报/获批临床),仅卫材的多替诺雷获批上市。除此之外,鲁兹诺雷钠跑在最前列,为国内第 2 款、国产第 1 款。
智翔金泰:斯乐韦米单抗
全球首个用于狂犬病被动免疫的双抗
2025 年 1 月 14 日,智翔金泰宣布,已向 CDE 提交了斯乐韦米单抗注射液(研发代号:GR1801)新药上市申请并获得受理,用于成人疑似狂犬病病毒暴露后的被动免疫。
斯乐韦米单抗是一款重组全人源抗狂犬病病毒(RABV)双抗,作用靶点为 RABV 的包膜糖蛋白(G 蛋白),通过靶向结合 G 蛋白表位 I 和/或 III,阻断其与受体的结合,在狂犬疫苗主动免疫完全发挥保护作用前阻滞病毒对神经的侵染,预防狂犬病。
作为全球首个用于狂犬病被动免疫的双特异性抗体,斯乐韦米单抗分子设计满足 WHO 关于抗狂犬病病毒抗体开发的建议,采用针对不同抗原位点的多株单抗组合成「鸡尾酒式」组合制剂,以保证对不同病毒株或病毒的不同基因型的有效性。
2025 年 9 月,智翔金泰与康哲药业就斯乐韦米单抗在内的两款产品签订独家合作协议,授权康哲药业在中国大陆地区的所有商业化活动,以及除中国大陆之外的亚太地区及中东、北非区域的注册与商业化等工作,总金额超 5 亿元。
Insight 数据库显示,目前全球范围内共有超 10 款狂犬病抗体在研(仅统计活跃状态),其中绝大多数为单抗,还有 2 款混合抗体,仅斯乐韦米单抗 1 款双抗。
麓鹏制药:洛布替尼
全球首个第四代共价兼非共价 BTK 抑制剂
2025 年 5 月 28 日,麓鹏制药宣布 CDE 已正式受理洛布替尼片的新药上市申请,并已将其纳入优先审评程序,拟用于治疗既往接受过 BTK 抑制剂治疗的成人套细胞淋巴瘤(MCL)患者。
洛布替尼是全球首个第四代共价兼非共价 BTK 抑制剂,不仅能克服多种由 BTK 突变导致的对第一、二、三代 BTK 抑制剂的耐药,而且具有极高的活性和优异的靶点选择性,有望成为一款 BIC BTK 抑制剂。
此项 NDA 申请是基于一项在中国开展的 II 期关键性注册临床试验 ROCK-1 研究的积极结果(CTR20230100)。其数据已于 2025 年 9 月在 CSCO 大会上首次公布,并于同年 12 月在 ASH 年会上以口头报告的形式公布更新数据。
截至 2025 年 6 月,试验共入组 61 例经中心病理确认的 R/R MCL 患者。结果显示,IRC 评估的 ORR 为 63.9%,其中完全缓解率为 23.0%,中位 PFS 为 7.39 个月;中位随访 11.27 个月时,中位 DOR 为 16.46 个月,12 个月 DOR 率预估为 61.2%;中位随访 17.02 个月时,中位 OS 尚未达到。
安全性方面,严重出血(3 级及以上出血)发生率为 3.2%,未报告任何级别的心房颤动或心房扑动。33.9% 的患者因 TEAEs 暂停用药,3.2% 的患者需要剂量降低。未发生因 TEAEs 导致的永久停药或死亡事件。
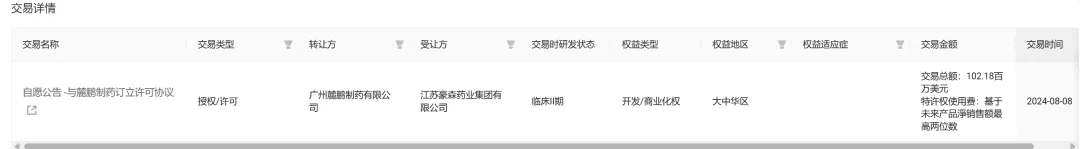
除了血液瘤以外,麓鹏制药也在开展针对慢性自发性荨麻疹、多发性硬化、视神经脊髓炎等非肿瘤适应症的临床研究。2024 年 8 月,翰森制药与麓鹏制药达成战略合作,获得了该产品所有非肿瘤适应症在中国 (包括香港、澳门和台湾地区) 的研发、注册、生产及商业化的权益。
截图来源:Insight 数据库
GSK:玛贝兰妥单抗
全球首个 BCMA ADC
2024 年 12 月 7 日,GSK 的 BCMA ADC 药物玛贝兰妥单抗在中国申报上市,与硼替佐米和地塞米松(BVd)联合用于治疗既往接受过至少一种治疗的多发性骨髓瘤成年患者。
该申请基于一项多中心、开放、随机、III 期研究 DREAMM-7 试验的积极结果。数据显示,玛贝兰妥单抗联合用药将患者死亡风险降低 51%,中位 PFS 延长至 31.3 个月,而达雷妥尤单抗三联疗法组的中位 PFS 为 10.4 个月(HR 0.31)。玛贝兰妥单抗联合用药的安全性和耐受性与各药物的已知特性大致一致。
2025 年 10 月,基于 DREAMM-7 试验的阳性结果,玛贝兰妥单抗获得 FDA 批准上市,适应症为玛贝兰妥单抗+硼替佐米+地塞米松用于治疗复发/难治性多发性骨髓瘤成年患者,这也是全球唯一获批上市的 BCMA ADC。
拜耳:塞伐艾替尼
HER2 口服靶向药
2025 年 7 月 23 日,拜耳塞伐艾替尼(BAY 2927088)申报上市,适应症为用于治疗携带 HER2(ERBB2)激活突变且既往接受过一种全身性治疗的晚期或转移性非鳞状非小细胞肺癌(NSCLC)成人患者。
塞伐艾替尼是一种口服可逆酪氨酸激酶抑制剂,可有效抑制突变型 HER2(包括外显子 20 插入和点突变),以及 EGFR(对突变型 EGFR 较野生型 EGFR 具有高选择性)。2025 年 11 月,FDA 基于 I/II 期 SOHO-01 试验的阳性结果,加速批准该药用于既往接受过治疗的晚期 HER2 突变非鳞状 NSCLC 患者。
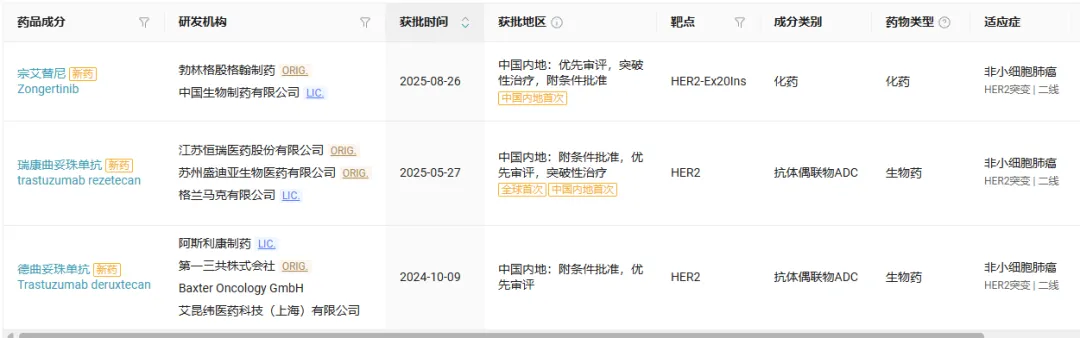
Insight 数据库显示,目前国内共有 3 款针对 HER2 突变的 NSCLC 靶向疗法获批,分别是瑞康曲妥珠单抗(恒瑞医药,注射剂)、德曲妥珠单抗(第一三共/阿斯利康,注射剂)以及宗艾替尼(勃林格殷格翰/中国生物制药,口服片剂)。塞伐艾替尼成功获批后,将成为国内第 4 款针对 HER2 突变的 NSCLC 靶向疗法,第 2 款 HER2 口服靶向药。
截图来源:Insight 数据库
辉瑞/再鼎医药:维替索妥尤单抗
宫颈癌领域首个 ADC 疗法
2025 年 3 月 13 日,再鼎医药宣布 CDE 已正式受理维替索妥尤单抗用于治疗系统性治疗期间或之后病情进展的复发或转移性宫颈癌患者的新药上市申请。
维替索妥尤单抗是再鼎从 Seagen(现已被辉瑞收购)引进的一款靶向组织因子(TF)的 ADC。该药已于 2024 年 4 月获得美国 FDA 完全批准,用于治疗在化疗期间或化疗后疾病进展的复发或转移性宫颈癌成年患者,是目前宫颈癌领域唯一一款获批的 ADC 疗法。
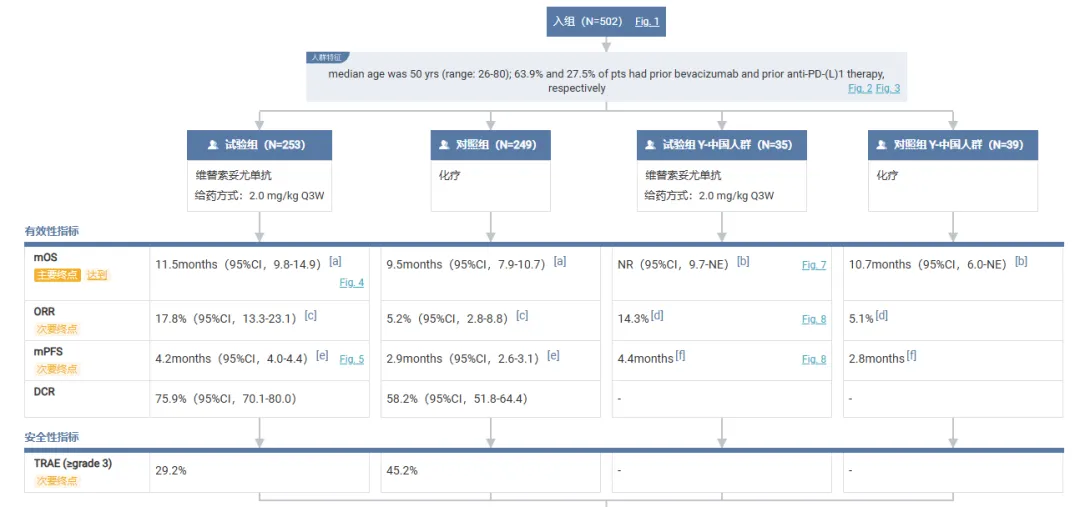
国内申请提交是基于全球随机 III 期 innovaTV 301 临床研究(NCT04697628)的结果以及该研究中国亚组的结果。根据 2025 年 1 月报告,中国亚组的结果与全球人群的结果一致。
结果显示,与化疗相比,维替索妥尤单抗降低死亡风险 45%,这些患者曾接受过标准系统性治疗,其中超过一半的中国人群曾接受过抗 PD(L)1 治疗。经过 11.5 个月的中位随访,维替索妥尤单抗组的中位 OS 未达到,而化疗组的中位 OS 为 10.7 个月。PFS 和确认的 ORR 的次要终点也有利于使用维替索妥尤单抗治疗。维替索妥尤单抗在中国亚组中的安全性是可控的,与全球概况一致。
截图来源:Insight 数据库
舒泰神:波米泰酶α
全球首创的凝血因子 X 激活剂
2025 年 5 月 31 日,舒泰神自主研发的波米泰酶 α(研发代号:STSP-0601)上市申请获得 CDE 受理,适应症为:本品可促进快速止血,适用于伴抑制物的血友病 A 或 B 成人患者出血按需治疗。
波米泰酶 α 是全球首创的凝血因子 X 激活剂,2019 年 7 月,获准开展临床试验,2024 年 3 月启动了一项针对伴抑制物的血友病患者出血按需治疗的 IIb 期临床试验(登记号:CTR20240597),并于 2025 年 1 月取得该研究总结报告。
IIb 期数据显示,波米泰酶 α 用于伴抑制物的血友病 A 或 B 患者出血按需治疗的疗效显著,且安全性良好,出血访视的有效止血率为 81.94%,显著优于 OPC(55%),差异具有统计学差异(P<0.0001),达到有效止血所需的给药次数为 1.9±0.7 次,77.12% 的出血访视给药 1~2 次即可有效止血。
值得一提的是,除了伴抑制物血友病治疗以外,2022 年 9 月,波米泰酶 α 获准开展「不伴抑制物的血友病 A 或 B 患者出血按需治疗」的临床试验,于 2023 年 12 月取得关于不伴抑制物的血友病 A 或 B 患者出血按需治疗的 II 期临床总结报告,有效止血率>95%。
永泰生物:爱可仑赛
国内首个实体瘤 CIK 细胞疗法
2025 年 3 月 31 日,永泰生物宣布 CDE 正式受理爱可仑赛注射液(扩增活化的淋巴细胞)的附条件上市许可申请,适应症为高复发风险原发性肝细胞癌外科根治术后预防复发,标志着中国首款针对实体瘤的 CIK(细胞因子诱导杀伤细胞)疗法进入上市审批阶段,更标志着实体瘤自体免疫细胞治疗药品从实验室走向临床应用的重大跨越。
爱可仑赛属于个性化自体细胞治疗产品,主要活性成分为 CD3+CD8+ 杀伤性 T 细胞,同时包含 NK 细胞、辅助 T 细胞等免疫细胞亚群,形成广谱抗肿瘤效应。与 CAR-T 类等基因改造疗法不同,爱可仑赛为非基因修饰技术,无需病毒载体转导,避免了基因插入突变风险,长期安全性更受到临床认可。
Insight 数据库显示,爱可仑赛于 2015 年提交 IND 申请, 并获得 CDE 受理,2017 年 10 月获得 IND 批件,2018 年 9 月入组第一例 II 期临床试验患者,该试验共纳入 430 例患者,目前其 II 期研究结果尚未披露。2025 年 3 月,该适应症被纳入优先审评。
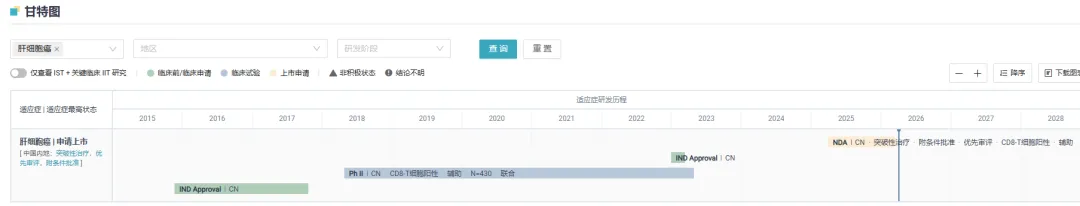
截图来源:Insight 数据库
华奥泰:瑞西奇拜单抗
首个国产 IL-36R 单抗
2025 年 10 月 1 日,华奥泰自主研发的瑞西奇拜单抗注射液(研发代号:HB0034)申报上市,用于治疗成人泛发性脓疱型银屑病(GPP)发作,并于 2025 年 8 月被 CDE 纳入优先审评。
作为一款创新抗 IL-36R 抗体,瑞西奇拜单抗可通过抑制 IL-36 通路发挥抗炎的生物学效应。2025 年 3 月,瑞西奇拜单抗用于治疗泛发性脓疱型银屑病急性发作的关键性临床试验达到主要疗效终点和所有次要疗效终点。研究分析结果显示,相比于安慰剂,瑞西奇拜单抗单次静脉给药后的第 1 周 GPP 发作患者的皮肤脓疱得到明显清除,达到方案预设的主要研究终点;安全性方面表现良好,未发现新的安全性信号。
根据 Insight 数据库统计,目前国内共有 6 款 IL-36R 抗体进入临床阶段,仅有勃林格殷格翰的 IL-36R 抗体司柏索利单抗获批治疗 GPP,瑞西奇拜单抗是首个申报上市的国产 IL-36R 单抗。

截图来源:Insight 数据库

 产业资讯
产业资讯
 研发客
研发客  2026-04-03
2026-04-03
 298
298

 产业资讯
产业资讯
 同写意
同写意  2026-04-08
2026-04-08
 5
5

 产业资讯
产业资讯
 丁香园Insight数据库
丁香园Insight数据库  2026-04-08
2026-04-08
 7
7