 产业资讯
产业资讯
 药智网
药智网  2026-04-23
2026-04-23
 11
11
当前,全球已有12款TCE药物获批上市,其中9款用于血液瘤治疗,靶点集中在CD20、BCMA、CD19及GPRC5D等肿瘤靶向抗原。而在研管线中,一批“萌芽期”的新靶点也开始崭露头角。
近日,迈威生物宣布,NMPA已受理其自主研发的6MW5311的临床试验申请,拟开发适应症为血液瘤(急性髓系白血病、慢性粒单核细胞白血病以及多发性骨髓瘤)。
值得注意的是,6MW5311为全球首款申报临床的靶向LILRB4/CD3 TCE双抗创新药,其美国临床试验申请也已处于pre IND阶段,公司计划于2026年第二季度向FDA正式递交申请。
01
差异化瞄准“缺药”市场
LILRB4(白细胞免疫球蛋白样受体亚家族B成员4)是一种新型免疫检查点分子,在近年来逐渐进入行业视野。
这是一种主要表达于髓系来源免疫细胞膜上的Ⅰ型膜蛋白,主要参与免疫应答的负向调控。研究发现,在单核细胞急性髓系白血病(AML)中LILRB4显著高表达,且与不良预后密切相关。在慢性粒单核细胞白血病(CMML)、多发性骨髓瘤(MM)中,该靶点同样显著表达,且在正常组织中表达谱狭窄,为靶向治疗提供了理想的治疗窗口。
目前,全球已有针对LILRB4的单抗、CAR-T和ADC疗法进入临床,但尚无靶向LILRB4/CD3的TCE双抗进入临床阶段。迈威生物的6MW5311率先提交临床申请,有望成为该领域的首个突破者。
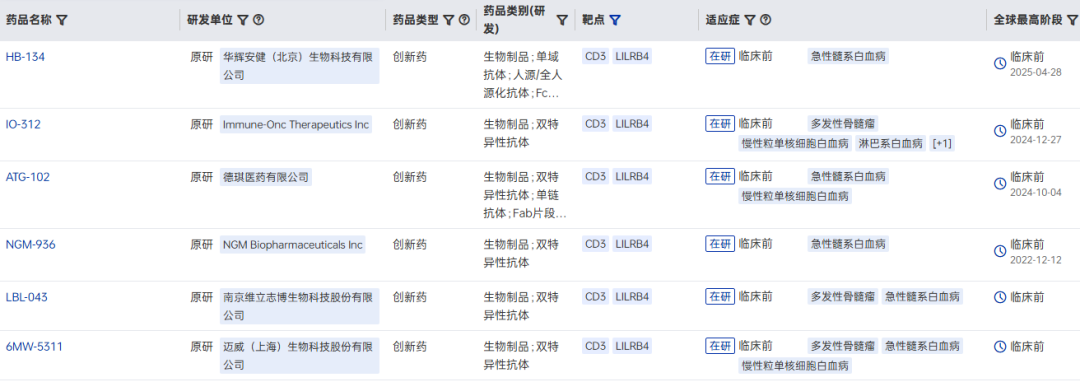
图1 全球在研LILRB4/CD3 TCE双抗
图片来源:药智数据
从适应症看,迈威生物采取了一贯的差异化策略。
目前已获批上市的TCE药物适应症主要覆盖B细胞淋巴瘤、淋巴细胞白血病及多发性骨髓瘤等血液瘤亚型。但针对AML、CMML等血液瘤,尚无TCE产品获批。
AML是成人中最常见的急性白血病,2022年全球AML新发病例数约为17.24万例,预计2035年将增长到22.14万例,年复合增长率为1.94%。其中中国AML新发病例约为3.08万例,约占全球总量的17.9%。尽管近年来去甲基化药物联合维奈克拉等方案提升了治疗效果,但难治/复发患者仍面临严峻挑战。
CMML是一种罕见的血液恶性肿瘤,年发病率约为(3~4)/10万。目前除异基因造血干细胞移植外,CMML患者极度缺乏有效治疗药物。
MM患者则困于复发,仍需要寻找新靶点和新机制的治疗手段。
LILRB4作为一个新的免疫治疗靶点,如果TCE双抗能够验证有效,将为这些患者带来新的治疗希望。6MW5311精准切入这些“缺药”领域,瞄准未被满足的临床需求市场。
6MW5311采用“2+1”非对称分子结构,同时靶向LILRB4和CD3,通过桥接肿瘤细胞与T细胞形成免疫突触,激活T细胞并高效杀伤肿瘤。其关键设计在于引入了独特的空间位阻结构——显著降低CD3抗体在无肿瘤细胞环境下对T细胞的结合活性,仅在肿瘤细胞存在时特异性激活T细胞。
这一“条件性激活”思路在行业内备受关注。TCE药物研发的一大难点就在于安全性,其治疗窗口与能否将T细胞激活严格限制在肿瘤微环境内密切相关。
体外研究显示,6MW5311对多个肿瘤细胞系及患者来源样本均表现出强效杀伤活性;在食蟹猴模型中,也表现出良好的安全性特征。
体内药效学研究表明:在LILRB4高表达及低表达的AML肿瘤模型中,6MW5311均显示出明确的肿瘤抑制作用,尤其在高表达模型中可实现肿瘤完全清除。
整体来看,迈威生物选择了一个有挑战但逻辑清晰的靶点,在分子设计上巧妙构思,采取“条件性激活”策略,增强疗效的同时降低毒副作用。但最终的效果还需要人体数据来回答。
02
千亿风口市场
6MW5311的背后是迈威生物自主研发的创新型TCE技术平台。
该平台的核心是一组具有不同结合特征和活化特性的经改造靶向CD3抗体。这些具有自主知识产权的抗体分子具备不同的结合活性和激活能力:一方面保持对人CD3的高亲和力,另一方面具有与食蟹猴CD3的交叉反应性。这一特性为在非人灵长类动物模型中准确评估TCE分子的安全性提供了关键工具。
近年来,T细胞衔接器(TCE)成为下一代免疫治疗的热门方向。其分子一端靶向T细胞CD3分子,另一端精准结合癌细胞特异性抗原,直接“拉近”T细胞与肿瘤细胞的距离,触发T细胞的定向杀伤效应,兼具靶向性和高效性。
根据沙利文预测,全球TCE药物市场规模预计将从2022年的约10亿美元增至2035年1211亿美元以上,年复合增长率超40%。沙利文最新发布的《2026全球抗体药物行业发展蓝皮书》进一步指出,T细胞衔接类双抗(TCE)在全球抗体市场中的占比预计将从2024年的1.2%飙升至2035年的17.9%,成为增速最快的细分领域之一。
与市场高增长相伴的是竞争的白热化。药智数据显示,近几年在研TCE管线数量大幅增长,其中大部分处于临床前和早期临床阶段,可见大批药企正在涌入这一赛道。
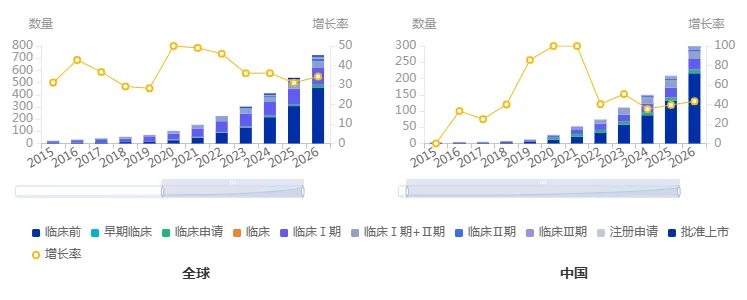
图2 在研TCE疗法整体趋势
图片来源:药智数据
此时,平台化的创新能力便成为竞争的核心。
目前大部分TCE产品使用的是单一CD3抗体,激活强度固定。但不同靶点、不同肿瘤类型对T细胞激活的阈值要求差异很大。
迈威生物的CD3抗体库思路,本质上是把‘选择权’前置到分子设计阶段,有可能在未来实现更精细化的开发策略。
该抗体库涵盖了从强效激活到温和激活的完整活性谱系。研发人员可以根据靶点的表达水平和肿瘤微环境的特征,选择最合适的CD3抗体进行组装,实现“按需调控T细胞激活强度”。
此外,迈威生物还前瞻性地布局了下一代TCE,引入共刺激信号,探索三抗、多抗等分子形式,通过多靶点协同激活,提升T细胞在实体瘤和免疫抑制性微环境中的持久杀伤能力。
目前,除了6MW5311,迈威生物预计还有多个靶向实体瘤的TCE项目将陆续进入临床前阶段。
03
TCE+ADC双引擎协同可期
在肿瘤免疫治疗2.0时代,TCE正成为继ADC之后又一备受瞩目的技术方向。
迈威生物凭借6MW5311这一全球首创的LILRB4/CD3 TCE双抗,率先切入AML、CMML等缺乏有效疗法的血液瘤细分市场,同时依托其差异化的TCE技术平台,形成了从靶点选择到分子设计的完整护城河。
同时,迈威生物已在ADC领域建立优势,拥有9MW2821(Nectin-4 ADC)、7MW3711(B7-H3 ADC)、7MW4911(CDH17 ADC)等多个临床阶段的潜力ADC药物。
行业内普遍认为,ADC与TCE的联合使用有望成为肿瘤治疗的新标准疗法。前者可精准高效杀伤肿瘤细胞,具备替代传统化疗的潜力;后者可高效激活人体自身免疫系统攻击癌细胞;两者有望形成协同增效。
迈威生物同时握有ADC和TCE两大技术平台,给未来在联合治疗上留下探索空间,值得持续关注。

 产业资讯
产业资讯
 药智网
药智网  2026-04-23
2026-04-23
 11
11

 产业资讯
产业资讯
 医药笔记
医药笔记  2026-04-23
2026-04-23
 9
9

 产业资讯
产业资讯
 氨基观察
氨基观察  2026-04-23
2026-04-23
 31
31
 热门资讯
热门资讯