 产业资讯
产业资讯
 氨基观察
氨基观察  2026-04-24
2026-04-24
 8
8
继年初24亿美元收购Orna Therapeutics,礼来再次重金押注体内CAR-T。
4月20日,礼来宣布以70亿美元的价格收购Kelonia Therapeutics,将体内CAR-T赛道的交易估值推向一个新高峰。算起来,礼来2026年仅在体内CAR-T赛道就已投入近100亿美元。
值得注意的是,这次收购的也并非成熟资产,Kelonia的核心药物KLN-1010仍处I期,仅完成4例患者的早期验证。Orna的核心资产ORN-252则处于临床试验准备阶段。
显然,礼来押注的并不是某个分子,而是两条差异化的体内CAR-T技术路径。
Orna采用LNP递送+环状RNA体系,在体内稳定性与蛋白表达持续性上具备优势,更契合自身免疫疾病等长期治疗场景;Kelonia则基于慢病毒递送,延续了传统CAR-T在肿瘤领域的技术逻辑。
不止礼来,过去一年,从阿斯利康到艾伯维,再到吉利德、BMS,多家MNC纷纷重金收购体内CAR-T公司,掀起赛道并购热潮。
MNC的集体重仓加持,既推高了体内CAR-T资产的价值,也印证了赛道的核心价值与广阔潜力。但需要认清的是,目前体内CAR-T整体仍处于早期阶段,疗效稳定性、安全性等关键问题尚未得到充分验证。
这一轮并购潮是对“下一代”细胞治疗的提前卡位,未来几年内能否兑现预期,仍有待观察。
/ 01 /
估值水涨船高
礼来最新的收购,刷新了体内CAR-T领域的交易纪录。
在此之前,赛道已频现重磅交易。阿斯利康以10亿美元收购EsoBiotec,吉利德旗下Kite以3.5亿美元买下Interius Bio Therapeutics,并与Pregene签署了价值高达16亿美元的合作协议;艾伯维也先后两次出手,14.4亿美元与Umoja达成合作后,又以21亿美元收购了Capstan Therapeutics,BMS则以15亿美元拿下了Orbital Therapeutics。
仅对比收购价,礼来70亿美元的收购属实不低。体内CAR-T资产整体也呈现出越来越贵的趋势,这背后是由临床数据驱动的。
Kelonia核心管线KLN-1010,是一款靶向BCMA的体内CAR-T疗法,用于治疗复发/难治性多发性骨髓瘤,目前处于一期临床阶段。
礼来之所以愿意重金收购,核心原因之一就是其早期临床数据表现出的疗效潜力。
2025年ASH年会上,Kelonia展示了KLN-1010的首批数据:四例复发/难治性多发性骨髓瘤患者,在接受单次KLN-1010输注后,1个月均实现了骨髓微小残留病(MRD)阴性缓解,随访时间最长的两名患者在三个月内均保持了MRD阴性反应。在最长的5个月随访期内,所有患者均保持应答状态,显示出一定的持续性信号。
其体内扩增能力也接近已上市体外CAR-T水平,在未进行淋巴清除化疗的前提下,循环T细胞中CAR-T占比可达85%。
安全性方面,KLN-1010同样表现良好,四名患者接受KLN-1010治疗后未出现≥3级CRS,无免疫效应细胞相关神经毒性综合征(ICANS),无延迟性神经毒性,且细胞减少症明显降低,这是体外CAR-T无法实现的。
基于上述数据,2026年1月,KLN-1010获FDA批准IND申请,用于复发/难治性多发性骨髓瘤治疗。
礼来肿瘤业务发展负责人Jacob Van Naarden表示:“自体CAR-T疗法显著改善了多种癌症患者的治疗效果,但由于生产、安全性和可及性方面存在诸多障碍,只有一小部分符合条件的患者能够真正接受治疗。Kelonia的体内平台有望改变这一现状,它能够以更简单、更便捷的方式提供快速、持久的疗效。”
由此来看,支撑本轮交易的高溢价,是Kelonia体内CAR-T平台的治疗潜力,而这4例患者的数据虽然规模有限,却提供了最直观的疗效证据。
未来,随着更多临床数据的读出,或许我们会看到体内CAR-T估值的继续上涨。
/ 02 /
技术两头下注
自2024年以来,体内CAR-T开始快速发展,多家MNC掀起了技术军备竞赛。礼来入场虽晚,但通过先后收购Orna Therapeutics和Kelonia Therapeutics,已完成体内CAR-T两大核心领域的布局:肿瘤与自免。
2026年2月,礼来收购Orna Therapeutics,其核心资产ORN-252是一款靶向CD19的体内CAR-T产品,主要用于治疗系统性红斑狼疮(SLE)等B细胞驱动的自身免疫疾病,目前处于IND准备阶段。
在2025年ASH大会上,Orna公布了ORN-252的早期体内数据。在人源化狼疮模型中,ORN-252在低至0.03mg/kg剂量下即可有效清除B细胞,并显著降低dsDNA抗体水平,表现出优于利妥昔单抗治疗的效果。在非人灵长类实验中,仅需0.1mg/kg剂量,即可实现外周血及脾脏B细胞的完全清除,同时诱导CAR-T细胞短暂扩增。
更重要的是,其呈现出可控的持久性:在B细胞再生后,免疫系统向幼稚B细胞重建,提示其具有免疫重置潜力。
适应症之外,礼来也对技术路线进行了双线押注。
ORN-252的研发基于LNP递送+环状RNA(panCAR™)平台。其中环状RNA通过将线性RNA自环化,显著提升稳定性与表达效率,并降低免疫原性风险。且环状RNA无帽、无尾、无修饰核苷的特性,相较传统mRNA,具有更长半衰期、更高蛋白表达、更易规模化生产,有利于封装进LNP体系。
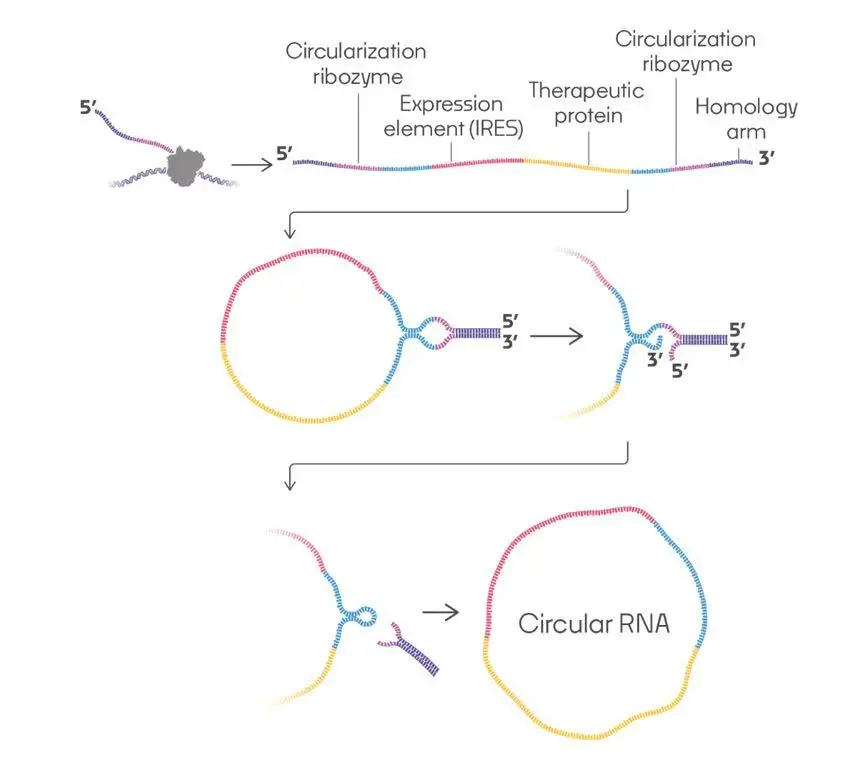
而其递送依赖的LNP避免复杂的配体修饰,从而降低免疫原性风险。具体表现为短期可衰减,支撑重复给药。而可控长期的的优势也更适配自身免疫疾病。
与之对应,Kelonia则代表另一条的路线。Kelonia基于iGPS®平台,通过工程化慢病毒在体内直接改造T细胞,实现CAR基因的稳定整合与长期表达。
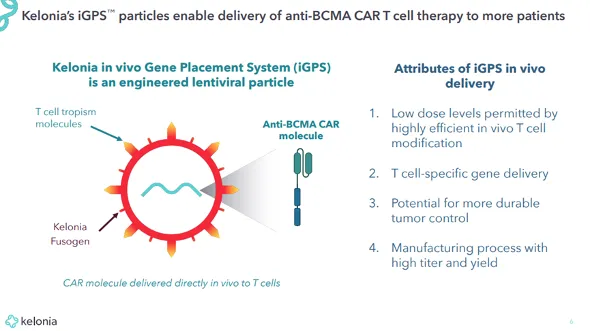
慢病毒的递送方式,延续了传统CAR-T在肿瘤领域的技术逻辑,即通过慢病毒载体将CAR基因稳定整合到T细胞基因组中,具备更强的持久性,有望实现
“功能性治愈”。
进一步,其体内基因定位系统(iGPS) 通过去除病毒天然受体结合能力,并在包膜结构中掺入抗CD3单链抗体片段(scFv),实现对T细胞的选择性识别与靶向递送,从而提高体内转导的细胞特异性。降低给药剂量的同时有潜力应用于更多患者。
被收购之前,Kelonia的技术平台也与多家MNC达成合作。2025年初,Kelonia与安斯泰来旗下Xyphos Biosciences达成体内CAR-T开发合作;10月,强生宣布与Kelonia达成战略合作,依托iGPS®平台共同开发下一代体内CAR-T疗法。
完成这两笔交易后,礼来成为了全球唯一一家拥有自免+肿瘤两款体内CAR-T技术平台的公司。这也提醒我们,在这个前沿赛道没有所谓赢家通吃,技术与临床的最终验证,才是决定赛道走向的核心。
/ 03 /
谨慎与乐观并存
尽管技术前景可期,过去两年,体内CAR-T研发也取得了一些实质性进展,获得了MNC的集体押注。然而,作为一种新型体内基因疗法,其临床疗效与安全性表现仍需审慎看待。
毕竟,颠覆性的潜力并不能掩盖研发风险。
以阿斯利康收购EsoBiotec获得的体内CAR-T产品ESO-T01为例。ESO-T01在治疗复发/难治性多发性骨髓瘤的I期临床中,释放出较强的早期疗效信号:80%(4/5)患者实现客观缓解,其中3例达到严格意义上的完全缓解。
但与疗效信号同步出现的,是不可忽视的安全性问题。
今年3月,《nature medicine》杂志上公布了ESO-T01的临床完整数据,“普遍耐受良好””的安全性结论背后,隐藏着令人担忧的副作用。
体外CAR-T常出现的CRS同样发生在ESO-T01治疗的患者身上,五名患者中四名出现了CRS,其中三名患者出现3级CRS。此外,研究中还观察到两名患者在30天内出现2级单纯疱疹病毒和一名患者在输注后6个月出现肺部感染。这提示在免疫系统重塑窗口期,患者仍存在一定程度的免疫抑制或免疫失衡状态。
更严重的是,有1例患者发生ICANS,并最终因髓外病灶进展导致脊髓压迫死亡。尽管该事件与疾病进展本身存在交叉因素,但也暴露了体内CAR-T存在不可控风险。
虹信生物的HN2301则指向了体内CAR-T的另一约束:持久性。
HN2301是基于LNP载体的CD19 in vivo CAR-T,用于SLE。在针对SLE患者的I期临床试验中,5例患者在接受治疗后3个月观察到 SLEDAI 2000 评分下降。安全性问题上,无ICANS和≥3级CRS发生。
但该药的持续时间较短,给药后约6小时快速达到峰值,但整体体内持续时间仅维持2–3天,显著短于慢病毒整合或LNP表达体系。
当然,尽管挑战重重、临床验证之路也道阻且长,但作为肿瘤与自身免疫疾病治疗的颠覆性创新方向,体内CAR-T仍将以技术革新重构细胞治疗的底层逻辑。
随着全球药企的持续投入与临床的不断验证,这项前沿技术终将突破现有局限,为无数难治性疾病患者打开全新治疗窗口。

 产业资讯
产业资讯
 E药经理人
E药经理人  2026-04-24
2026-04-24
 8
8

 产业资讯
产业资讯
 动脉网
动脉网  2026-04-24
2026-04-24
 9
9

 产业资讯
产业资讯
 氨基观察
氨基观察  2026-04-24
2026-04-24
 8
8
 热门资讯
热门资讯