 产业资讯
产业资讯
 瞪羚社
瞪羚社  2026-04-30
2026-04-30
 7
7
4月28日,一家名不见经传开发脱发药的Biotech公司Veradermics(NYSE: MANE)暴涨。
暴涨源自MANE旗下的米诺地尔缓释口服片VDPHL01,II/III期Study 302研究大获成功。
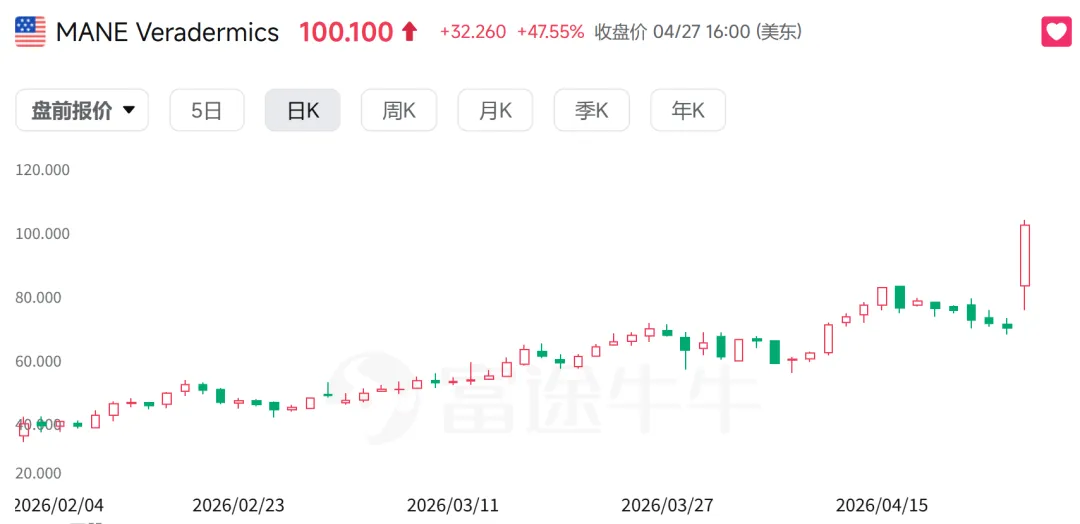
Study
302研究,519例男性,随机双盲对照,44个美国临床中心,主要终点全部达到,p<0.0001。这是美国近30年来,口服脱发治疗领域第一个站得住脚的Phase
2/3结果。
消息出来,Jefferies重申买入评级,目标价75美元——随后公司直接在高位发行融资约2.13亿美元,账上现金一并延伸至2030年。
MANE,正在主导一场新的生发革命。
01
被低估的脱发市场
卫健委数据显示,中国脱发人群超过2.5亿——平均每6个人里,就有1个正在为自己的头顶发愁。全球范围内,美国一地的雄激素性脱发(AGA)患者就超过8000万,其中5000万男性,3000万女性。
目前药物治疗的市场却长期被两款老药把持:1988年获批的外用米诺地尔,和1997年获批的口服非那雄胺。整整三十年,没有新的收到FDA批准的口服选项出现。
先说非那雄胺(Finasteride),其通过抑制5α-还原酶II型,降低双氢睾酮(DHT)水平来减缓毛囊微小化。它有效,这一点毋庸置疑——数据显示安慰剂调整后TAHC(目标区域毛发计数)增量约Δ+14.4 hairs/cm²,是过去二十年里口服治疗的事实标准。
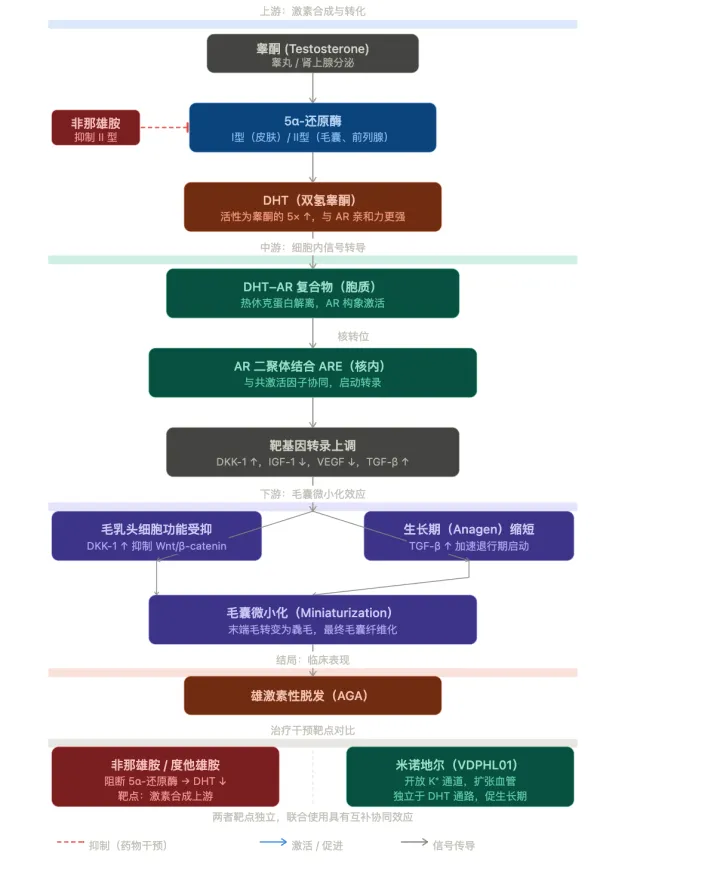
非那雄胺的治疗代价同样沉重:性功能障碍是其广为人知的副作用,更值得关注的是,2025年10月FDA进一步更新警示,一份发表于《JAMA
Dermatology》的评论正式指出,FDA在调查非那雄胺与抑郁症风险之间联系上的工作力度不够。这不是一个新的担忧,但正式进入监管视野,意味着后续标签变更的可能性在上升。
度他雄胺(Dutasteride)是双重5α-还原酶抑制剂,在韩国和日本已批准用于AGA,疗效略优于非那雄胺(TAHC增量约Δ+17 hairs/cm²),但携带同类风险:性功能障碍、长达5周的半衰期、停药后至少6个月才能献血。美国FDA至今未批准这个适应症。
市场调研的数字更直接:仅9%的患者对现有治疗选项感到满意,而46%正在主动寻找新的替代方案。这两个数字放一起,藏着的是一个行业巨大的外满足需求空间,也是VDPHL01此次数据如此受市场关注的根本原因。
三十年没有新选项,不是因为这个病不重要,是因为它太难做——米诺地尔的心脏安全性顾虑限制了剂量,非那雄胺的激素副作用框死了它的边界,真正干净的新机制药物又迟迟未到。
02
Study 302临床数据深度拆解
VDPHL01这款米诺地尔的缓释口服片,来自Veradermics专有的缓释平台。
其核心逻辑在于:米诺地尔的活性代谢物(米诺地尔硫酸盐)在毛囊局部的SULT1A1酶催化下生成,起效浓度阈值约1.62 ng/mL,而心脏活动阈值约20 ng/mL——两者之间有10倍窗口。缓释技术的价值,是把血药浓度维持在生发有效区间内更长时间(约为即释片的2倍),同时将Cmax压低至心脏活动阈值以下,规避即释口服米诺地尔的心血管风险。如此PK设计的巧思,令人赞叹不已。
然后主要终点上,其实这个是值得细究的。因为虽然FDA从90年代开始把TAHC这个指标用作脱发药物的主要终点,但是它只反映一个1cm²小区域的变化,不能代表整个头皮的情况。更重要的是,它是一个替代终点——发数增加不等于患者主观感受到改善,这也是为什么监管机构越来越要求同时纳入PRO(患者自报结局)作为co-primary endpoint,Study 302的设计正是如此。
主要终点上数字摆在就这里:
Study 302的两个共同主要终点均已经达到,p<0.0001。在非绒毛发目标区域发数(TAHC)方面,安慰剂组+7.3 hairs/cm²,QD组+30.3,BID组+33.0——安慰剂调整后Δ分别为+23.1和+25.8。患者自报(PRO,AAIRS量表≥+2分)方面,安慰剂组13.4%,QD组48.4%,BID组62.9%。这两组数字的差距,不像临床试验常见的那种统计学显著但临床意义存疑的情形。
在次要终点上,QD和BID两组在第2个月即与安慰剂实现统计学显著分离——这对于一个此前标准为4-12个月才能见到临床意义疗效的领域来说,是一个真正有意义的差异化。研究者整体评估(IGA)中重度改善应答率:安慰剂10.7%,QD 39.5%,BID 56.0%(p<0.0001)。
而更为惊艳的,或许是它的安全性。
总TEAE发生率:QD 45.6%,BID 40.6%,安慰剂42.2%——三组相当。零治疗相关SAE,零心源性AESI(特别关注不良事件)。外周水肿(QD 5.3%,BID 6.3%,安慰剂0%)和多毛症(QD 3.5%,BID 6.3%)是米诺地尔类药物的已知效应,均未导致显著停药率(外周水肿致停药率1.1-1.2%,多毛症未致停药)。没有心率、血压或ECG的临床显著异常。
与其它药物的数据对比表格如下图所示:
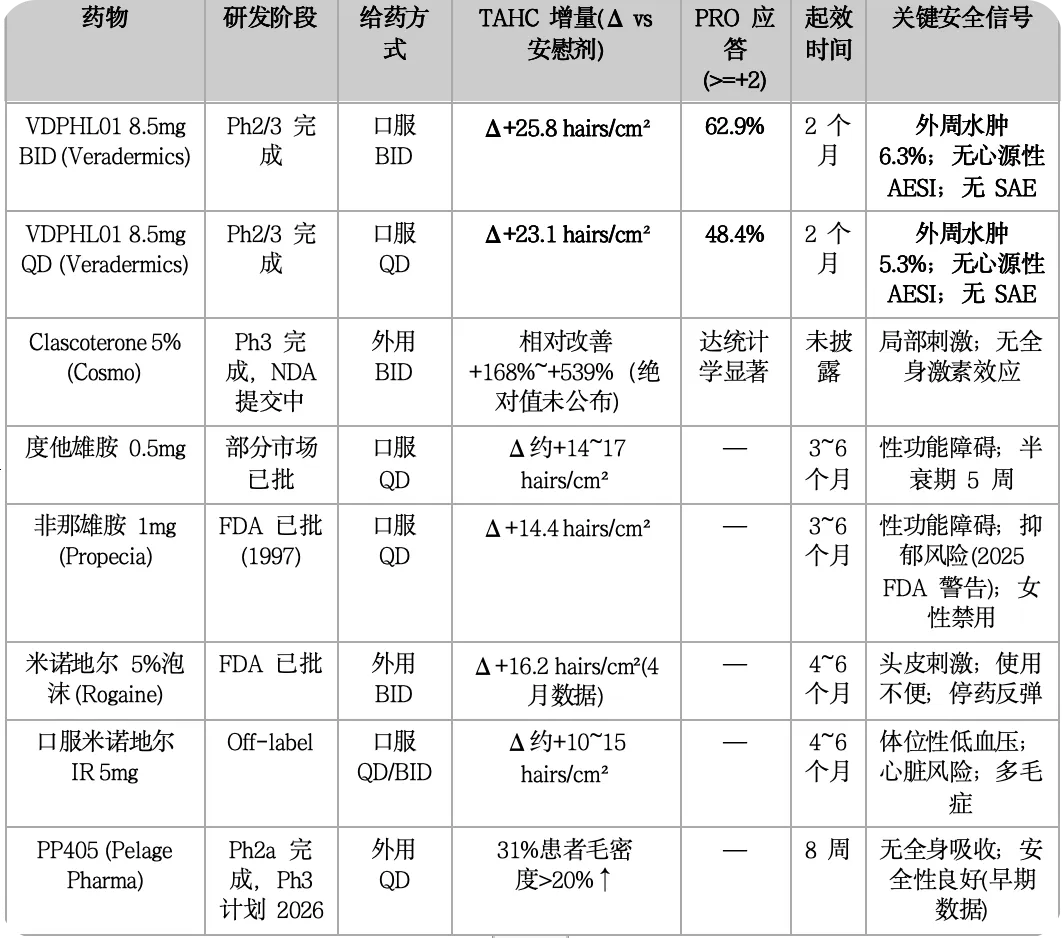
VDPHL01的市场规模估算上:
Veradermics的市场分析显示,美国PHL患者约8000万,其中可寻址市场约7400万(扣除约600万无法诊断/治疗人群)。市场调研(n=153名HCP,190名患者)显示:73%的医生在获知数据后表示高度愿意开具处方,并预计其患者中约52%的男性AGA患者会接受VDPHL01治疗。
以bottom-up逻辑简单估算:当前约100万Rx患者(走处方药渠道的患者),假设渗透提升至5%,按月费用约150美元(参考口服非那雄胺定价)×12个月,约为9000万美元/年潜在近期Rx峰值。若渗透率进一步向OTC换药和治疗空白患者延伸(约1400万OTC患者),按10%渗透率估算,潜在销售峰值可超过25亿美元/年。女性适应症(Study 306正在招募)一旦落地,市场天花板将进一步上移——目前美国3000万女性PHL患者目前无任何FDA批准的口服治疗选项。
确证性Phase 3(Study 304)数据预计2026年下半年公布,Study 302 Part B延伸期数据亦在同期披露。
03
中国生发市场情况
Veradermics的故事发生在大洋彼岸,但中国市场,正悄然催生出另外的脱发治疗的高阶玩家。
2024年1月,三生制药(01530.HK)旗下浙江万晟药业宣布,蔓迪5%米诺地尔泡沫剂获NMPA批准上市——中国第一个本土获批的米诺地尔泡沫剂型,也是唯一一个。
中国药学会数据显示,按销售额计,蔓迪2023年上半年在中国内地米诺地尔酊市场中拥有70.3%的市场份额;整体脱发药物市场占有率达57%,米诺地尔细分领域更是达到71%。米诺地尔类产品2023年在中国三大终端六大市场合计销售额超25亿元,其中蔓迪以超60%的份额领跑。
财务面:2022年至2024年,蔓迪国际营收从9.82亿元增至14.55亿元,净利润从2.02亿元增至3.90亿元,复合增长率分别21.7%和39.1%。2025年上半年净利润1.74亿元,同比增长64.10%。
并且,其新新剂型蔓迪泡沫剂相比传统酊剂,不含丙二醇(减少过敏瘙痒),泡沫密度低、附着性强、给药精准。更关键的是,头皮下蓄积率高于溶液剂,透皮速度可提高9倍以上。临床等效性试验已证明其与Rogaine具有相当疗效,并达到预设统计学终点。
此外,科笛的脱发管线也达到了临床终点,SCALP 1试验的TAHC相对改善为539%,SCALP 2为168%;PRO方面,一项达到统计学显著性,另一项显示积极趋势,联合分析达到统计学显著。12个月持续用药的患者TAHC持续增长,与6个月后换回安慰剂组相比,改善幅度达到统计学显著的2.39倍;治疗满意度相对改善24.5%(p值显著);安全性与安慰剂组组相当,支持长期慢性使用。科笛将会在2027年向FDA提交上市申请。
结语:在Study 302之前,脱发治疗的叙事是一个关于将就的故事——男人将就着用副作用明显的非那雄胺,女人将就着每天涂抹液体剂,双方都在等一个更好的答案。
VDPHL01的数据,或许就是这个答案开始成形的样子。+33 hairs/cm²,62.9%的患者自报改善,2个月起效,零心源性不良事件——放在三十年的背景下,这组数字足够镇住众人。
30年河东,30年河西,脱发市场该被革命了。

 产业资讯
产业资讯
 医药魔方Info
医药魔方Info  2026-05-04
2026-05-04
 7
7

 产业资讯
产业资讯
 药融圈
药融圈  2026-05-04
2026-05-04
 4
4

 产业资讯
产业资讯
 Medaverse
Medaverse  2026-05-04
2026-05-04
 6
6
 热门资讯
热门资讯