 产业资讯
产业资讯
 思宇MedTech
思宇MedTech  2026-04-28
2026-04-28
 7
7
2013年,制药巨头拜耳(Bayer)以11亿美元的代价,意气风发地完成了对Essure的收购。当时的资本市场普遍认为,这是一笔锁定未来十年的优质投资。
仅仅五年后,随着FDA的一纸限令,这款曾被誉为“非手术永久避孕”明星的产品在美国全面退市。
代价是惨痛的: 75万例植入带来的不仅是财务上的11亿美元“打水漂”,更有后续因近4万起法律诉讼而支付的16亿美元巨额赔偿。
从实验室的“绝妙想法”到商业世界的“史诗级亏损”,事情是怎么变成这样的?本文按 产品设计 → 监管路径 → 资本故事 三条主线,梳理它为何从明星产品,走到患者群体集中维权、监管加码、企业撤退与大额和解的结局。结尾给出面向医生与研发团队的“转化要点清单”。
# 产品设计:一个小线圈,为什么在真实世界里失灵?
装置形态与材料构成
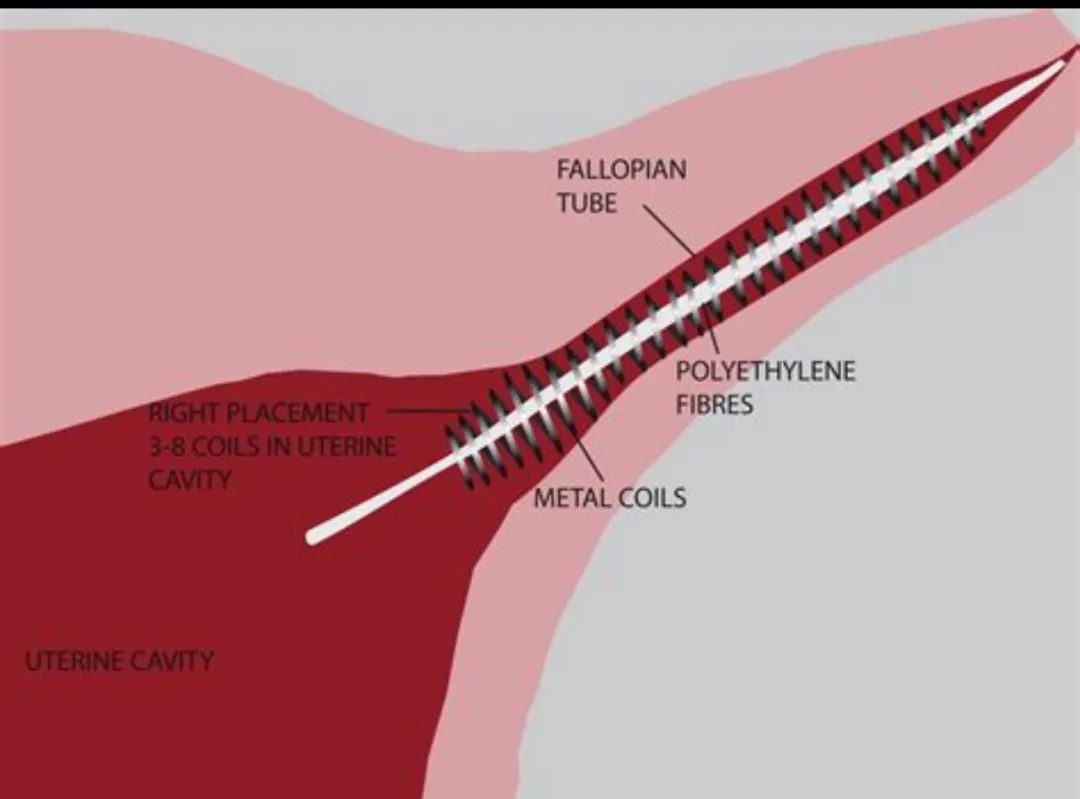
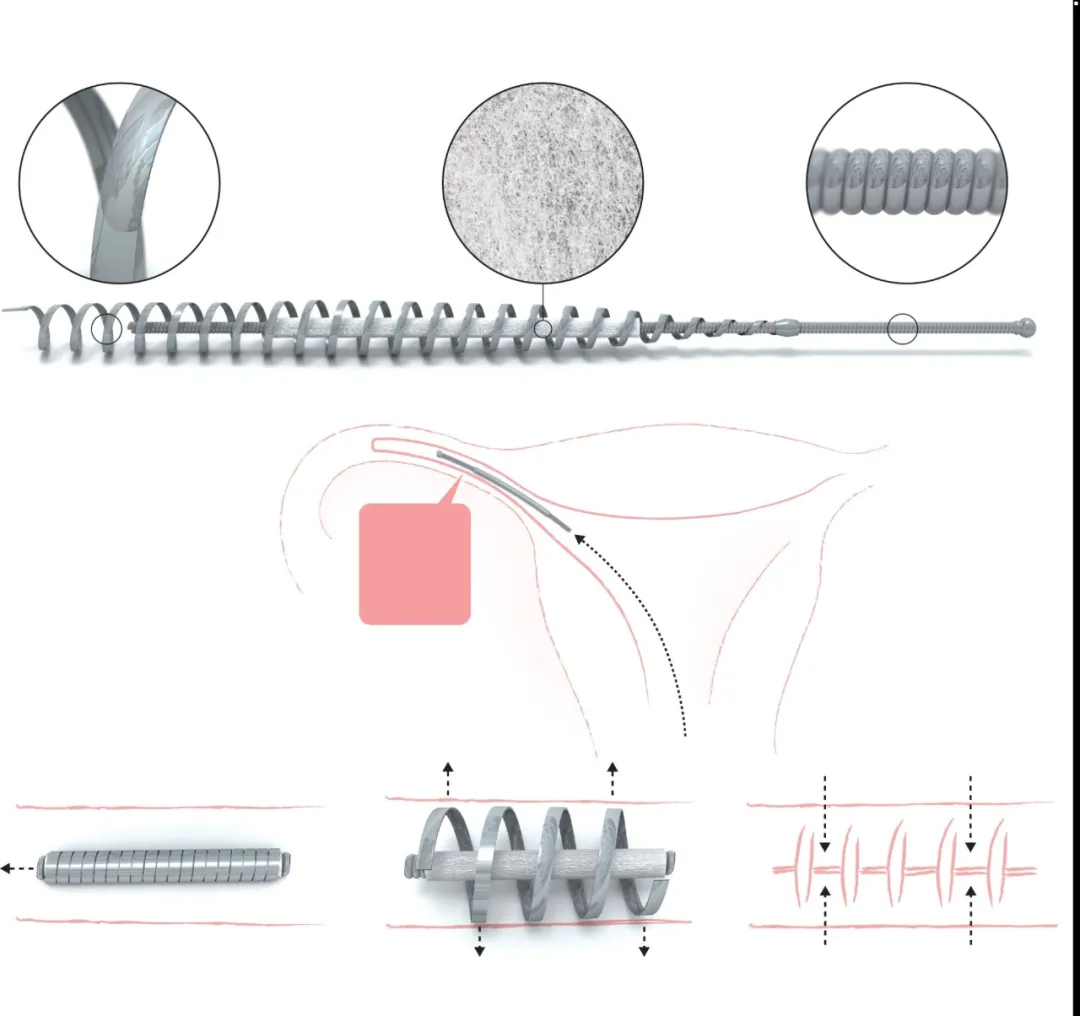
形态:长度约 4 cm 的小型双层螺旋线圈,植入输卵管开口近端,依靠金属的机械撑开力保持位置。
三层结构:
外层线圈:镍钛合金(Nitinol),提供形状记忆与超弹性,保证释放后可自动展开并固定;
内层线圈:不锈钢,起结构支撑作用;
纤维填充:PET(聚对苯二甲酸乙二醇酯)纤维夹在螺旋间隙,诱发局部纤维化,数周至数月内形成瘢痕,永久堵塞输卵管。
植入流程:经阴道,在宫腔镜引导下将装置送抵输卵管口,释放后自动展开;按设计,随时间完成组织性封堵,实现不可逆避孕。

# 真实世界失败的四个关键点
位置不可控
输卵管口解剖差异显著,宫腔镜操作存在角度与视野限制;
偏位/移位 可致穿孔或进入腹腔,避孕失效并引发慢性疼痛或器官损伤。
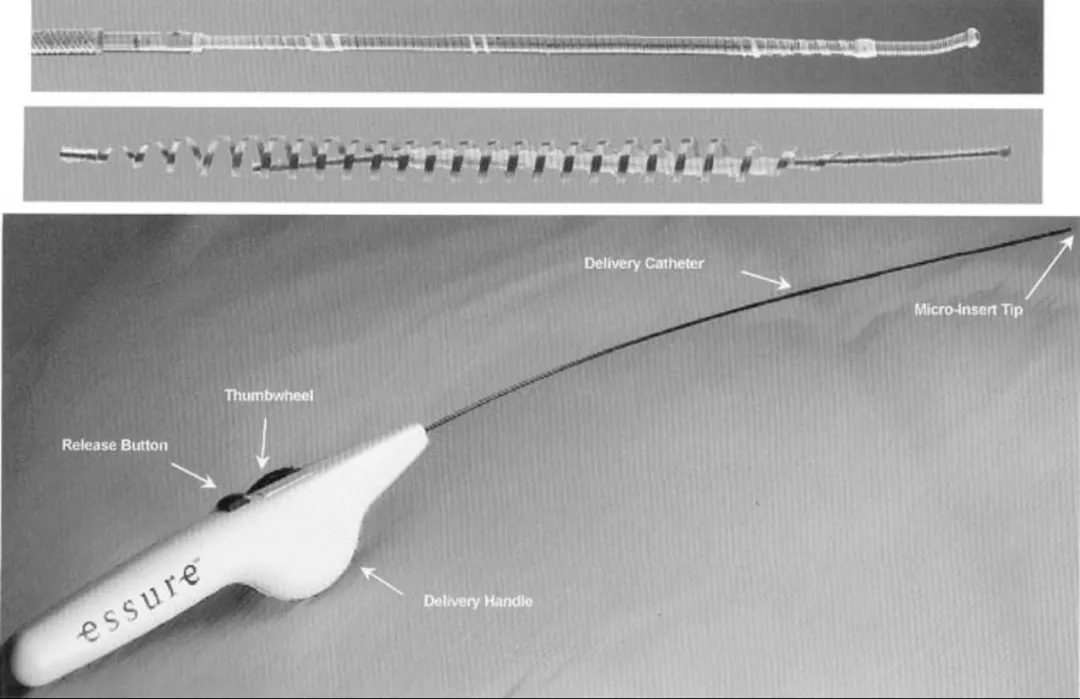
材料相关反应差异大
镍钛合金含镍,部分患者出现过敏或炎症;
在狭小而脆弱的组织中,超弹性的撑开力可能成为局部损伤的诱因。
纤维化机理的个体变异
PET纤维诱发的 “慢性异物反应”,在不同人体内极不稳定。这是导致后续万余起法律诉讼(因慢性疼痛和自身免疫反应)的核心诱因。
纤维化不足 → 避孕失败;
纤维化过度或反应异常 → 慢性疼痛与粘连。
不可逆与取出困难
设计目标就是“永久”,但一旦出现并发症,完整取出极其困难;
取出过程可能导致输卵管/子宫损伤,部分病例不得不行子宫切除。
小结:Essure 的失败不是单一材料或单一形状的问题,而是“用一个不可逆的小线圈,以期在高度多变的解剖环境里获得可控纤维化”这一设计理念在真实世界不可控。位置、材料反应与不可逆共同放大了风险。
# 监管路径:从有限证据的快速批准,到被动加码的撤市
上市前数据(批准依据)
样本量:核心临床试验约 745 名女性,来源于美欧约 10 个中心;
可评估人群:约 664 名;植入成功率 86%–90%;
避孕有效性:1 年随访有效率接近 99%;
随访长度:主要为 1 年,少量延至 2 年;缺乏 ≥5 年的长期数据;
关键空白:几乎没有系统的撤出可行性与安全性研究。
这些数据足以证明“短期有效”,却不足以证明长期安全——尤其针对不可逆植入物。
批准与上市后要求
2002 年走PMA(III 类)路径通过;
审评投票:10 票赞成、1 票弃权;
附带条件:要求开展至少 5 年、≥2000 人的上市后随访,用于监测长期安全性与有效性。
上市后监测的缺口与后续动作
不良事件报告(MDR)长期累积:2000 年代至 2010 年代中期,患者投诉不断增多(慢性盆腔痛、异常出血、移位、穿孔等),但自愿上报体系导致信号分散且滞后;
2015 年召开公开听证会;
2016 年监管加码:
在说明书上加“黑盒警告”;
引入“患者—医生共同决策清单”;
要求新一轮上市后研究;
2018 年 4 月实施销售与使用限制(未履行共识清单流程不得使用),临床采用迅速下滑(随后销量约下降 70%);
2018 年 12 月 31 日起停止在美国销售与分销;
之后监管要求企业持续提交“522”上市后研究进展;但由于失访与随访质量等问题,进展长期被评估为不充分。
MDR 年度数据概览(用于把握风险暴露节奏)
2017 年:约 11,854 份
2018 年:约 6,000 份
2019 年:约 15,083 份
2020 年:约 16,086 份
2021 年:约 3,701 份
2022 年:约 1,606 份
2023 年:约 3,626 份
2024 年:约 803 份
说明:部分年份的尖峰与下降,与集中补报/诉讼推动有关,不能简单等同于真实发生率变化,但能反映风险认知与监管关注的节奏。
小结:这是一个典型的“前期证据不足—放行→后期靠被动上报—发酵→监管加码—急刹车”的轨迹。
# 市场与资本:大规模采用、舆论拐点与一笔失败的收购
采用规模与舆论转折
采用规模:到宣布停售时,全球累计植入超过 75 万例,多数发生在美国;
患者行动与社会监督:患者在社交媒体组群集中发声,纪录片和媒体调查形成舆论拐点,推动监管加码与医生观念转变;
销量的“刹车点”:2018 年限制性措施落地后,销量约降 70%,渠道与使用条件的收紧直接改变了临床采用节奏。
并购与财务后果
并购进入:2013 年,拜耳以约 11 亿美元收购开发商 Conceptus,将 Essure 作为女性健康业务的旗舰之一;
退出代价:
2018 年美国停止销售;
2020 年就美国近 3.9 万起索赔达成约 16 亿美元和解(不承认过错);
投资结果:从“买入—推广—撤退—和解”的现金流视角看,该交易呈明显负回报;除直接成本外,还伴随品牌、法务与合规的长期外溢成本。
小结:当产品处在快速放量阶段而长期证据不牢时,规模越大,风险外溢越快;并购尽调若低估上市后真实世界证据与声誉/诉讼风险,容易把业务增长期的“资产”变成撤退期的“负担”。
关键时间轴
1997–2001:核心临床研究(约 745 例,1–2 年随访为主)
2001:获欧洲 CE 标志
2002:美国 PMA 批准(10 赞成/1 弃权;附带 5 年、≥2000 人随访要求)
2013:拜耳以约 $1.1B 收购 Conceptus
2015:听证会,患者与医生质疑安全性
2016:加贴黑盒警告,引入共同决策清单
2017:多国暂停/撤市
2018.04:实行销售与使用限制(销量随后约降 70%)
2018.12.31:在美国停止销售与分销
2020:就~3.9 万起索赔达成约 $1.6B 和解;继续“522”随访
2021–2024:随访进度长期被评估为不充分,MDR 报告量逐年回落
给创新团队与临床研发者的“转化要点清单”
不可逆=证据门槛更高:设计成“永久”的植入物,必须在长期安全性与撤出路径上给出同等级别的证据与预案。
位置与力学可控性优先:在微小、脆弱、差异大的解剖区域,固定机制与释放力要有冗余与缓冲,尽量避免“硬撑”。
把个体反应当作一级风险:对材料过敏、纤维化变异等,需入组前评估—术后监测—再干预策略三段闭环。
上市后证据是“第二次临床试验”:RWE(真实世界证据)与主动监测要内嵌到商业化流程,避免被动应对。
监管交互“前置化”:用风险管理计划(RMP)+ 取出 SOP + 患者知情工具,把“最坏情况”写在前面。
并购尽调拉高非财务权重:把上市后证据质量、诉讼/声誉风险与财务指标等权审视,防止“滞后爆雷”。
# 结语
Essure 的故事让我们看到:设计的不确定性、监管的迟缓、资本的乐观一旦同频,就会把“小概率并发症”放大为系统性失败。对正在开展创新的团队而言,最好的致敬不是回避,而是把这类失败写进流程、写进标准、写进尽调与决策,让每一代产品都更稳、更安全。

 产业资讯
产业资讯
 思宇MedTech
思宇MedTech  2026-04-28
2026-04-28
 7
7

 产业资讯
产业资讯
 深蓝观
深蓝观  2026-04-28
2026-04-28
 7
7

 产业资讯
产业资讯
 药智网
药智网  2026-04-28
2026-04-28
 7
7
 热门资讯
热门资讯